
【题目】下列合成有机高分子材料的化学方程式和反应类型都正确的是( )
A.nCH2=CH-CN![]()
![]() 加聚反应
加聚反应
B.![]() 缩聚反应
缩聚反应
C.nCH2=CH2+nCH2=CH-CH3![]()
![]() 缩聚反应
缩聚反应
D.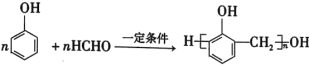 缩聚反应
缩聚反应
【答案】B
【解析】
A.—CN应为支链,碳碳单键可以旋转;
B.乙二酸与乙二醇发生缩聚反应生成高聚物;
C.烯烃发生加聚反应;
D.甲醛与苯酚发生缩聚反应生成高聚物,同时产生水。
A.碳碳单键可以旋转,断开双键的碳原子彼此连接,形成的生成物为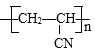 ,A错误;
,A错误;
B.乙二酸与乙二醇发生缩聚反应生成高聚物,反应方程式的书写和反应类型的判断符合反应事实,B正确;
C.烯烃断开双键中较活泼的键,然后这些不饱和碳原子彼此连接形成高聚物,发生的反应类型为加聚反应,不是缩聚反应,C错误;
D.苯酚与甲醛发生缩聚反应形成酚醛树脂和水,反应方程式为n![]() +nHCHO
+nHCHO![]()
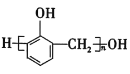 +(n-1)H2O,缺少小分子水,不符合质量守恒定律,D错误;
+(n-1)H2O,缺少小分子水,不符合质量守恒定律,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】生活中常见的荧光棒的发光原理可用下式表示,该反应产生的能量传递给荧光染料,再由染料发出荧光。下列说法正确的是( )
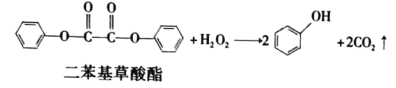
A..上述反应是酯的水解反应
B.二苯基草酸酯的一溴代物有3种
C.二苯基草酸酯在酸性条件下水解生成三种有机物
D.二苯基草酸酯与草酸(![]() )互为同系物
)互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )
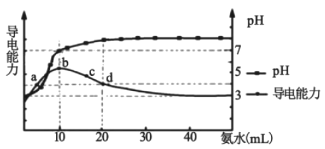
A. 各点溶液中的阳离子浓度总和大小关系:d>c>b>a
B. 常温下,R- 的水解平衡常数数量级为10 -9
C. a点和d点溶液中,水的电离程度相等
D. d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)26H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
(资料1)
沉淀 | Fe(OH)2 | Fe(OH)3 |
开始沉淀 pH | 7.6 | 2.7 |
完全沉淀 pH | 9.6 | 3.7 |
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________。
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
实验1 | pH=1 | pH=5 | 8.4 |
实验2 | pH=1 | pH=1 | 6.5 |
实验3 | pH=6 | pH=5 | 7.8 |
实验4 | pH=6 | pH=1 | 5.5 |
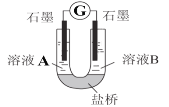
(资料2)原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
(资料3)常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对(资料3)实验事实的解释为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1,2-二氯乙烷在常温下为无色液体,沸点为83.5 ℃,密度为1.23 g·mL-1,难溶于水,易溶于醇、醚、丙酮等有机溶剂;乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如图所示的实验装置。请回答下列问题:

(1)为了检查整套装置的气密性,某同学将导气管末端插入盛有水的烧杯中,用双手捂着装置A中大试管,但该方法并不能准确说明装置的气密性是否良好。则正确检查整套装置气密性的方法是_______________。
(2)向装置A中大试管里先加入1,2-二氯乙烷和NaOH的乙醇溶液,再加入______,目的是______,并向装置C中试管里加入适量稀溴水。
(3)为了使反应在75 ℃左右进行,常用的方法是_______________________________。
(4)与装置A中大试管相连接的长玻璃管的作用是______,装置B的作用是______。
(5)能证明1,2-二氯乙烷已发生消去反应的实验现象是______,装置A、C中发生反应的化学方程式分别为_________________________;________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯的结构简式为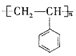 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的分子式为__________,链节是____________,单体是_________________。
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度![]() 为________。
为________。
(3)一定条件下合成聚苯乙烯的化学方程式为______,该反应类型为_______反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某中草药提取的有机物结构如图所示,该有机物的下列说法中错误的是( )
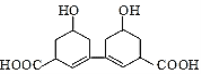
A.分子式为C14H18O6
B.1mol该有机物最多可与2mol的H2发生加成反应
C.既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应
D.1mol该有机物最多可反应2mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃分子中若含有双键、叁键或环,其碳原子所结合的氢原子则少于同碳原子数对应烷烃所含的氢原子数,亦具有一定的不饱和度![]() 用
用![]() 表示
表示![]() 。下表列出几种烃的不饱和度:
。下表列出几种烃的不饱和度:
有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
| 1 | 2 | 1 | 4 |
据此下列说法不正确的是![]()
![]()
A.![]() 的不饱和链烃再结合6molH即达到饱和
的不饱和链烃再结合6molH即达到饱和
B.![]() 的
的![]() 等于6
等于6
C.![]() 与环丁烷的不饱和度相同
与环丁烷的不饱和度相同
D.![]() 的不饱和度与
的不饱和度与![]() 、
、![]() 的不饱和度相同
的不饱和度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或折开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为

A.-1 638 kJ/molB.+1 638 kJ/molC.-126 kJ/molD.+126 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com