
【题目】(1)工业上制取纯净的CuCl2·2H2O的主要过程是
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;
②对①所得滤液按下列步骤进行操作:
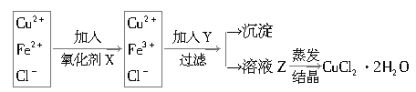
已知:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ mol3·L-3 | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
请回答下列问题:
①加入的氧化剂X,下列物质最好选用的是 ______ .
A.KMnO4 B.H2O2 C.氯水D.HNO3
②加入Y的作用是___________________________,Y的化学式为____________。
③溶液乙在蒸发结晶时应注意:________________________________。
(2)如图为相互串联的甲、乙两个电解池,试回答下列问题:
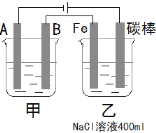
甲池若为用电解原理精炼铜的装置,阴极增重19.2 g,则乙池阳极放出气体在标准状况下的体积为__________L(不考虑气体的溶解情况)
【答案】BC 调节PH值使Fe3+沉淀完全 CuO或Cu(OH)2或CuCO3 或Cu2(OH)2CO3 在HCl气流中加热蒸发 6.72
【解析】
(1)①根据流程,加入氧化剂X后,只有Fe2+被氧化成Fe3+,没有引入新的杂质,据此分析;
②根据流程的目的,以及表格中的数据,加入Y的目的是调节pH,使Fe3+以Fe(OH)3形式沉淀出来,加入Y不能引入新的杂质,据此分析;
③Cu2+以水解,因此加热蒸发时注意防止Cu2+水解;
(2)该装置为电解池,根据电解原理,甲为精炼铜,A为阴极,纯铜作阴极,电极反应式为Cu2++2e-=Cu,B为阳极,粗铜作阳极,电极反应式为Cu-2e-=Cu2+,Fe为阴极,碳棒为阳极,书写出电极反应式,根据电子守恒进行计算;
(1)①加入氧化剂X后,除Fe2+转化成Fe3+外,其余离子不发生变化,试剂X可以是Cl2、H2O2等氧化剂,使用KMnO4引入K+、Mn2+杂质,使用HNO3,引入NO3-,且产生氮的氧化物,对环境与污染;
②加入Y后过滤,除去Fe元素,根据表格中数据,加入Y的目的是调节pH,使Fe3+以Fe(OH)3形式沉淀出来;加入的Y,能与H+发生反应,为不引入新杂质,加入物质不溶于水,即Y可以是CuO也可以是Cu(OH)2、CuCO3、Cu2(OH)2CO3;
③Cu2+能发生水解,加热促进其水解,因此蒸发结晶为防止Cu2+水解,需要在HCl气流中加热蒸发;
(2) 该装置为电解池,根据电解原理,甲为精炼铜,A为阴极,纯铜作阴极,电极反应式为Cu2++2e-=Cu,B为阳极,粗铜作阳极,电极反应式为Cu-2e-=Cu2+,Fe为阴极,碳棒为阳极,阳极反应式为2Cl-2e-=Cl2↑,根据得失电子数目守恒,建立Cu~2e-~Cl2↑,因此乙池中阳极放出气体在标准状况下的体积为![]() =6.72L。
=6.72L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有下列五组物质:
①O2和O3;②![]() 和
和![]() ;③CH3CH2CH2CH3与
;③CH3CH2CH2CH3与![]() ;④
;④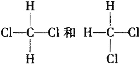 ;
;
⑤C2H6与C7H16
(1)___组两种物质互为同位素;
(2)____组两种物质互为同素异形体;
(3)_____组两种物质互为同系物;
(4)____组两种物质互为同分异构体;
(5)_____组两种物质实质上是同一种物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应4HCl(g)+O2(g)═2Cl2(g)+2H2O(g),已知2 mol O2被还原时,放出a kJ的热量,且知断开1 mol O=O键需要吸收b kJ的热量,断开1 mol Cl—Cl键需要吸收c kJ的热量。则断开1 mol H—O键比断开1 mol H—Cl键所需能量高
A. (b-a-2c)/4kJB. (a+2b-4c)/8kJC. (a+b-2c)/4kJD. (2b-a-4c)/8kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2 (g)+3H2(g)![]() 2NH3(g)ΔH<0。该反应的速率与时间的关系如下图所示:如果t2、t4、t6、t8时都只改变了一个反应条件,则对应t2、t4、t6、t8时改变条件的判断正确的是( )
2NH3(g)ΔH<0。该反应的速率与时间的关系如下图所示:如果t2、t4、t6、t8时都只改变了一个反应条件,则对应t2、t4、t6、t8时改变条件的判断正确的是( )

A.增大反应物浓度、使用了催化剂、减小压强、升高温度
B.升高温度、减小压强、减小反应物浓度、使用催化剂
C.使用催化剂、增大压强、减小反应物浓度、降低温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2![]() CH3OH(g)。该可逆反应达到平衡的标志是________。
CH3OH(g)。该可逆反应达到平衡的标志是________。
A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
0 | 0.40 | 1.00 | 0 | 0 |
5 | a | 0.80 | c | 0.60 |
7 | 0.20 | b | 0.20 | d |
10 | 0.21 | 0.81 | 0.19 | 0.64 |
请回答下列问题:
①该温度下,上述反应的平衡常数K=________;
②反应在7~10min内,CO的物质的量减少的原因可能是____________(填字母)。
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向_____(填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,则a的取值范围为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.将1mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为![]()
B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
D.某电池的总反应为Fe+2Fe3+=3Fe2+,当有5.6gFe溶解时电路中有0.2mol e-通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
A.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2
B.电池的电解质溶液为碱性溶液,阳离子向正极移动
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A.18g冰(图1)中含O—H键数目为2NA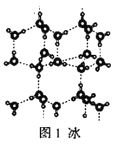
B.28g晶体硅(图2)中含有Si—Si键数目为2NA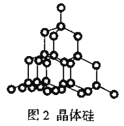
C.44g干冰(图3)中含共用电子对2NA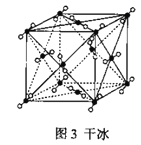
D.石墨烯(图4)是碳原子单层片状新材料,12g石墨烯中含C—C键数目为1.5NA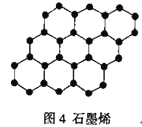
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某项目学习小组在实验失室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:
①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应.温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O。
5Cl-+ClO3-+3H2O。
该项目小组设计了下列实验装置,进行实验。
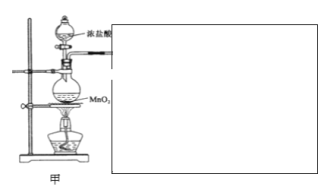
请回答下列问题:
(1)甲装置用于制备氯气。
①请你将装置在图中方框中补充完整___(并标明所加药品)
②该项目小组用100mL12mol/L盐酸与8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2的物质的量为___。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,原因有二:
①部分氯气未与石灰乳反应而逸出;
②___。
(3)为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为如图(不考虑氯气和水的反应)。
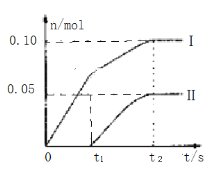
①图中曲线I表示___离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为___。
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37mol,则产物中![]() =___(填比值)。
=___(填比值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com