
【题目】关于丙烯醛(CH2=CH﹣CHO)的下列叙述中,不正确的是( )
A.在丙烯醛分子中,含有两种官能团
B.丙烯醛能发生加聚反应,生成高聚物 ![]()
C.等物质的量的丙烯醛和丙醛完全燃烧,消耗等物质的量的O2
D.丙烯醛能使溴水褪色,能使酸性高锰酸钾溶液褪色
【答案】C
【解析】解:A.该有机物中含有醛基和碳碳双键两种官能团,故A正确;
B.丙烯醛碳碳双键能发生加聚反应生成高分子化合物,生成高聚物 ![]() ,故B正确;
,故B正确;
C.1molCH2=CH﹣CHO消耗氧气为1mol×(3+ ![]() ﹣
﹣ ![]() )=3.5mol,1molC3H6O消耗氧气为1mol×(3+
)=3.5mol,1molC3H6O消耗氧气为1mol×(3+ ![]() )=4mol,则等物质的量的丙烯醛和丙醛完全燃烧,消耗氧气的物质的量不等,故C错误;
)=4mol,则等物质的量的丙烯醛和丙醛完全燃烧,消耗氧气的物质的量不等,故C错误;
D.碳碳双键能与溴发生加成反应、能被酸性高锰酸钾溶液氧化,醛基能被溴、酸性高锰酸钾溶液氧化,所以丙烯醛能使溴水、酸性高锰酸钾溶液褪色,故D正确;
故选C.
【考点精析】本题主要考查了有机物的结构和性质的相关知识点,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】实验室用少量的溴水和足量的乙醇制备1,2﹣二溴乙烷的装置如下图所示: 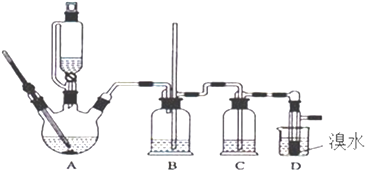
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣l30 | 9 | ﹣1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式 .
(2)装置B的作用是 .
(3)在装置C中应加入(填字母). a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2 , 最好用(填字母)洗涤除去. a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是 .
(7)判断该制备反应已经结束的最简单方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属Fe和金属钙Ca,并含有3.5%(质量分数)CaO.
(1)Ca的原子结构示意图为 . 其最高价氧化物对应水化物的碱性比Mg(OH)2(填“强”或“弱”).
(2)Ca与非金属性最强的元素A形成化合物D,写出D的电子式
(3)配平用“金属钙线”脱氧脱磷的方程式:
P+FeO+Cao ![]() Ca3(PO4)2+
Ca3(PO4)2+
(4)将“金属钙线”溶于稀盐酸后,再滴加双氧水发生的离子方程式是 .
(5)取3.2g“金属钙线”试样,与水充分反应生成448mL H2(标准状况),在所得溶液中通入适量CO2 , 最多能得到CaCO3g(取两位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学查阅文献,并用图装置进行实验. ⅠSO2不能与BaCl2反应;ⅡBaSO3是白色难溶于水的物质,但可溶解于盐酸.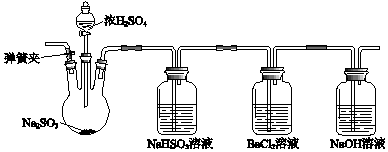
(1)该实验制备SO2的化学方程式是 .
(2)BaCl2溶液中出现了不溶于稀盐酸的白色沉淀,该沉淀可能是 .
(3)甲同学认为出现白色沉淀是由于装置中存在O2 , 排除干扰的方法是 .
(4)按照(3)中改进后的方法重新进行实验,现象是 , 实验结论与文献一致.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.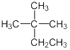 的系统命名为2﹣甲基﹣2﹣乙基丙烷
的系统命名为2﹣甲基﹣2﹣乙基丙烷
B.用酸性KMnO4溶液可以确定CH2=CH﹣CHO中含有C=C双键
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义.
(1)用CO可以合成甲醇.已知:
CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2O(l)△H 1 kJmol﹣1
O2(g)═CO2(g)+2H2O(l)△H 1 kJmol﹣1
CO(g)+ ![]() O2(g)═CO2(g)△H2 kJmol﹣1
O2(g)═CO2(g)△H2 kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(l)△H3 kJmol﹣1
O2(g)═H2O(l)△H3 kJmol﹣1
则CO(g)+2H2(g)CH3OH(g)△H=kJmol﹣1 .
(2)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2 , 在催化剂作用下发生反应:CO(g)+2H2(g) CH3OH(g)△H,平衡转化率与温度、压强的关系如图1所示. 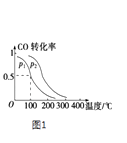
①下列说法正确的是
A.若容器内气体密度恒定,反应达到平衡状态
B.若容器内各气体浓度恒定,反应达到平衡状态
C.上述反应中,△H>0
D.反应中,催化剂使平衡向正反应方向移动
②p2p1 (填“大于”、“小于”或“等于”);
③100℃时,该反应的化学平衡常数K=;
(3)某科研小组用SO2为原料制取硫酸.
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池负极的电极反应式: .
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸.电解原理示意如图2所示.请写出开始时阳极反应的电极反应式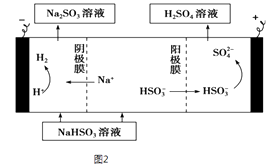
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的好似( )
A.已知2H2O(l)═2H2(g)+O2(g)△H=+571.6KJmol﹣1 , 无法求H2的燃烧热
B.已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性
C.已知500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放出19.3KJ的热量,无法推出该反应的热化学方程式
D.已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2 , 无法得出△H2>△H1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的多种化合物在工业中有重要的应用.
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性.
①Na2S2O4中S元素的化合价为 .
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为(填化学式).
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2 . 该反应的化学方程式为 .
(2)铬会造成环境污染.某酸性废水中含有Cr2O72﹣ , 处理时可用焦亚硫酸钠(Na2S2O3)将Cr2O转化为毒性较低的Cr3+ , 再调节pH至8,使铬元索沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg/L,达到排放标准.
①Na2S2O3参加反应的离子方程式为 .
②处理后的废水中Cr3+的物质的量浓度为mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com