
����Ŀ������ͭ��һ����Ũ���ᷴӦ���õ�����ͭ��Һ��NO2��NO�Ļ������4.48L(����������ڱ�״���²ⶨ����ͬ)����Щ������һ�����������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᣬ������������ͭ��Һ�м���5mol/LNaOH��Һ��Cu2+ǡ����ȫ����������NaOH��Һ�������60mL������˵������ȷ����![]()
![]()
A.�˷�Ӧ������ת�Ƶĵ���Ϊ0.6mol
B.���������������1.68L
C.��������к�NO23.36L
D.�μӷ�Ӧ��������0.5mol
���𰸡�A
��������
�����4.48LNO2��NO�����������ʵ���Ϊn=![]() =0.2mol��60mL5mol/L������������Һ���������Ƶ����ʵ���Ϊn(NaOH)=5mol/L��0.06L=0.3mol��
=0.2mol��60mL5mol/L������������Һ���������Ƶ����ʵ���Ϊn(NaOH)=5mol/L��0.06L=0.3mol��
A.����Cuʧȥ���ӵ���O2��õĵ��ӵ����ʵ�������OH-�����ʵ������㣻
B.����OH-�غ��֪����������ͭ�����ʵ���Ϊn[Cu(OH)2]=0.3mol��![]() =0.15mol����Ӧ���ĵ�ͭ�����ʵ���Ϊ0.15mol��0.15molͭ��ȫ��Ӧʧȥ0.3mol���ӣ����ݵ����غ㣬�����õ��ĵ�����ͭʧȥ�ĵ���һ����ȣ����ݵ����غ����������������ʵ������ټ�����������
=0.15mol����Ӧ���ĵ�ͭ�����ʵ���Ϊ0.15mol��0.15molͭ��ȫ��Ӧʧȥ0.3mol���ӣ����ݵ����غ㣬�����õ��ĵ�����ͭʧȥ�ĵ���һ����ȣ����ݵ����غ����������������ʵ������ټ�����������
C.��NO�����ʵ���Ϊx���������������ʵ���Ϊy���ֱ����������������غ���ʽ����
D.ͭ����ǡ�ó���ʱ����Ӧ�������Ϊ�����ƣ������������غ��֪����������������ӵ����ʵ���Ϊ0.3mol���ٸ��ݵ�ԭ���غ�ɵ���������ʵ�����
n��������壩=![]() =0.2mol��60mL5mol/L������������Һ���������Ƶ����ʵ���Ϊn(NaOH)=5mol/L��0.06L=0.3mol��
=0.2mol��60mL5mol/L������������Һ���������Ƶ����ʵ���Ϊn(NaOH)=5mol/L��0.06L=0.3mol��
A.�ڷ�Ӧ��Cuʧȥ���ӱ�ΪCu2+��������Cu2+���OH-����Cu(OH)2�������ɼ���Ӧ�����е���ת�Ƶ����ʵ������ڷ�Ӧ���ĵ�NaOH�����ʵ�������˷�Ӧת�Ƶĵ���Ϊ0.3mol��A����
B.����������ͭ�����ʵ���n[Cu(OH)2]=0.3mol��![]() =0.15mol����Ӧ���ĵ�ͭ�����ʵ���Ϊ0.15mol��0.15molͭ��ȫ��Ӧʧȥ0.3mol���ӣ����ݵ����غ㣬�����õ��ĵ�����ͭʧȥ�ĵ���һ����ȣ����������������ʵ���n(O2)=
=0.15mol����Ӧ���ĵ�ͭ�����ʵ���Ϊ0.15mol��0.15molͭ��ȫ��Ӧʧȥ0.3mol���ӣ����ݵ����غ㣬�����õ��ĵ�����ͭʧȥ�ĵ���һ����ȣ����������������ʵ���n(O2)=![]() mol=0.075mol�������ı�������������V(O2)=22.4L/mol��0.075mol=1.68L��B��ȷ��
mol=0.075mol�������ı�������������V(O2)=22.4L/mol��0.075mol=1.68L��B��ȷ��
C.��NO�����ʵ���Ϊx��NO2�����ʵ���Ϊy����x+y=0.2mol�����ݵ����غ�ɵã�3x+y=0.3mol����ã�x=0.05mol��y=0.15mol�����������ж������������V(NO2)=0.15mol��22.4L/mol=3.36L��C��ȷ��
D.ͭ����ǡ�ó���ʱ����Ӧ�������Ϊ�����ƣ������������غ��֪����������������ӵ����ʵ���Ϊ0.3mol�����ݵ�ԭ���غ�ɵ���������ʵ���Ϊ��0.3mol+0.2mol=0.5mol��D��ȷ��
�ʴ�ѡA��


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1��Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����һ�ֻ�ѧԪ�ء�
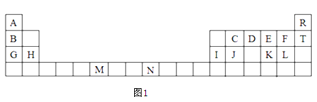
�Իش��������⣺
��1��F-�Ľṹʾ��ͼ��__��
��2��D����̬�⻯���VSEPRģ��Ϊ___��������ԭ�ӵ��ӻ�����Ϊ___�����ӵĿռ乹��Ϊ___��
��3��G��H��I�ĵ�һ��������ֵ�ɴ�С��˳��Ϊ��___(��Ԫ�ط�������)��
��4��Ԫ��M�Ļ�����(MO2Cl2)���л��ϳ��п������������Ȼ��������������л��ﷴӦ����ش��������⣺
����Mͬ���ڵ�����Ԫ�صĻ�̬ԭ����������������Mԭ����ͬ��Ԫ�ػ���____(��Ԫ�ط���)��
��MO2Cl2������Ϊ���ɫҺ�壬����CCl4��CS2�Ȼ��ܣ��ݴ˿��ж�MO2Cl2��___(���������������Ǽ�����)���ӡ�
����C2H4��CH3Cl��CH2O��CS2��CCl4�����л��������У�̼ԭ�Ӳ�ȡsp2�ӻ��ķ�����___(�����ʽ)��
��5����֪Ԫ��N���γ�һ�ֺ���ɫ���������ΪNCl3��5NH3��H2O����������е���������N�����ڻ�̬ʱ��������Ų�ʽΪ___������֪��������N���ӵ���λ����6��1mol����������������������Ӧ������3molAgCl��������ʵ�������___��
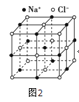
��6����ȥ����JE2Ϊ���������塣JE2�ľ������������Ƶ����Ƚ�NaCl�����е�����Na+ȥ��������Cl-ȫ������Jԭ�ӣ�����ÿ�������������С�����������Ĵ�������һ��Jԭ�ӱ㹹���˾���J��һ����������һ��J�ľ�������___��Jԭ�ӣ�����ÿ�������ڵ�Jԭ��(�������������Jԭ��)�������ߵ��е㴦����һ��Eԭ�ӣ��㹹����JE2��������JE2��������___��Eԭ�ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǹ�˿��֮·�е���Ҫó����Ʒ�������й�˵���������
|
|
|
|
���� | ˿�� | ��Ҷ | �� |
A.�մ�������������ս���ɣ�����Ҫ�ɷ��ǹ�����
B.˿��Ļ�ѧ�ɷ���Ҫ����ά�أ���ά��������Ȼ�л��߷��ӻ�����
C.��Ҷ�к����ַ������ʣ��������ÿɿ���������˥��
D.�ҹ��Ͷ�����������������Ƽ�������������п��ܻẬ�м״����к����ʣ�������ֱ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������;�㷺,��¯�������ܷ�ӦΪ:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g),��ش���������:
2Fe(s)+3CO2(g),��ش���������:
��1��һ���¶���,������̶����ܱ������з���������Ӧ,�����жϸ÷�Ӧ�Ѿ��ﵽƽ�����___________
A.�ܱ���������ѹǿ����
B.�ܱ������л�������ƽ��Ħ����������
C.�ܱ������л��������ܶȲ���
D.c(CO)=c(CO2)
E.Fe2O3���������ٱ仯
��2��һ���¶���,������Ӧ�Ļ�ѧƽ�ⳣ��Ϊ3.0,���¶��½�4molCO��2molFe2O3��6molCO2��5molFe�����ݻ�Ϊ2L���ܱ�������,��ʱ��Ӧ����________________��Ӧ�������(������������������������ƽ��״̬��);��Ӧ��ƽ���,�������¶�,CO��CO2�����������,������ӦΪ______________��Ӧ(��������������������)��
��3����֪:3Fe2O3(s)+CO(g)![]() 2Fe3O4(s)+CO2(g) ��H=�C47kJ/mol
2Fe3O4(s)+CO2(g) ��H=�C47kJ/mol
Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g) ��H=+19kJ/mol
3FeO(s)+CO2(g) ��H=+19kJ/mol
FeO(s)+CO(g)![]() Fe(s)+CO2(g) ��H=�C11kJ/mol
Fe(s)+CO2(g) ��H=�C11kJ/mol
��Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)�� ��H=________________��
2Fe(s)+3CO2(g)�� ��H=________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����ȷ���ǣ� ��
A.NH4HCO3����������������Һ��Ӧ�����ӷ���ʽ��HCO3-+OH-=CO32-+H2O
B.����ˮ������Ӧ�Ļ�ѧ����ʽ��2Fe+3H2O(g)=Fe2O3+3H2
C.FeSO4������Һ��¶�ڿ����У�4Fe2++O2+4H+=4Fe3++2H2O
D.�ƺ�����ͭ��Һ��Ӧ�����ӷ���ʽ��2Na+Cu2+=2Na++Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ȤС����ݽ̲�ʵ����Ƶ�һ����˵��̼������̼���������ȶ��Ե���ʵ�顣��۲�����ͼ��ʾʵ��װ�ã�����ʵ��ԭ�������ж�����˵�������������в���ѧ����(�� )

A. ��ΪС�մ���Ϊ����
B. Ҫ֤��̼�����������ܲ���ˮ������С�Թ�������մ����ˮ����ͭ��ĩ������
C. ���Ȳ��þ��ܿ���A�ձ��ij���ʯ��ˮ�����
D. ����ʵ������ж�û�з���A�ձ��ij���ʯ��ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�������Ϣ���ж�����˵����ȷ���ǣ� ��
A.��NaCl�����У�����Na+�����Cl-�γ���������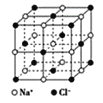
B.����̬�Ŵط��ӵķ���ʽΪE4F4��F4E4
C.CO2������ÿ��������Χ��8�����ڵ�CO2����
D.�ڵ⾧���У�����ӵ�������4�ֲ�ͬ�ķ���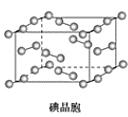
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B�������д̼���ζ�����塣�Ը�������ʵ����ʵ��ա�
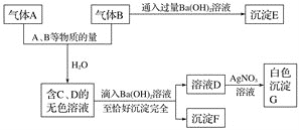
(1)д��A��F�����ʵĻ�ѧʽ��
A__________��B__________��C__________��D__________��E__________��F__________��
(2)д��A��B��ˮ��Ӧ�����ӷ���ʽ��______________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com