
【题目】如图所示,当容器A中的反应开始后,若分别进行下列操作,请回答有关问题:
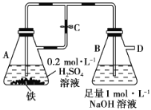
(1)若止水夹C打开,B容器中有什么现象发生:__________________________________________。
(2)若开始时止水夹C关闭,容器A中的反应还在进行时,B容器中有什么现象发生:_________________,写出B容器中有关反应的化学方程式:_____________________。
(3)若先打开止水夹C一段时间,容器A中的反应还在进行时,再关闭止水夹C一会儿,B容器中有什么现象发生:_________________________________________________________。
【答案】 容器B中的导管口有气泡冒出 容器A中溶液进入容器B,容器B中有白色沉淀生成,沉淀迅速变为灰绿色,最后变成红褐色 2NaOH+FeSO4===Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O===4Fe(OH)3 开始时容器B中的导管口有气泡冒出,止水夹关闭后容器A中溶液进入容器B,有白色沉淀生成
【解析】
若弹簧止水夹C打开,则产生的H2经C进入B容器中产生气泡,排出空气。若关闭止水夹C,则反应产生的H2会将A中溶液压入B中而发生反应,若B中无氧气,则发生反应FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;若B中有氧气,则继续发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(1). 若弹簧止水夹C打开,则产生的H2经C进入B容器中产生气泡,排出空气,所以B中的现象是导管口有气泡冒出;
(2) 若开始时止水夹C关闭,仪器中混有部分空气,反应产生的H2会将A中溶液压入B中而发生反应,方程式为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 ,Fe(OH)2为白色沉淀,遇空气中的氧气沉淀迅速变为灰绿色,最后变成红褐色的Fe(OH)3。
(3) 若先打开止水夹C一段时间,容器A中的反应还在进行,排出装置中的空气。若关闭止水夹C,则反应产生的H2会将A中溶液压入B中而发生反应,则发生反应FeSO4+2NaOH=Fe(OH)2↓+Na2SO4。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,图甲是镁-次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是

A. 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
B. 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合,转化成Cr(OH)3除去
C. 图乙电解池中,若有0.84 g阳极材料参与反应,则阴极会有168 mL(标准状况)的气体产生
D. 若图甲燃料电池消耗0.36 g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
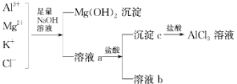
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:_______________________。
(2)氢氧化钠溶液能否用氨水代替,为什么?___________________________。
(3)溶液a中存在的离子有________________;在溶液a中加入盐酸时需控制盐酸的量,为什么?__________________________________。为此,改进方法是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是()
A. 标准状况下,l mol任何物质的体积均为22.4 L
B. CH4的摩尔质量为16 g
C. 1mol H2O的质量为18 gmol-1
D. 1 mol·L-1NaCl溶液的含义是1 L溶液中含有58.5 g NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关电解质溶液的说法正确的是( )
A. 将Na2CO3溶液用水稀释后,pH变大,Kw不变
B. 向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变
C. pH=4.75浓度均为0.1mol/L的CH3COOH、CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)<c(H+)+c(CH3COOH)
D. 分别用pH=2和pH=3 的 CH3COOH溶液中和等物质的量的NaOH,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va=Vb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据下图所示的关系,回答下列问题。

(1)确定A、B、C、D、E、F的化学式,A为________,B为________,C为________,D为________,E为________,F为________。
(2)写出反应⑧的化学方程式和反应④、⑤的离子方程式。
⑧_____________________________________________________;
④_____________________________________________________;
⑤_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器已略)。实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内。在玻璃反应管内装入适量水(使钠块不与水接触)。实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起,使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内。
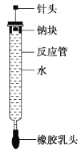
(1)钠与水反应的离子方程式为__________________________________________________。
(2)实验中“钠块熔化为闪亮的小球”说明_____________________;向烧杯中的溶液中滴加____________,溶液变红,说明钠与水反应生成碱性物质。
(3)如果实验前加入反应管内水的体积为a mL,欲使水最终全部被排出,则所取金属钠的质量至少为____________g(设当时实验条件下气体摩尔体积为V mL/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Br位于元素周期表第_____周期第_____族;基态Na+核外有_____种运动状态不同的电子;Mg基态原子核外电子排布式为_____。
(2)用“>”或“<”填空:
第一电离能 | 粒子半径 | 熔点 | 键的极性 |
N_____S | S2—_____ Mg2+ | SO3______Na2O2 | H﹣O_____H﹣N |
(3)已知多硫化钠﹣溴储能电池是一种二次电池,结构如图。电池总反应为:2Na2S3+2NaBr![]() 3Na2S2+Br2。
3Na2S2+Br2。
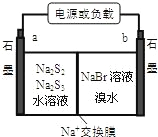
①放电时Na+向_____极迁移(填“a 或 b”);
②充电时阴极电极反应式为:______________。
(4)已知N4为正四面体结构,N﹣N键能为167kJ/mol,N≡N 键能为 942kJ/mol。写 出N4(g)转化为N2(g)的热化学方程式________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com