
【题目】电解质溶液有许多奇妙之处,你只有深入的去思考,才能体会到它的乐趣。下列关于电解质溶液的叙述中正确的是( )
A.浓度相同的![]() 、
、![]() 两种盐溶液中,所有阴离子总浓度后者大
两种盐溶液中,所有阴离子总浓度后者大
B.常温下,1![]() 的
的![]() 溶液与1
溶液与1![]() 的NaOH溶液混合后,所得混合液中:
的NaOH溶液混合后,所得混合液中:![]()
C.物质的量浓度相同的![]() 和
和![]() 两种溶液中,
两种溶液中,![]() 前者小于后者
前者小于后者
D.常温下,某溶液中由水电离出的![]() ,则此溶液可能是盐酸
,则此溶液可能是盐酸
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g)在下列四种不同情况下化学反应速率最快的是( )
2C(g)+2D(g)在下列四种不同情况下化学反应速率最快的是( )
A.v(D)=0.45 mol/(Lmin)B.v(B)=0.01 mol/(Ls)
C.v(C)=0.40 mol/(Lmin)D.v(A)=0.15 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图与表述一致的是
A.图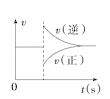 可以表示对某化学平衡体系改变温度后反应速率随时间的变化
可以表示对某化学平衡体系改变温度后反应速率随时间的变化
B.用图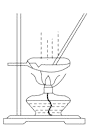 所示装置蒸发AlCl3溶液制备无水AlCl3
所示装置蒸发AlCl3溶液制备无水AlCl3
C.图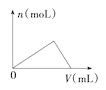 可以表示向一定量的明矾溶液中逐滴滴加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化
可以表示向一定量的明矾溶液中逐滴滴加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化
D.图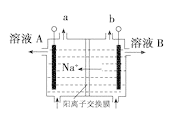 电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B
电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数,下列说法不正确的是 ( )
A.标准状况下的22.4 L辛烷完全燃烧,生成二氧化碳分子数为8NA
B.18 g水中含有的电子数为10 NA
C.46 g二氧化氮和46 g四氧化二氮含有的原子总数均为3 NA
D.在1 L 2 mol/L的硝酸镁溶液中含有的硝酸根离子数为4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应是工业生产硝酸的一个反应过程,4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-1025 kJ/mol,若反应物起始的物质的量相同。下列关于该反应的示意图不正确的是
4NO(g)+6H2O(g) ΔH=-1025 kJ/mol,若反应物起始的物质的量相同。下列关于该反应的示意图不正确的是
A.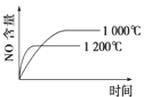 B.
B.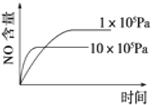
C.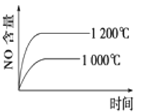 D.
D.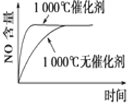
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入![]() 和
和![]() ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液
,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液![]() 滴有几滴酚酞
滴有几滴酚酞![]() 电解实验如图所示。下列说法不正确的是
电解实验如图所示。下列说法不正确的是![]()
![]()
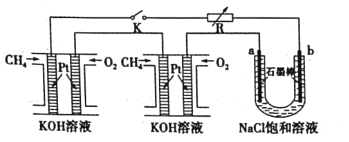
A.甲烷燃料电池正极反应:![]()
B.电解过程中a极附近会出现红色
C.将a、b两极的产物相互反应可得到“84”消毒液的有效成分
D.标况下每个电池甲烷通入量为1L,反应完全,理论上最多能产生氯气8L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计如下实验方案,将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
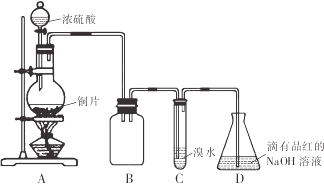
请回答下列问题:
(1)装置B的作用是______。
(2)设计装置C的目的是验证SO2的______性,装置C中发生反应的离子方程式是______装置D中NaOH全部转化为NaHSO3的标志是______。
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
序号 | 实验操作 | 现象 | 结论 |
① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
② | 滴加少量淀粉KI溶液,振荡 | _______ | Ⅲ |
③ | 滴加少量溴水,振荡 | _________ | Ⅱ |
④ | 滴加少量酸性KMnO4溶液、振荡 | 溶液为紫色 | ____ |
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图。
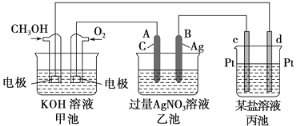
请回答:
(1)甲池是________池,通入O2的一极电极反应式为__________________,该电池的总反应方程式为______________。
(2)乙池中A电极名称为________极,电极反应式为__________________。一段时间后溶液的pH________(填“增大”、“减小”或“不变”)。
(3)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2________mL(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HA溶液,溶液的pH与所加NaOH溶液体积(V)的关系如图所示。下列说法不正确的是
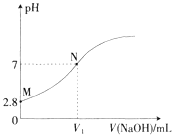
A. V1<20
B. Ka(HA)的数量级为10-5
C. M点溶液加少量水稀释,![]() 增大
增大
D. N点后,随着NaOH溶液的加入,溶液中水的电离程度逐渐增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com