
下列叙述正确的是
A.将5.85 g NaCl晶体溶入100 mL水中,制得0.1 mol/L NaCl溶液
B.将1体积c mol/L硫酸溶液用水稀释为5体积,得到0.2c mol/L硫酸溶液
C.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol/L
D.将w g a% NaCl溶液蒸发掉w/2 g水,得到4a%NaCl溶液
科目:高中化学 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:选择题
在恒容条件下,能使NO2(g)+CO(g) CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增加的措施是( )
CO2(g)+NO(g)正反应速率增大且活化分子的百分数也增加的措施是( )
A.增大NO2或CO的浓度 B.减小CO2或NO的浓度
C.通入Ne使气体的压强增大 D.升高反应的温度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:选择题
为了探索外界条件对反应aX(g)+bY(g)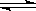 cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如右图所示.以下判断正确的是(
cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如右图所示.以下判断正确的是(  )
)

A.△H>0,a+b>c B.△H>0,a+b<c
C.△H<0,a+b>c D.△H<0,a+b<c
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
二氯化二硫(S2C12)是广泛用于橡胶工业的硫化剂,其分子结构如右图所示。常温下,S2C12是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是
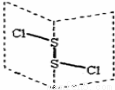
A.S2C12的结构式为Cl—S—S—Cl
B.反应中SO2是还原产物,S是氧化产物
C.S2C12为含有极性键和非极性键的分子
D.反应中,生成1molSO2,转移电子为3mol
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
在20℃、1个大气压下,将三个分别盛满氨气、氯化氢、二氧化氮的等容积烧瓶分别倒置于盛有水的水槽中,当水进入烧瓶中,并使气体充分溶解后(假设试管中的溶液不向外扩散),三种溶液的物质的量浓度之比为
A.1∶1∶1 B.3∶3∶2 C.1∶2∶3 D.1∶1∶2
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:填空题
硫酸是基础化工的重要产品,硫酸的消费量可作为衡量一个国家工业发展水平的标志。生产硫酸的主要反应为: SO2(g)+ 1/2O2(g) SO3(g)
SO3(g)
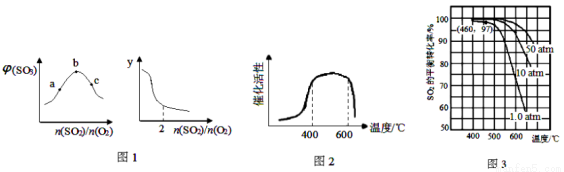
(1)恒温恒容下,平衡体系中SO3的体积分数[φ(SO3)]和y与SO2、O2的物质的量之比[n(SO2)/n(O2)]的关系如图1:则b点n(SO2)/n(O2)=_________;y为_________(填编号)。
A.平衡常数 B.SO3的平衡产率 C.O2的平衡转化率 D.SO2的平衡转化率
(2 Kp是以各气体平衡分压代替浓度平衡常数Kc中各气体的浓度的平衡常数。在400-650℃时,Kp与温度(TK)的关系为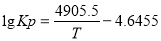 ,则在此条件下SO2转化为SO3反应的△H_________(填“>0”或“<0”)。
,则在此条件下SO2转化为SO3反应的△H_________(填“>0”或“<0”)。
(3)①该反应的催化剂为V2O5,其催化反应过程为:
SO2+ V2O5 SO3+V2O4 K1
SO3+V2O4 K1
1/2 O2+V2O4  V2O5 K2
V2O5 K2
则在相同温度下2SO2(g)+ O2 (g)  2SO3 (g)的平衡常数K=________(以含K1、K2的代数式表示)。
2SO3 (g)的平衡常数K=________(以含K1、K2的代数式表示)。
②V2O5加快反应速率的原因是___________,其催化活性与温度的关系如右图2:
(4)在7.0% SO2、11% O2、82% N2(数值均为气体体积分数)时,SO2平衡转化率与温度、压强的关系如图3,则列式计算460℃、1.0 atm下,SO2 (g)+l/2 O2 (g)  SO3 (g)的Kp=_________(己知:各气体的分压=总压×各气体的体积分数)。
SO3 (g)的Kp=_________(己知:各气体的分压=总压×各气体的体积分数)。
(5)综合第(3)、(4)题图给信息,工业生产最适宜的温度范围为____________,压强通常采用常压的原因是_________。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素,其中X与W处于同一主族,Z元素的原子半径在短周期中最大(稀有气体除外),W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21。下列说法正确的是
A. Y的简单离子半径小于Z的简单离子半径
B. Z的最高价氧化物对应水化物分别与X、Y的最高价氧化物对应水化物反应生成1 mol水时所放出的热量相同
C. Y的简单气态氢化物在一定祭件下可被Q单质氧化
D. Q可分别与X、Y、Z、W形成化学键类型相同的化合物
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期9月月考化学试卷(解析版) 题型:填空题
以橄榄石(主要成分是Mg9FeSi5O20)等为原料生产硅胶、碱式碳酸镁[Mg2(OH)2CO3]的部分工艺流程如下图所示:

(1)Mg9FeSi5O20中铁元素的化合价为 ,为提高镁的浸出率,可采用的两种主要措施是 渣料II的成分是 。
(2)若试剂b是氯碱工业中的某种气体产物,写出加入b后反应的离子方程式 。试剂c的用途是调节溶液的pH,比较恰当的物质是 (写化学式,后同),余液中溶质的主要成分是 。
(3)操作I的名称是 ,写出生成碱式碳酸镁(同时有气体生成)的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:选择题
利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,错误的是( )

A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为:Cu2++2e-===Cu
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处时溶液中各离子浓度都不会发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com