
��ͭ���ǹ�ҵ��ͭ����Ҫԭ�ϣ�����Ҫ�ɷ�ΪCuFeS2������һ����Ȼ��ͭ��SiO2����Ϊ�˲ⶨ�û�ͭ��Ĵ��ȣ�ijͬѧ���������ʵ�飺
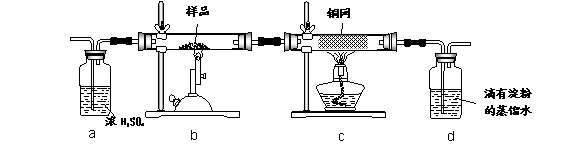 |
�ֳ�ȡ��ϸ�Ļ�ͭ����Ʒ1.840g���ڿ��������½������գ�����Cu��Fe3O4��SO2���壬ʵ���ȡd����Һ��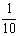 ������ƿ�У���0.05mol/L������Һ���еζ������ı���Һ20.00ml����ش��������⣺
������ƿ�У���0.05mol/L������Һ���еζ������ı���Һ20.00ml����ش��������⣺
��1��������Ʒ���õ�����Ϊ_____(�������ƽ��������ƽ��)������Ʒ��ϸ���ٷ�Ӧ����Ŀ����_______ ��
��2��װ��a��c�����÷ֱ���____��____�����ţ���
a����ȥSO2���� b����ȥ�����е�ˮ���� c��������������
d�������ڹ۲�������� e.��ȥ��Ӧ����������
��3��������Ӧ����������ͨһ��ʱ��Ŀ�������Ŀ����___________��
��4��ͨ�������֪���û�ͭ��Ĵ���Ϊ________��
��5��������ͼװ���������ʵ��װ��d��ͬ�����Դﵽʵ��Ŀ�ĵ���____������ţ���
 |
��6������ԭװ��d�е���Һ��ΪBa(OH)2����õĻ�ͭ�����Ϊ��1%������ʵ���������ȷ�����ܵ�ԭ����Ҫ��_____________________________________________��
��֪ʶ�㡿��ѧʵ��ԭ�����������ζ�������ʵ���еļ���
���𰸽�������1��������ƽ(2��)��ʹԭ�ϳ�ַ�Ӧ���ӿ췴Ӧ���ʣ�2�֣���
��2��b��d��e ����1�֣���3�֣�
��3��ʹ��Ӧ���ɵ�SO2ȫ������dװ���У�ʹ�����ȷ��2�֣���
��4��50%��2�֣��� ��5���ڣ�2�֣���
��6�������е�CO2��Ba(OH)2��Ӧ����BaCO3������BaSO3��������BaSO4����������2�֣�
������
��1����ȡ��Ʒ1.840g��������ƽ�ľ�ȷ��Ϊ0.1g����Ҫѡ�õ�����ƽ������Ʒ��ϸ���ٷ�Ӧ��������Ӵ������ʹԭ�ϳ�ַ�Ӧ���ӿ췴Ӧ���ʡ�
��2����Ʒ������ʱ���ɶ��������������ˮ���еζ�������װ��aҪ�������е�ˮ������ȥ�����Ӱ������������d�IJ�����ͬʱ��ͨ���۲�����ܿ����ݵĶ����жϿ������٣���ֹ��������������������������ɽ��ƫ�ͣ���Ӧ����������������������������ͨ��cװ�ó�ȥ��
��3��������Ӧ����������ͨһ��ʱ��Ŀ�����ʹ��Ӧ���ɵ�SO2ȫ������dװ���У�ʹ�����ȷ��
��4���ñ���Һ���еζ�ʱ��I2+H2SO3+H2O=4H++I-+SO42-��ͨ����ԭ���غ��У�
CuFeS2����2SO2����ȡ��Һ��1/10���еζ�����2 H2SO3����2 I2
0.005mol 0.001mol��10=0.01mol 0.001mol 0.05mol/L��0.02L=0.001mol
�û�ͭ��Ĵ���Ϊ:0.005mol��184g/mol��1.84g��100%=50%
��5����װ�ö����������գ��������ǿ�ᣩ����װ�������ն���������൱����ǿ�����Ե�������ڽ����������������������Ӷ��������ᱵ���������ˡ��������������ٸ�����ԭ���غ�Ҳ���Լ�����Ʒ���ȣ���װ���ű�������������Һ�ķ���ֻ�ܲ�����������������¶ȡ�ѹǿ���ÿ��ƣ����������ʵ�����
��6������ԭװ��d�е���Һ��ΪBa(OH)2�����γ������ᱵ������ͨ��������������������ԭ���غ�ȥ������Ʒ���ȣ�����������У������еĶ�����̼Ҳ���ܱ���������̼�ᱵ���������߿����е������������ᱵ���������ᱵ��������ɽ��ƫ�
��˼·�㲦��������Ҫ���������ѧʵ��ԭ����ע�����ÿһ�����������ã������ɴ��Ʋ��װ�õ����ã������ʵ�鲽���ͬС�죬���ͨ�������֤�𰸵���ȷ�ԣ��ۺ��Խ�ǿ������ѧ����ʵ�����������ϸ�ķ������⡢��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�����ԴΣ�����������в���һ���������Ҵ��������Ҵ����͡������Դ���һ�������͡��Ҵ�����������ȫȼ�յ��Ȼ�ѧ����ʽΪ��
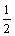 C2H5OH(l)��
C2H5OH(l)��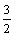 O2(g)��CO2(g)��
O2(g)��CO2(g)��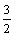 H2O(l) ��H1����683.4 kJ/mol
H2O(l) ��H1����683.4 kJ/mol
����˵����ȷ����
A���÷�Ӧ�����У����ѻ�ѧ����ų�����
B���÷�Ӧ�У�����������������ڷ�Ӧ���������
C���Ҵ���ȼ����Ϊ683.4 kJ/mol
D����Ӧ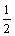 C2H5OH(l)��
C2H5OH(l)��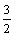 O2(g)��CO2(g)��
O2(g)��CO2(g)��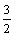 H2O(g)�ġ�H2����683.4 kJ/mol
H2O(g)�ġ�H2����683.4 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ����( )
A. ��CO��ԭCuO��ʵ��ʱ��β���õ�ȼ�ķ�����ȥ
B. FeCl2��Na2O2��Fe(OH)3����ͨ�����Ϸ�Ӧ����
C. �����ơ�����𣬿�����ĭ��������
D. ��ˮ��ʯ��������Ϊ�ܽ���CO2����ˮ��CaCO3��������Ca(HCO3)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ɼ������ӻ�������ɵĻ����������������е������֣�K+��NH4+��Mg2+��Ba2+��Cl����SO42����CO32�������û��������ˮ��ó�����Һ����ȡ3��l00mL����Һ�ֱ��������ʵ�飺
| ������� | �������� | ������ |
| 1 | ��AgNO3��Һ | �а�ɫ�������� |
| 2 | ������NaOH��Һ������ | �ռ������� 1.12L��������ɱ�״���µ������[][] |
| 3 | ������BaCl2��Һʱ�������ó�������ϴ�ӡ������������������м�����ϡ���ᣬȻ�������� | ��һ�γ�������Ϊ 6.27g,�ڶ��γ�������Ϊ 2.33g |
�Իش��������⣺
(1)����ʵ��1��Cl���Ƿ���ڵ��ж����� (�һ�����ڡ�����һ�������ڡ�����ȷ����)������ʵ��l��3�жϻ������һ�������ڵ������������� ������
(2)��ȷ����Һ��һ�����ڵ������Ӽ������ʵ���Ũ��(�ɲ�����)��
| �����ӷ��� | ���ʵ���Ũ�ȣ�mo1��L���� |
(3)��ȷ��K+�Ƿ����?���� ���жϵ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ס��ҡ���������Ϊ��ѧ��ѧ���������ʣ�����֮���ת����ϵ����ͼ(��Ӧ������������������ȥ)��
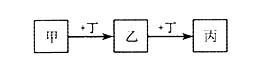
����˵������ȷ����
A��������AlCl3��Һ��������NaOH��Һ
B��������Fe��������Cl2
C��������CO2�������ΪMg
D��������O2�����ҡ�������Է��������������16
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳɰ��������������ˮú����Ӧ�Ƶã����е�һ����ӦΪ��CO��g��+H2O��g��⇌CO2��g��+H2��g������H=��43kJ•mol��1����������Ӧ�����д�ʩ�������COת���ʵ��ǣ�������
| �� | A�� | ����ѹǿ | B�� | �����¶� |
| �� | C�� | ����ˮ������Ũ�� | D�� | ����CO��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��Ӧ��2NO2 ��g��⇌N2O4��g������NO2��N2O4�Ļ������ʢװ��������ͨ����ƿ�Ȼ����ֹˮ�м�ס��Ƥ�ܣ�����ƿA������ˮ�����ƿB�����ˮ���ͼ��ʾ���볣��ʱ��ƿ���������ɫ���жԱȷ��֣�A��ƿ��������ɫ���B��ƿ��������ɫ��dz������˵��������ǣ�������
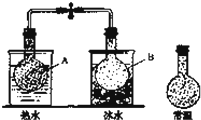
| �� | A�� | ���������У�A��ƿ�������淴Ӧ���ʾ��ӿ� |
| �� | B�� | ���������У�B��ƿ��c��NO2����С��c��N2O4������ |
| �� | C�� | ���������У�A��B��ƿ�������ܶȾ����ֲ��� |
| �� | D�� | ��Ӧ2NO2��g��⇌N2O4��g�����淴ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���û�ѧ��Ӧԭ���о��������ȵȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮
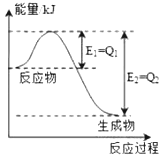
��1�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ͼ��һ�����¶Ⱥ�ѹǿ��N2��H2��Ӧ����lmolNH3�����������仯ʾ��ͼ����д����ҵ�ϳɰ����Ȼ�ѧ����ʽ����N2��g��+3H2��g��⇌2NH3��g����H=��2��Q2��Q1��kJ•mol��1������H����ֵ�ú���ĸQ1��Q2�Ĵ���ʽ��ʾ����
��2�����������У�SO2����������SO3��2SO2��g��+O2��g��⇌2SO3��g���������ϵ��SO3������������¶ȵĹ�ϵ��ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣬

��2SO3⇌2SO2+O2�ġ�H������0��
�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1������K2��
�۷�Ӧ���е�״̬Dʱ��v��������v�棨�������=����
��3��Cl2�ϳ��л���ʱ�����������HC1.4HCl��g��+O2��g��⇌2Cl2��g��+2H2O��g����ʵ���ȵ�ѭ�����ã�
�ٸ÷�Ӧƽ�ⳣ���ı���ʽK=��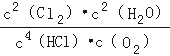 ��������Ӧ�������ݻ�Ϊ2L��4min��ﵽƽ�⣬���������������2.5mol������2.25mol����HCl��ƽ����Ӧ����Ϊ��0.125��mol/L∙min��
��������Ӧ�������ݻ�Ϊ2L��4min��ﵽƽ�⣬���������������2.5mol������2.25mol����HCl��ƽ����Ӧ����Ϊ��0.125��mol/L∙min��
�����÷�Ӧ�����������ܱ������з���������Ӧ��ƽ��ʱ������������ȷ���ǡ�b����
a��4v����HCl��=v�棨O2��
b���ּ���1mol O2������ƽ��ʱ��HCl��ת��������
c�������H2O������ƽ��ʱ��v����HCl������
��ͼ2�Ǹ÷�Ӧ����Ͷ�ϱ�[n ��HCl����n ��O2���ֱ�Ϊ4��1��2��1�£���Ӧ�¶ȶ�HClƽ��ת����Ӱ������ߣ�����������ȷ���ǡ�c����
a�������������䣬�����¶ȣ�ƽ�ⳣ��Kֵ����
b����ƽ�ⳣ��Kֵ�����ƽ��ǰv��ʼ�ռ�С
c����ƽ�ⳣ��Kֵ�����ƽ��������Ӧ�����ƶ�
��Ͷ�ϱ�Ϊ4��1���¶�Ϊ400��ʱ��ƽ��������
Cl2�����ʵ��������ǡ�35.3��%��������������һλС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
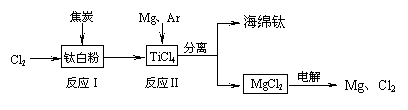 21�������ѵ����͡������������Ѱۣ�TiO2�����������ѣ�Ti����һ�ֹ������̣�
21�������ѵ����͡������������Ѱۣ�TiO2�����������ѣ�Ti����һ�ֹ������̣�
��֪��
�� Mg(s)��Cl2 (g)��MgCl2 (s) ��H����641 kJ��mol��1
 �� Cl2(g)��1/2Ti (s)��1/2TiCl4 (l) ��H����385 kJ��mol��1
�� Cl2(g)��1/2Ti (s)��1/2TiCl4 (l) ��H����385 kJ��mol��1
��1���Ѱ�������TiO2������ˮ���������ᣨH2TiO3��
�����������ճ����Ƶõġ�TiO2������ˮ�������
����ʽΪ ��
��2����Ӧ����800��900���½��У�������һ�ֿ�ȼ
����ɫ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ ��
��Ӧ����Ȼ�ѧ����ʽΪ ��
��3���ù��������У�����ѭ��ʹ�õ������� ��
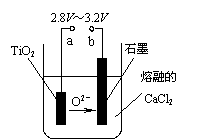
��4����800�桫1000��ʱ���TiO2Ҳ���Ƶú����ѣ�װ������ͼ��ʾ��ͼ��b�ǵ�Դ�� ���������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com