
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要意义.
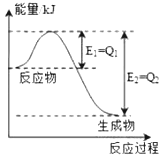
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式: N2(g)+3H2(g)⇌2NH3(g)△H=﹣2(Q2﹣Q1)kJ•mol﹣1 (△H的数值用含字母Q1、Q2的代数式表示).
(2)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)⇌2SO3(g),混合体系中SO3的体积分数和温度的关系如图1所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题,

①2SO3⇌2SO2+O2的△H < 0.
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1 > K2;
③反应进行到状态D时,v正 > v逆(填<、>或=).
(3)Cl2合成有机物时会产生副产物HC1.4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)可实现氯的循环利用.
①该反应平衡常数的表达式K= 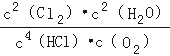 ;若反应容器的容积为2L,4min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 0.125 mol/L∙min.
;若反应容器的容积为2L,4min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 0.125 mol/L∙min.
②若该反应在体积不变的密闭容器中发生,当反应达平衡时,下列叙述正确的是 b .
a.4v正(HCl)=v逆(O2)
b.又加入1mol O2,达新平衡时,HCl的转化率增大
c.分离出H2O,达新平衡时,v正(HCl)增大
③图2是该反应两种投料比[n (HCl):n (O2)分别为4:1和2:1下,反应温度对HCl平衡转化率影响的曲线.下列叙述正确的是 c .
a.其他条件不变,升高温度,平衡常数K值增大
b.若平衡常数K值变大,达新平衡前v逆始终减小
c.若平衡常数K值变大,则平衡向正反应方向移动
④投料比为4:1、温度为400℃时,平衡混合物中
Cl2的物质的量分数是 35.3 %.(计算结果保留一位小数)
| 产物的百分含量随浓度、时间的变化曲线;热化学方程式;化学平衡的影响因素;转化率随温度、压强的变化曲线. . | |
| 专题: | 化学反应中的能量变化;化学平衡专题. |
| 分析: | (1)由图求出N2和H2反应生成1molNH3的反应热,再根据热化学反应方程式的书写要求解答; (2)①由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应进行,据此判断; ②根据温度和化学平衡常数之间的关系来判断; ③D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡; (3)①化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;根据物质的量差量计算参加反应的HCl的物质的量,再根据v= ②a.平衡时不同物质表示的速率之比等于化学计量数之比; b.增大一种反应物的浓度,平衡向正反应移动,其它反应物的转化率增大; c.分离出H2O,生成的浓度降低,达新平衡时,v正(HCl)降低; ③由图可知,投料比一定时,温度越高HCl的转化率越低,故该反应正反应是放热反应,升高温度平衡向逆反应方向移动,平衡常数k降低;平衡常数增大应降低温度,平衡向正反应方向移动,改变体积瞬间反应速率降低,此后正反应速率降低、逆反应速率增大; ④增大一种反应物的浓度,平衡向正反应移动,其它反应物的转化率增大,故投料比n (HCl):n (O2)=2:1到达平衡时HCl的转化率更高,由图象可知,a曲线表示的HCl的转化率更高,故a表示投料比为2:1,b表示投料比为4:1.由图可知,投料比为4:1、温度为40℃时,HCl的转化率为75%,令n (HCl)=4mol、n (O2)=1mol,计算参加反应的HCl,利用三段式计算平衡时各组分的物质的量,据此计算. |
| 解答: | 解:(1)由图可知,N2和H2反应生成1molNH3放出的热量为(b﹣a)kJ,该反应的热化学反应方程式为N2(g)+3H2(g)⇌2NH3(g)△H=﹣2(Q2﹣Q1)kJ•mol﹣1, 故答案为:N2(g)+3H2(g)⇌2NH3(g)△H=﹣2(Q2﹣Q1)kJ•mol﹣1; (2)①由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应方向进行,该反应是放热的,即△H<0,故答案为:<; ②由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应方向进行,K值减小,故平衡常数K1>K2, 故答案为:>; ③D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡,所以V正>V逆, 故答案为:>; (3)①4HCl+O2⇌2Cl2+2H2O的平衡常数k=的表达式K= 4HCl+O2⇌2Cl2+2H2O 物质的量减少△n 4 1 n(HCl) 2.5mol﹣2.25mol=0.25mol 故n(HCl)=0.25mol×4=1mol, 故v(HCl)= 故答案为: ②a.4v正(HCl)=v逆(O2)即v正(HCl):v逆(O2)=1:4,不等于化学计量数之比4:1,反应未到达平衡,向逆反应进行,故a错误; b.加入1mol O2,氧气的浓度,平衡向正反应移动,HCl的转化率增大,故b正确; c.分离出H2O,生成的浓度降低,达新平衡时,v正(HCl)降低,故c错误; 故答案为:b; ③a.升高温度平衡向逆反应方向移动,平衡常数k降低,故a错误; b.平衡常数增大应降低温度,平衡向正反应方向移动,改变体积瞬间反应速率降低,此后正反应速率降低、逆反应速率增大,故b错误; c.平衡常数增大应降低温度,该反应正反应是放热反应,平衡向正反应方向移动,故c正确; 故答案为:c; ④增大一种反应物的浓度,平衡向正反应移动,其它反应物的转化率增大,故投料比n (HCl):n (O2)=2:1到达平衡时HCl的转化率更高,由图象可知,a曲线表示的HCl的转化率更高,故a表示投料比为2:1,b表示投料比为4:1.由图可知,投料比为4:1、温度为40℃时,HCl的转化率为75%,令n (HCl)=4mol、n (O2)=1mol,则参加反应的HCl为4mol×75%=3mol,则: 4HCl+O2⇌2Cl2+2H2O 开始(mol):4 1 0 0 变化(mol):3 0.75 1.5 1.5 平衡(mol):1 0.25 1.5 1.5 故平衡混合物中Cl2的物质的量分数是 故答案为:35.3%. |
| 点评: | 本题考查化学平衡、本题考查化学平衡常数、化学反应速率、化学平衡状态与有关计算、化学平衡图象、热化学方程式及读图能力等,根据图象判断曲线表示的投料比与反应热效应是解题关键.难度中等,(2)中用字母表示反应热数值,符号的确定容易忽略,为易错点. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
离子方程式:RO3n—+F2+2OH-==RO4—+2F—+H2O,由此可知在RO3n—中,元素R的化合价是
A.+4 B.+5 C.+6 D.+7
查看答案和解析>>
科目:高中化学 来源: 题型:
黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:
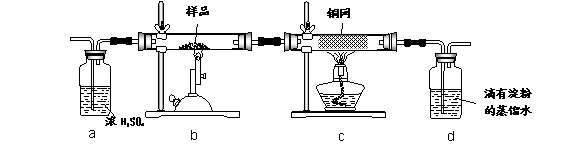 |
现称取研细的黄铜矿样品1.840g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的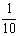 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
(2)装置a和c的作用分别是____和____(填标号)。
a.除去SO2气体 b.除去空气中的水蒸气 c.有利于气体混合
d.有利于观察空气流速 e.除去反应后多余的氧气
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____(填序号)。
 |
(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)⇌2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
|
| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
|
| B. | 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
|
| C. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
|
| D. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中充入A(g)和B(g),它们的初始浓度均为2mol•L﹣1,在一定条件下发生反应:A(g)+B(g)⇌2C(g),该温度下,此反应的平衡常数为4,则A的转化率为( )
|
| A. | 20% | B. | 30% | C. | 40% | D. | 50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化
B.红宝石、水晶、玻璃、陶瓷等都是硅酸盐制品
C.光导纤维、醋酸纤维、铜氨纤维、玻璃纤维等的主要成分都是糖类
D.PM2.5是指大气中直径小于或等于2.5纳米的颗粒物
查看答案和解析>>
科目:高中化学 来源: 题型:
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,同温下测得容器内压强不变,且反应后气体C的密度是原气体密度的4倍。则下列判断正确的是 ( )
A.A、B两种单质的摩尔质量之比为1∶4
B.生成物C中A的质量分数为75%
C.生成物C中A、B的原子个数之比为3∶1
D.反应前后气体分子数之比为1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,能达到实验目的的是( )
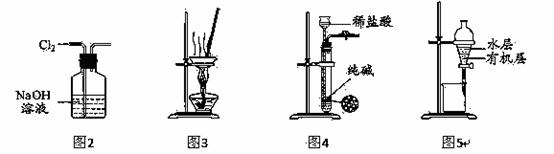
A. 用图2 所示装置除去Cl2中含有的少量HCl
B. 用图3 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 用图4 所示装置制取少量纯净的CO2气体
D. 用图5 所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是分离混合物时常用的主要仪器,从左至右,可以进行的混合物分离操作分别是( )

A、蒸馏、蒸发、萃取、过滤 B、蒸馏、过滤、萃取、蒸发
C、萃取、过滤、蒸馏、蒸发 D、过滤、蒸发、萃取、蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com