
”¾ĢāÄæ”æÄųļÓ£ØNi©Cd£©æɳäµēµē³ŲŌŚĻÖ“śÉś»īÖŠÓŠ¹ć·ŗÓ¦ÓĆ”£µē½āÖŹČÜŅŗĪŖKOHČÜŅŗ£¬µē³Ų·“Ó¦ĪŖ£ŗCd+2NiO(OH£©+2H2O![]() Cd(OH)2+2Ni(OH)2£¬ĻĀĮŠÓŠ¹ŲÄųļÓµē³ŲµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
Cd(OH)2+2Ni(OH)2£¬ĻĀĮŠÓŠ¹ŲÄųļÓµē³ŲµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.³äµē¹ż³ĢŹĒ»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵĹż³Ģ
B.³äµēŹ±Ńō¼«·“Ó¦ĪŖCd(OH)2+2e-=Cd+2OH-
C.·ÅµēŹ±µē³ŲÄŚ²æOH-Ļņøŗ¼«ŅʶÆ
D.³äµēŹ±ÓėÖ±Į÷µēŌ“øŗ¼«ĻąĮ¬µÄµē¼«ÉĻ·¢ÉśNi(OH)2×Ŗ»ÆĪŖNiO(OH)µÄ·“Ó¦
”¾“š°ø”æC
”¾½āĪö”æ
A£®³äµē¹ż³ĢĪŖµē½ā³Ų£¬½«µēÄÜ×Ŗ»Æ³É»ÆѧÄÜ£¬¹ŹA“ķĪó£»
B£®³äµēŹ±Ńō¼«·¢ÉśŹ§µē×ÓµÄŃõ»Æ·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ£ŗNi(OH)2-e-+OH-=NiOOH+H2O£¬¹ŹB“ķĪó£»
C£®·ÅµēŹ±ĪŖŌµē³Ų£¬Ōµē³ŲÖŠŅõĄė×ÓĮ÷Ļņøŗ¼«£¬¹ŹCÕżČ·£»
D£®³äµēŹ±ÓėÖ±Į÷µēŌ“øŗ¼«ĻąĮ¬µÄµē¼«ŹĒŅõ¼«£¬Ņõ¼«·“Ó¦ĪŖCd(OH)2+2e-=Cd+2OH-£¬¹ŹD“ķĪó£»
¹Ź“š°øĪŖC”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖC”ŖC¼üæÉŅŌŠż×Ŗ£¬ĻĀĮŠ¶Ō½į¹¹¼ņŹ½ČēĻĀĶ¼µÄĢžµÄĖµ·ØÕżČ·µÄŹĒ( )

A.øĆĢžŹōÓŚ±½µÄĶ¬ĻµĪļ
B.·Ö×ÓÖŠÖĮÉŁÓŠ9øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
C.·Ö×ÓÖŠÖĮÉŁÓŠ10øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
D.·Ö×ÓÖŠÖĮÉŁÓŠ11øöĢ¼Ō×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞ĆÆĢś[(C2H5)2Fe]µÄ·¢ĻÖŹĒÓŠ»ś½šŹō»ÆŗĻĪļŃŠ¾æÖŠ¾ßÓŠĄļ³Ģ±®ŅāŅåµÄŹĀ¼ž£¬ĖüæŖ±ŁĮĖÓŠ»ś½šŹō»ÆŗĻĪļŃŠ¾æµÄŠĀĮģÓņ”£ŅŃÖŖ¶žĆÆĢśµÄČŪµćŹĒ173”ę(ŌŚ100”ęŅŌÉĻÄÜÉż»Ŗ)£¬·ŠµćŹĒ249”ę£¬²»ČÜÓŚĖ®£¬Ņ×ČÜÓŚ±½”¢ŅŅĆѵČÓŠ»śČܼĮ”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A.¶žĆÆĢśŹōÓŚ·Ö×Ó¾§Ģå
B.ŌŚ¶žĆÆĢśÖŠ£¬C5H5-ÓėFe2+Ö®¼äŠĪ³ÉµÄ»Æѧ¼üĄąŠĶŹĒĄė×Ó¼ü
C.ŅŃÖŖ»·Īģ¶žĻ©µÄ½į¹¹Ź½ĪŖ £¬ŌņĘäÖŠ½öÓŠ1øöĢ¼Ō×Ó²ÉČ”sp3ŌÓ»Æ
£¬ŌņĘäÖŠ½öÓŠ1øöĢ¼Ō×Ó²ÉČ”sp3ŌÓ»Æ
D. C5H5-ÖŠŅ»¶Øŗ¬ÓŠ![]() ¼ü
¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘĻĢŃĢĒ·¢½ĶæÉÖʵĆČéĖį£¬“ÓĖįÅ£ÄĢÖŠŅ²ÄÜĢįČ”³öČéĖį£¬“æ¾»µÄČéĖįĪŖĪŽÉ«š¤³ķŅŗĢ壬Ņ×ČÜÓŚĖ®”£ĪŖĮĖŃŠ¾æČéĖįµÄ·Ö×Ó×é³ÉŗĶ½į¹¹£¬½ųŠŠČēĻĀŹµŃé£ŗ
£Ø1£©³ĘČ”ČéĖį![]() £¬ŌŚÄ³ÖÖדæöĻĀŹ¹ĘäĶźČ«Ęū»Æ£¬ČōĻąĶ¬×“æöĻĀµČĢå»żĒāĘųµÄÖŹĮæĪŖ
£¬ŌŚÄ³ÖÖדæöĻĀŹ¹ĘäĶźČ«Ęū»Æ£¬ČōĻąĶ¬×“æöĻĀµČĢå»żĒāĘųµÄÖŹĮæĪŖ![]() £¬ŌņČéĖįµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ_______”£
£¬ŌņČéĖįµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ_______”£
£Ø2£©Čō½«ÉĻŹöČéĖįÕōĘųŌŚ![]() ÖŠČ¼ÉÕֻɜ³É
ÖŠČ¼ÉÕֻɜ³É![]() ŗĶ
ŗĶ![]() £¬µ±ĘųĢåČ«²æ±»¼īŹÆ»ŅĪüŹÕŗ󣬼īŹÆ»ŅµÄÖŹĮæŌö¼Ó
£¬µ±ĘųĢåČ«²æ±»¼īŹÆ»ŅĪüŹÕŗ󣬼īŹÆ»ŅµÄÖŹĮæŌö¼Ó![]() £»Čō½«“ĖĘųĢåĶعż×ćĮæµÄŹÆ»ŅĖ®£¬²śÉś
£»Čō½«“ĖĘųĢåĶعż×ćĮæµÄŹÆ»ŅĖ®£¬²śÉś![]() °×É«³Įµķ”£ŌņČéĖįµÄ·Ö×ÓŹ½ĪŖ________”£
°×É«³Įµķ”£ŌņČéĖįµÄ·Ö×ÓŹ½ĪŖ________”£
£Ø3£©ČéĖį·Ö×ÓÄÜ·¢Éś×ŌÉķõ„»Æ·“Ó¦£¬ĒŅĘä“ß»ÆŃõ»Æ²śĪļ²»ÄÜ·¢ÉśŅų¾µ·“Ó¦”£ČōĘĻĢŃĢĒ·¢½Ķֻɜ³ÉČéĖį£¬ŹŌŠ“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_______£ØŗöĀŌ·“Ó¦Ģõ¼ž£©”£
£Ø4£©Š“³öČéĖįŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ӧɜ³É·Ö×ÓŹ½ĪŖ![]() µÄ»·×“õ„µÄ½į¹¹¼ņŹ½£ŗ__”£
µÄ»·×“õ„µÄ½į¹¹¼ņŹ½£ŗ__”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĪĖįĆĄĪ÷ĀÉ£ØE£©ŹĒŅ»ÖÖ湊ÄĀÉŹ§³£Ņ©£¬ĘäŅ»ĢõŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
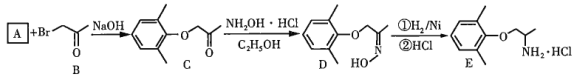
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖAµÄ·Ö×ÓŹ½ĪŖ![]() £¬Ęä»ÆѧĆū³ĘĪŖ______”£
£¬Ęä»ÆѧĆū³ĘĪŖ______”£
£Ø2£©BÖŠµÄ¹ŁÄÜĶŵÄĆū³ĘĪŖ_________”£
£Ø3£©ÓÉAÉś³ÉCµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ________£¬·“Ó¦ĄąŠĶŹĒ_________”£
£Ø4£©ÓÉDµÄ½į¹¹æÉÅŠ¶Ļ£ŗDÓ¦“ęŌŚĮ¢ĢåŅģ¹¹”£øĆĮ¢ĢåŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖ______”£
£Ø5£©ČōÓĆøüĪŖĮ®¼ŪŅ׵ƵݱĖ®Ģę“śŃĪĖįōĒ°±![]() ÓėC·“Ó¦£¬Éś³ÉĪļµÄ½į¹¹¼ņŹ½ĪŖ______”£
ÓėC·“Ó¦£¬Éś³ÉĪļµÄ½į¹¹¼ņŹ½ĪŖ______”£
£Ø6£©AµÄĶ¬·ÖŅģ¹¹ĢåÖŠÄÜÓėČżĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦µÄ»¹ÓŠ__ÖÖ£»ĘäÖŠ£¬ŗĖ“Ź²ÕńĒāĘ×ĪŖĖÄ×é·å£¬·åĆ껿±ČĪŖ6”Ć2”Ć1”Ć1µÄ½į¹¹¼ņŹ½ĪŖ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆµ½µÄ½įĀŪÕżČ·µÄŹĒ£Ø””””£©
Ń”Ļī | ŹµŃé²Ł×÷ŗĶĻÖĻó | ½į””””ĀŪ |
A | ŗ¬ÓŠ·ÓĢŖµÄNa2CO3ČÜŅŗÖŠ¼ÓČėÉŁĮæBaCl2¹ĢĢ壬ČÜŅŗŗģÉ«±äĒ³ | Ö¤Ć÷Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā |
B | ÓĆ²¬ĖæÕŗȔɣĮæNaClČÜŅŗ½ųŠŠŃęÉ«·“Ó¦£¬»šŃę³Ź»ĘÉ« | ÕāŹĒÄĘĄė×ӵķ¢Éä¹āĘ× |
C | NaIČÜŅŗ | ĖįŠŌĢõ¼žĻĀH2O2µÄŃõ»ÆŠŌ±ČI2Ēæ |
D | ĻņÅØ¶Č¾łĪŖ0.1 mol”¤L£1µÄNaClŗĶNaI»ģŗĻČÜŅŗÖŠµĪ¼ÓÉŁĮæAgNO3ČÜŅŗ£¬ĻČ³öĻÖ»ĘÉ«³Įµķ | Ksp£ØAgCl£©<Ksp£ØAgI£© |
A.AB.BC.CD.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ×ĖįĀČąŹĒŅ»ÖÖæ¹Å±¼²Ņ©Īļ£¬ ŃŠ¾æ·¢ĻÖ£¬øĆŅ©ŌŚĻø°ūĖ®Ę½ÉĻÄÜÓŠŠ§ŅÖÖĘŠĀŠĶ¹Ś×“²”¶¾µÄøŠČ¾”£ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
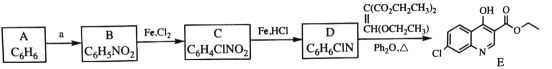

ŅŃÖŖ£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AŹĒŅ»ÖÖ·¼Ļć¾£¬ B ÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ__________________”£
£Ø2£©·“Ó¦ A”śB ÖŠŠė¼ÓČėµÄŹŌ¼Įa ĪŖ___________________”£
£Ø3£©B ·“Ӧɜ³É C µÄ·“Ó¦»Æѧ·“Ó¦·½³ĢŹ½ŹĒ______________________”£
£Ø4£©C”śD ·“Ó¦ĄąŠĶŹĒ_________£¬ DµÄ½į¹¹¼ņŹ½ĪŖ_______________”£
£Ø5£©F”śG·“Ó¦ĄąŠĶĪŖ________________”£
£Ø6£©IŹĒEµÄĶ¬·ÖŅģ¹¹Ģ壬ÓėE ¾ßÓŠĻąĶ¬µÄ»·×“½į¹¹£¬ Š“³öČĪŅāŅ»ÖÖ·ūŗĻĻĀĮŠĢõ¼žµÄIµÄ½į¹¹¼ņŹ½ŹĒ__________________________”£
¢ŁIŹĒȿȔ“śµÄ»·×“ÓŠ»śĪļ£¬ ĀČŌ×ÓŗĶōĒ»łµÄČ”“śĪ»ÖĆÓėEĻąĶ¬£»
¢ŚŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾I ³żĮĖ»·×“½į¹¹ÉĻµÄĒāĶā£¬»¹ÓŠ4×é·å£¬ ·åĆ껿±Č3:1:1:1£»
¢ŪI¼ÓČėNaHCO3ČÜŅŗ²śÉśĘųĢ唣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×”¢ŅŅĮ½øöŹµŃ銔×éĄūÓĆKMnO4ĖįŠŌČÜŅŗÓėH2C2O4ČÜŅŗ·“Ӧъ¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ”£
£Ø1£©øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________”£
Éč¼ĘŹµŃé·½°øČēĻĀ£ØŹµŃéÖŠĖłÓĆKMnO4ČÜŅŗ¾łŅŃ¼ÓČėH2SO4£©£ŗ
£Ø2£©¼××é£ŗĶعż²ā¶Øµ„Ī»Ź±¼äÄŚÉś³ÉCO2ĘųĢåĢå»żµÄ“󊔥“±Č½Ļ»Æѧ·“Ó¦ĖŁĀŹµÄ“óŠ””£ŹµŃé×°ÖĆČēĶ¼£¬ŹµŃ鏱·ÖŅŗĀ©¶·ÖŠAČÜŅŗŅ»“ĪŠŌ·ÅĻĀ£¬A”¢BµÄ³É·Ö¼ūĻĀ±ķ£ŗ

ŠņŗÅ | AČÜŅŗ | BČÜŅŗ |
¢Ł | 2 mL 0.1 mol/L H2C2O4ČÜŅŗ | 4 mL 0.01 mol/L KMnO4ČÜŅŗ |
¢Ś | 2 mL 0.2 mol/L H2C2O4ČÜŅŗ | 4 mL 0.01 mol/L KMnO4ČÜŅŗ |
¢Ū | 2 mL 0.2 mol/L H2C2O4ČÜŅŗ | 4 mL 0.01 mol/L KMnO4ČÜŅŗŗĶÉŁĮæMnSO4 |
øĆŹµŃéĢ½¾æµÄŹĒ______¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ”£ŌŚ·“Ó¦Ķ£Ö¹Ö®Ē°£¬ĻąĶ¬Ź±¼äÄŚÕė¹ÜÖŠĖłµĆCO2µÄĢå»żÓɓ󵽊”µÄĖ³ŠņŹĒ____________(ÓĆŹµŃéŠņŗÅĢīæÕ)”£
£Ø3£©ŅŅ×é£ŗĶعż²ā¶ØKMnO4ČÜŅŗĶŹÉ«ĖłŠčŹ±¼äµÄ¶ąÉŁĄ“±Č½Ļ»Æѧ·“Ó¦ĖŁĀŹµÄ“óŠ””£Č”Į½Ö§ŹŌ¹Üø÷¼ÓČė2 mL 0.1 mol/L H2C2O4ČÜŅŗ£¬ĮķČ”Į½Ö§ŹŌ¹Üø÷¼ÓČė4 mL 0.1 mol/L KMnO4ČÜŅŗ”£½«ĖÄÖ§ŹŌ¹Ü·Ö³ÉĮ½×é£Øø÷ÓŠŅ»Ö§Ź¢ÓŠH2C2O4ČÜŅŗŗĶKMnO4ČÜŅŗµÄŹŌ¹Ü£©£¬Ņ»×é·ÅČėĄäĖ®ÖŠ£¬ĮķŅ»×é·ÅČėČČĖ®ÖŠ£¬¾¹żŅ»¶ĪŹ±¼äŗ󣬷ֱš»ģŗĻ²¢Õńµ“£¬¼ĒĀ¼ČÜŅŗĶŹÉ«ĖłŠčŹ±¼ä”£øĆŹµŃéÄæµÄŹĒŃŠ¾æ_________¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬µ«øĆ×éĶ¬Ń§Ź¼ÖÕĆ»ÓŠæ“µ½ČÜŅŗĶŹÉ«£¬ĘäŌŅņŹĒ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±½·Ö×Ó²»ÄÜŹ¹ĖįŠŌ![]() ČÜŅŗĶĖÉ«µÄŌŅņŹĒ( )
ČÜŅŗĶĖÉ«µÄŌŅņŹĒ( )
A.·Ö×ÓŹĒĘ½Ćę½į¹¹B.·Ö×ÓÖŠÖ»“ęŌŚ![]() ¼ü
¼ü
C.±½²»¾ßÓŠ»¹ŌŠŌD.·Ö×ÓÖŠ“ęŌŚ6µē×Ó“ó![]() ¼ü£¬½į¹¹ĪȶØ
¼ü£¬½į¹¹ĪȶØ
²éæ““š°øŗĶ½āĪö>>
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com