
����Ŀ��ij��ɫ��Һ�к���Mg2+��Al3+��Fe3+��Cu2+��NH4+��Na+�е�һ�ֻ��֣�ȡ100mL����Һ�������в��ϵμ�NaOH��Һ�������ij�������NaOH����仯�Ĺ�ϵ��ͼ��ʾ����������������ȷ����
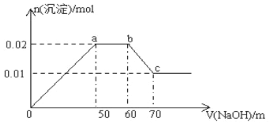
A. ����Һ��һ������Fe3+��Cu2+
B. ����Һ��һ������Mg2+��Al3+��NH4+�����������ʵ���Ũ��֮��Ϊ1��1��1
C. ����NaOH��Һ���ʵ���Ũ��Ϊ0.1mol/L
D. a�㵽b�㣬�����Ļ�ѧ��Ӧ��NH4++ OH��=NH3��H2O
���𰸡�C
��������
��ɫ��Һ��һ������Fe3+��Cu2+��ȡ100mL����Һ�������в��ϵμ�ijŨ�ȵ�NaOH��Һ�����ݲ����ij�������NaOH����仯�Ĺ�ϵ���ɵõ�һ�����У�Mg2+��Al3+��NH4+��oa��Al3++3OH-=Al��OH��3����Mg2++2OH-=Mg��OH��2����ab�Σ�NH4++ OH��=NH3��H2O��bc��Al��OH��3+OH-=AlO2-+2H2O���ݴ˻ش���
��ɫ��Һ��һ������Fe3+��Cu2+��ȡ100mL����Һ�������в��ϵμ�ijŨ�ȵ�NaOH��Һ�����ݲ����ij�������NaOH����仯�Ĺ�ϵ���ɵõ�һ�����У�Mg2+��Al3+��NH4+��oa��Al3++3OH=Al(OH)3����Mg2++2OH=Mg(OH)2����ab�Σ�NH4++ OH��=NH3��H2O��bc�Σ�Al(OH)3+OH=AlO2+2H2O��
A. ��ɫ��Һ��һ������Fe3+��Cu2+����A��ȷ��B. ����Һ��һ������Mg2+��Al3+��NH4+�������������Ƶ�����ֱ���20mL��30mL��10mL�����ݷ�Ӧ���Ĺ�ϵ���������ʵ���Ũ��֮��Ϊ1:1:1����B��ȷ��C. ����ͼ���������������ʵ�����0.01mol����bc�Σ�Al(OH)3+OH=AlO2+2H2O�������������������10mL�����ʵ�����0.01mol�����ԣ�����NaOH��Һ���ʵ���Ũ��Ϊ1mol/L����C������ D. ab�η�����Ӧ��NH4++ OH��=NH3��H2O����B��ȷ������ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ���д��ںܶ�����ѭ�����̡���ͼ����Ȼ���е�ѭ��ʾ��ͼ����ش��������⣺
��1����Ȼ���еĹ̵����˹��̵��Ĺ�ͬ����__________________________________________��
��2������ϸ�����Խ���������������������ƽ�÷�Ӧ: NH3�� O2�� HNO2�� H2O______�����л�ԭ����Ϊ__________________��
��3������ѭ��ͼ�ж�����˵������ȷ����______��
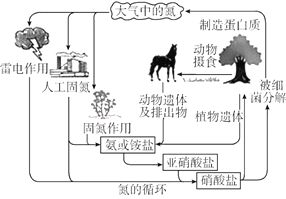
a����Ԫ�ؾ�������
b����������ͺ����л�����ת��
c����ҵ�ϳɰ������˹��̵�
d��ģ������̵����˹��̵���չ�ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯī���缫���KCl��CuSO4���������ϣ������Һ������������ҺpH��ʱ��t�ı仯��ͼ��ʾ������˵����ȷ����
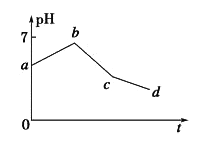
A. ab��H+����ԭ����Һ��pH ����
B. cd ���൱�ڵ��ˮ
C. c��ʱ��������CuCl2���壬���Һ�ɻָ�ԭ��Ũ��
D. ԭ��Һ��KCl��CuSO4�����ʵ���Ũ��֮��Ϊ2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȳ��Ϊ�л��ϳɵ�ԭ��ʱ�����й��̿������ɲ���ΪCH2Br��CHBrCl����( )
A����HCl�ټ�Br2 B����HCl�ټ�HBr
C����Cl2�ټ�HBr D����Cl2�ټ�Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
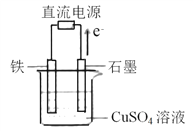
����Ŀ������ͼ��ʾװ���У�ʯī�缫�ĵ缫��ӦʽΪ___________________�������ʼ�����CuSO4����������һ��ʱ�䣬����·��ת��1.0 mol����ʱ��Ҫʹ��Һ�ָ���ԭŨ�ȣ��������м����������____________(�ѧʽ)��������Ϊ________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ƶ������У���ȷ���ǣ� ��
A.�Ʒ��ڿ������ױ���������Ϊ�������ƣ����Ӧ������ˮ����
B.����ǿ��ԭ�������ܴ���Һ���û����������˳������ƺ���Ľ���
C.ֱ�ӹ۲죬�Ƶ���ɫ��Ӧ�ʻ�ɫ
D.�������Ż�ʱ������ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������̷�(FeSO4��7H2O)�Ʊ���Ѫ���ʰ�������[(NH2CH2COO)2Fe] �й������������£�
�ʰ���(NH2CH2COOH) | ������ | �ʰ������� |
������ˮ�������Ҵ������Ի����� | ������ˮ���Ҵ�����ǿ���Ժͻ�ԭ�� | ������ˮ���������Ҵ� |
ʵ����̣�
��.���ƺ�0.10mol FeSO4���̷���Һ��
��.�Ʊ�FeCO3�������ƺõ��̷���Һ�У���������200mL 1.1mol��L-1NH4HCO3��Һ���ӱ߽��裬��Ӧ��������˲�ϴ�ӳ�����
��.�Ʊ�(NH2CH2COO)2Fe��ʵ��װ������ͼ���гֺͼ���������ʡ�ԣ�����ʵ���õ��ij����ͺ�0.20 mol�ʰ����ˮ��Һ��Ϻ����C�У�Ȼ������A�еķ�Ӧ��C�п����ž������ŵ�����������Һ�����ȡ���Ӧ��������ˣ���Һ�������ᾧ�����ˡ�ϴ�ӡ�����õ���Ʒ��
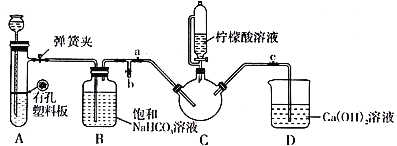
�ش��������⣺
��1��ʵ��I�У�ʵ���������̷���Һʱ��Ϊ��ֹFeSO4���������ʣ�Ӧ������Լ�Ϊ_______��д��ѧʽ�����ٵμ�����ϡ�����������__________________________��
��2��ʵ��II�У����ɳ��������ӷ���ʽΪ__________________________��
��3��ʵ����У���C��ʢ��������Һ����������Ϊ___________________��
��װ��A����ʢ�ŵ�ҩƷ��___________________��������ţ�
A.Na2CO3��ϡH2SO4 B.CaCO3��ϡH2SO4 C.CaCO3��ϡ����
��ȷ��C�п����ž���ʵ��������____________________��
�ܼ�����������Һһ����ɵ�����Һ��pH�ٽ�FeCO3�ܽ⣬��һ��������________________��
��ϴ��ʵ����еõ��ij�������ѡ�õ����ϴ���Լ���___________________��������ţ�
A.��ˮ B.�Ҵ���Һ C.��������Һ
������Ʒ������Ϊ17.34g,�����Ϊ________%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ������һ�����ʣ����ڸ���Һ�м���![]() ��Һ���ְ�ɫ�������ټ�ϡ����������ܽ⣬�����Һ�в����ܺ��е�������
��Һ���ְ�ɫ�������ټ�ϡ����������ܽ⣬�����Һ�в����ܺ��е�������
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ͬ���칹�������л����������Ƿdz��ձ�ġ����и��黯���
��CH3CH2CH2CH3��(CH3)2CHCH3�� ��CH3CH2OH��CH3CH2CH2OH��
��CH3COOCH2CH3��CH3CH2CH2COOH�� ��CH3CH=CHCH3��CH3CH2CH=CH2��
��![]() ��
��![]() �����л�Ϊͬ���칹�����______________________������ţ���
�����л�Ϊͬ���칹�����______________________������ţ���
��2������5���л����������������CH3COOCH2CH3�������ӣ�![]() ������ȩ��CH3CHO�������ᣨCH3COOH�����Ҵ���CH3CH2OH����
������ȩ��CH3CHO�������ᣨCH3COOH�����Ҵ���CH3CH2OH����
����������Na2CO3��Һ��Ӧ�������ݵ���______________________��
����������FeCl3��Һ������ɫ��Ӧ����________________________��
�������ܷ���������Ӧ����________________________��
��д������������������ˮ�ⷴӦ�Ļ�ѧ����ʽ____________________________��
��3���ٵ�������ά����������Ҫ���ʣ�������_____________________ͨ�����۷�Ӧ���ɵ�һ��߷��ӻ����������������к��еĹ�������____________________��____________________��������__________________�ԡ�
��2008�꣬��¹Ӥ���̷�������Ϊ���������谷�����³���ʳ�ø��̷۵IJ���Ӥ����������ʯ���������谷�Ľṹ��ʽ����ͼ��ʾ��
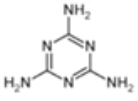
����Ԥ�������谷�ں˴Ź�������ͼ��1H�˴Ź�����ͼ���л����____________________���壻������ ���е�Ԫ�ص���������Ϊ______________________������ðٷ�����ʾ��������һλС���������������谷��ʹʳƷ�е����ʵĺ�����ߡ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com