
【题目】一定温度下,在容积固定的V L密闭容器中加入n mol A.2n mol B,发生反应:A(g)+2B(g) ![]() 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A.B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=________。在保证A浓度不变的情况下,扩大容器的体积,平衡______(填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。

①由图可知,反应在t1.t3.t7时都达到了平衡,而t2.t8时都改变了一种条件,试判断改变的条件:t2时_______________________;t8时_________________________。
②t2时平衡向___________________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线__________。
【答案】BCx 2V/n(1-x) 3C增大生成物C浓度或升高温度使用催化剂逆反应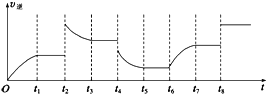
【解析】
(1)平衡状态的判断依据是正逆反应速率相等,各组分的浓度保持不变,据此判断;
(2)依据化学平衡是哪段是列式计算平衡浓度,结合平衡常数概念计算得到平衡常数,保证A浓度不变的情况下,增大容器的体积,BC浓度减小比例相同此时浓度商和平衡常数相同,平衡不动;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,t8时正逆反应速率都增大且平衡不移动;
②t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动;
③t4时降压,平衡向逆反应方向移动,据此分析解答.
(1)平衡状态的判断依据是正逆反应速率相等,各组分的浓度保持不变,
A、反应物A与B加入的反应物的物质的量之比等于其化学计量数之比,所以平衡后A与B的转化率之比等于1:1,故A错误;
B、转化率为x,则平衡后有A、B、C物质的量分别为n-nx、2n-nx、2nxmol,平衡后气体总物质的量为3n-nx,恒容容器中,气体物质的量之比等于其压强之比,故B正确;
C、当2v正(A)=v逆(B)时,说明正逆反应速率相等,反应达到平衡状态,故C正确;
D、恒容容器中,充入惰性气体(如Ar),平衡不移动,故D错误;
故选BC。
(2)在容积固定的V L密闭容器里加入n mol A、2n mol B,发生反应:A(g)+2B(g)![]() 2C(g)△H<0,反应达平衡后测得平衡常数为K,此时A的转化率为x
2C(g)△H<0,反应达平衡后测得平衡常数为K,此时A的转化率为x
A(g)+2B(g)![]() 2C(g)△H<0
2C(g)△H<0
起始量(mol) n 2n 0
变化量(mol) nx 2nx 2nx
平衡量(mol) n-nx 2n-2nx 2nx
平衡浓度为,c(A)=(n-bx)/Vmol·L-1,c(B)=(2n-2nx)/Vmol·L-1,c(C)=2nx/Vmol·L-1,平衡常数K=[C] 2/[A]·[B] 2=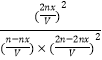 =x 2V/n(1-x) 3,
=x 2V/n(1-x) 3,
在保证A浓度不变的情况下,扩大容器的体积,B、C等比例减小,平衡K=[C] 2/[A]·[B] 2不变,故选C。
(3)由于纵坐标只表示v逆,为了便于求解,在解题时可把v正补上,t2时平衡逆向移动,采用的条件可以是升温或增大C的浓度;t8时平衡不移动,采用的条件是使用了催化剂.
①该反应是一个反应前后气体体积减小的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,改变的条件为增大生成物C浓度或升高温度,t8时平衡不移动,采用的条件是使用了催化剂.
②t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动;
③t4时降压,平衡向逆反应方向移动,所以逆反应速率瞬间减小,并且逐渐减小到达新的平衡,故图象为: 。
。


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】如图所示,电流表指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电解质溶液,

下列说法错误的是
A. B极为原电池的正极
B. A、B、C可能分别为Zn、Cu、稀盐酸
C. C中阳离子向A极移动
D. A极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蛋白质的叙述正确的是( )
A.加热会使蛋白质变性,因此生吃鸡蛋比熟吃好
B.天然蛋白质中仅含C、H、O、N四种元素
C.鸡蛋清加入食盐,会使蛋白质变性
D.一束光线照射蛋白质溶液,产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:

请回答下列问题:
(1)盛装双氧水的化学仪器名称是__________。
(2)如何检验该套装置的气密性__________________________________________________。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而__________。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入______g的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_________________,理由是_________________________________________________。(提示:H2O2的密度可认为近似相等)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18mol/L的浓硫酸配制100mL 1mol/L硫酸
(1)① 应取浓硫酸的体积为______mL,用量筒量取浓硫酸缓缓倒入盛水的烧杯中后,___(填“应该”或“不应”)用少量蒸馏水洗涤量筒2~3次并将洗涤溶液也倒入烧杯中。
②若实验仪器有:A.100mL量筒 B.托盘天平 C. 玻璃棒 D. 50mL容量瓶 E. 10mL量筒 F. 胶头滴管 G. 50mL烧杯 H. 100mL容量瓶
实验时应选用的仪器有(填入编号,下同)_______________________。
③定容时,若俯视液面,则所配溶液浓度_______(填“偏高”、“偏低”或“无影响”)
若不小心加水超过了容量瓶刻度线,应_______。
A.用胶头滴管将多余溶液吸出 B.加热容量瓶使水挥发
C.重新配制
(2)在配制一定物质的量浓度的氢氧化钠溶液过程中,下列操作正确的是_______。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,把称好的固体药品用适量水溶解后立即转入容量瓶中,加蒸馏水定容
D.定容后,把容量瓶反复上下颠倒摇匀,然后贴上标签备用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为: 2H2+O2=2H2O,下列有关说法错误的是

A. 电子通过外电路从a极流向b极
B. b极上的电极反应式为:O2+4H++4e-=2H2O
C. H+由b极通过固体酸电解质传递到a极
D. 每转移0.1 mol电子,标准状况下需消耗1.12 L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是
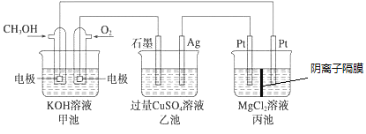
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使溶液恢复原浓度
D. 甲池中消耗4.48L(标准状况下)O2,此时丙池中理论上最多产生23.2 g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) ![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. X的分解速率与Y的消耗速率相等 D. 单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com