
【题目】在下列溶液中,一定能大量共存的一组离子是( )
A. 1.0 mol/L的KOH溶液中:H+、Fe2+、Cl-、SO42-
B. 某无色酸性溶液中:Fe3+、NO3-、Ba2+、H+
C. 加入Al能放出H2的溶液中:Cl-、NO3-、SO42-、NH4+
D. 通入足量CO2的溶液中:H+、NH4+、Al3+、SO42-
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 植物油和裂化汽油都不能使溴水褪色
B. 葡萄糖、油脂和蛋白质都能发生水解反应
C. 聚氯乙烯的单体是氯乙烯
D. 煤的气化是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A.通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B.甲烷是正四面体结构
C.甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3,还是CCl4,都属于取代反应
D.甲烷的四种取代物常温下均为液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是重要的含硫化合物,常用作分析滴定剂。某化学兴趣小组进行了以下有关实验。
实验一: 硫代硫酸钠的制备
硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:
Na2S+Na2CO3+SO2→Na2S2O3+CO2(未配平)
利用如图所示装置可以制取硫代硫酸钠。回答下列问题:

(1) 仪器a的名称为_________。
(2)装置C的作用有________、观察SO2的生成速率。若观察到SO2的生成速率过快,应进行的操作是______________。
(3) 为提高Na2S2O3纯度,应使装置D中Na2S和Na2CO3恰好完全反应,则装置D 中Na2S 和Na2CO3物质的量之比为___________。
(4)制得Na2S2O3后,关闭K2和仪器a的活塞,打开K1。装置A 的作用是_______。
(5)待D 中溶液冷却后,经过蒸发浓缩、冷却结晶可获得硫代硫酸钠晶体,所得晶体中可能含有Na2CO3、Na2S、Na2SO4等杂质。用实验证明产品中存在Na2SO4。完成下列表格:
实验 | 结论 |
取少量产品于试管中,加适量水溶解,加入足量_____,振荡、静置,取上层清液,滴加____溶液,产生白色沉淀。 | 产品中存在Na2SO4 |
实验二: 用硫代硫酸钠溶液测定KI 溶液浓度
①取待测KI 溶液100mL,通入Cl2将I-氧化为IO3-,除去多余Cl2。
②再向溶液中加入足量KI,将IO3-还原为I2。该过程中发生反应的离子方程式为_______。
③用移液管取25.00mL步骤②后的溶液于锥形瓶中,加入几滴______溶液作指示剂,用0.01mol/L的硫代硫酸钠标准溶液滴定(2S2O32-+I2=S4O62-+2I-),至滴定终点共消耗标准液24.00mL,待测KI 溶液的物质的量浓度为______mol/L。若实验中未用硫代硫酸钠标准液润洗滴定管,对测定结果造成的影响是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】增大压强对下列反应的速率无影响的是 ( )
A.CO2(g) + Ca(OH)2 = CaCO3↓ + H2O B.H2 + I2 ![]() 2HI
2HI
C.NaCl +AgNO3 = AgCl↓ + NaNO3 D.N2 +3H2 ![]() 2NH3
2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和周期律分析下面的推断,其中错误的是( )
A. 氢氟酸的酸性强于盐酸 B. 氢氧化钡的碱性强于氢氧化钙
C. 硅酸的酸性强于氢氧化铝 D. 砹化氢不稳定.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列表述中正确的是
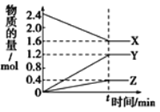
A. 反应的化学方程式为2X=3Y+Z
B. 若t=4,则0~t的X的化学反应速率为0.1mol·L-1·min-1
C. t时,正、逆反应都不再继续进行,反应达到平衡状态
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com