
【题目】现有反应:CO(g)+ H2O(g)![]() CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
(1)达平衡时,CO转化率为多少?
(2)H2的体积分数为多少?
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为多少?
【答案】(1)50﹪;(2)25﹪;(3)75﹪ 。
【解析】试题分析: CO(g)+ H2O(g)![]() CO2(g)+ H2(g)
CO2(g)+ H2(g)
起始浓度(mol/L) 2 2 0 0
转化浓度(mol/L) x x x x
平衡浓度(mol/L) 2-x 2-x x x
根据平衡常数可知(2-x)×(2-x)/x×x=1
解得x=1
(1)达平衡时,CO转化率为![]() ×100%=50%;
×100%=50%;
(2)H2的体积分数为![]() ×100%=25%;
×100%=25%;
(3) CO(g)+ H2O(g)![]() CO2(g)+ H2(g)
CO2(g)+ H2(g)
起始浓度(mol/L) 2 6 0 0
转化浓度(mol/L) y y y y
平衡浓度(mol/L) 2-y 6-y y y
根据平衡常数可知(2-y)×(6-y)/y×y=1
解得x=1.5
所以达平衡时,CO转化率为![]() ×100%=75%
×100%=75%


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F在元素周期表中的相对位置 如图,B与氧元素能形成两种无色气体,D是地壳中含量最多的元素,E是地壳中含量最多的金属元素。
B | ||
F |
(1)BF2的结构式为____________。
(2)D和 F氢化物中沸点较高的___________________填化学式)。
(3)工业制取E单质的化学方程式为______________。
(4)在微电子工业中,C的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________。
(5)火箭使用B2A8C2作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入 太空,并且产生三种无污染的气体,其化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与应用对应关系正确的是
A. 锂比能量(单位质量的电极材料放出电能的大小)大,可用作电池负极
B. 浓硫酸具有脱水性,可用于干燥氯气
C. (NH4)2SO4浓溶液使蛋白质溶液发生盐析,可用于杀菌消毒
D. 铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异戊醇薄荷酯P(![]() )是一种治疗心脏病的药物。一种制备异戊醇薄荷酯P的流程如下:
)是一种治疗心脏病的药物。一种制备异戊醇薄荷酯P的流程如下:
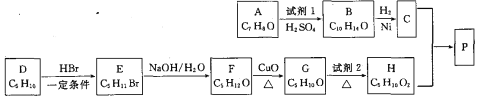
已知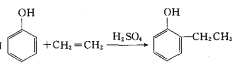 RCH=CH2
RCH=CH2![]() RCH2CHBr(R表示烃基)
RCH2CHBr(R表示烃基)
完成下列问题:
(1)A的化学名称为_____________。
(2)试剂1的结构简式为_____________。
(3)由E生成F的化学方程式为_____________,该反应类型是_____________。
(4)试剂2可以是_____________试剂。(填名称或化学式)
(5)由C和H生成P的化学方程式为_____________。
(6)H的同分异构体中,能发生水解反应的链状化合物共有___________种(不考虑立体异构);其中核磁共振氢谱有两种峰、且蜂值比为9:l的同分异构体的结构简式为_____________。
(7)苯乙烯是一种重要的化工原料。参考制备异戊酸薄荷酯中的方法,设计以苯、乙烯为有机原料(无机试剂自选),制备苯乙烯的合成线路:(合成路线常用的表示方式为:![]() _____________。
_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
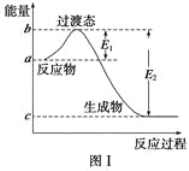
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是 (填“增大”、“减小”或“不变”,下同),ΔH的变化是 。请写出NO2和CO反应的热化学方程式 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)==CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
且H2O(g)==H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为 。
(3)如表所示是部分化学键的键能参数:
化学键 | P—P | P—O | O===O | P===O |
键能/kJ·mol-1 | a | b | c | x |
已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x= kJ·mol-1(用含a、b、c、d的代表数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2.0 L恒容密闭容器中充入1.0 mol PCl5,在温度为T℃时发生如下反应PCl5(g) ![]() PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
时间t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题:
(1)反应在前50 s的平均速率v(PCl5) = 。
(2)温度为T℃时,该反应的化学平衡常数= 。
(3)要提高上述反应的转化率,可采取的措施是 (任写一种)。
(4)在温度为T℃时,若起始时充入0.5 mol PCl5和a mol Cl2,平衡时PCl5的转化率仍为20%,则
a= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势如下图所示:

(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为________极(填“正”或“负”)。铜电极上产生的现象为____________,该极上发生的电极反应为____________________,外电路中电子由____________极(填“正”或“负”,下同)向________极移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com