
【题目】下列离子方程式正确的是( )
A.向氨水通入足量SO2:SO2+2NH3H2O═2NH4++SO32﹣+H2O
B.将Ba(OH)2溶液滴入NaHSO4溶液中至SO42﹣恰好完全沉淀:Ba2++SO42﹣+2OH﹣+2H+═BaSO4↓+2H20
C.向醋酸溶液中滴加过量NaOH溶液:H++OH﹣═H2O
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH﹣ ![]() CH3COO﹣+Cu2O↓+3H2O
CH3COO﹣+Cu2O↓+3H2O
【答案】D
【解析】解:A.向氨水通入足量SO2,反应生成亚硫酸氢铵,正确的离子方程式为:SO2+NH3H2O═NH4++HSO3﹣,故A错误;
B.将Ba(OH)2溶液滴入NaHSO4溶液中至SO42﹣恰好完全沉淀,氢氧根离子有剩余,正确的离子方程式为:Ba2++SO42﹣+OH﹣+H+═BaSO4↓+H2O,故B错误;
C.向醋酸溶液中滴加过量NaOH溶液,反应生成醋酸钠和水,醋酸不能拆开,正确的离子方程式为:CH3COOH++OH﹣═H2O+CH3COO﹣,故C错误;
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热,反应的离子方程式为:CH3CHO+2Cu(OH)2+OH﹣ ![]() CH3COO﹣+Cu2O↓+3H2O,故D正确;
CH3COO﹣+Cu2O↓+3H2O,故D正确;
故选D.
A.二氧化硫过量,反应生成亚硫酸氢铵;
B.硫酸根离子恰好沉淀时,二者物质的量之比为1:1,氢氧根离子过量;
C.醋酸为弱酸,离子方程式中醋酸不能拆开;
D.乙醛与新制氢氧化铜浊液反应生成氧化亚铜沉淀.


科目:高中化学 来源: 题型:
【题目】下列各组离子中,在酸性溶液中能大量共存的无色溶液( )
A.Na+、Cl-、NO3-、SO42-B.K+、Cu2+、NO3-、Cl-
C.Mg2+、Cl-、SO42-、HCO3-D.Ba2+、NO3-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(1)请写出金属钒与浓硝酸反应的离子方程式:__________________________________,
(2)灼烧NH4VO3时可生成钒的氧化物V2O5,请写出该反应的化学方程式:___________。
(3)V2O5是较强的氧化剂。它能与沸腾的浓盐酸作用产生氯气,其中钒元素被还原为蓝色的VO2+,请写出该反应的离子方程式:______________________________________。
(4)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:______、______。
(5)工业上用接触法制硫酸时要用到V2O5。在氧化SO2的过程中,450℃时发生V2O5与VO2之间的转化:V2O5+SO2=2VO2+SO3、4VO2+O2=2V2O5,说明V2O5在接触法制硫酸过程中所起的作用是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式不正确的是( )
A. 向Al2(SO4)3溶液中加入过量氨水:Al3++ 3NH3·H2O = Al(OH)3↓+ 3NH4+
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O
C. 碳酸氢钙溶液中加入足量烧碱溶液:Ca2+ +2HCO3-+2OH-=CaCO3 ↓+CO32- +2H2O
D. 氯气与H2O反应:Cl2+H2O=2H++Cl—+ClO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】上世纪80年代后期人们逐渐认识到,NO在人体内起着多方面的重要生理作用。下列关于NO的说法错误的是( )
A.NO是具有刺激性的红棕色气体
B.NO是汽车尾气的有害成分之一
C.NO在人体的血管系统内具有传送信号的功能
D.NO能够与人体血红蛋白结合,造成人体缺氧中毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种烃①2-甲基丁烷 ②2,2-二甲基丙烷 ③正戊烷 ④丙烷 ⑤丁烷,按沸点由高到低的顺序排列的是
A. ①>②>③>④>⑤ B. ②>③>⑤>④>①
C. ③>①>②>⑤>④ D. ④>⑤>②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是( )
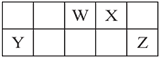
A. 氢化物沸点:W>Z B. 氧化物对应水化物的酸性:Y>W
C. WX2是酸性氧化物 D. 简单离子的半径: Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列们关说法正确的是
A. 石墨具有良好的润滑性,故可用做电池的电极材料。
B. 碳酸钠溶液呈碱性,故可用带玻璃塞的试剂瓶盛放
C. 液氮的沸点较低,故可为超导材料提供低温环境
D. 单晶硅的硬度较高,故可用于制备电子芯片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.短周期元素形成离子后,最外层都达到8电子稳定结构
B.第二周期元素的最高正化合价等于它所处的主族序数
C.同一元素可能既表现金属性,又表现非金属性
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com