
【题目】实验室中Y形管是一种特殊的仪器,通常与其他仪器组合可以进行某些实验探究。利用下图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。回答下列问题:

(1)广口瓶中间那根玻璃管的作用是:__________________________________________。
(2)实验前需要将BaCl2溶液煮沸,其目的是:_________________________________。
(3)甲中发生反应的化学方程式为:____________________________________________。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体。该反应的化学方程式为:____________________________________________。
(5)实验时,先使甲中产生的足量气体通入BaCl2溶液中,始终无沉淀生成。由此得出的结论是_______。
(6)向上述⑸实验所得溶液中通入乙产生的气体,产生白色沉淀,请写出发生反应的离子方程式:_____。
(7) 请指出该实验的一个不足之处:____________________________________________。
【答案】平衡压强,使甲、乙中的气体可顺利进入BaCl2溶液中 排除溶解的O2防止将SO2在溶液中氧化为SO42-而对实验产生干扰 Na2SO3+H2SO4(浓)=SO2↑+Na2SO4+H2O CaO + NH3·H2O=Ca(OH)2+NH3↑(或NH3·H2O![]() NH3↑ +H2O ) 在酸性条件下不能生成BaSO3沉淀 SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+ SO2可能对环境产生污染(或没尾气处理装置)、通NH3时有可能倒吸
NH3↑ +H2O ) 在酸性条件下不能生成BaSO3沉淀 SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+ SO2可能对环境产生污染(或没尾气处理装置)、通NH3时有可能倒吸
【解析】
本题的实验目的是探究SO2与BaCl2反应生成BaSO3沉淀的条件。甲装置中Na2SO3与浓H2SO4反应制备SO2;为了防止BaCl2溶液中溶解的O2与SO2作用产生的SO42-干扰实验的判断,实验前需要将BaCl2溶液煮沸赶尽溶解氧;通过实验现象得出在酸性条件下SO2不能与BaCl2反应生成BaSO3沉淀;装置乙中产生的碱性气体为NH3,由CaO和氨水作用产生NH3;SO2、NH3通入BaCl2溶液中产生BaSO3沉淀;SO2、NH3都能污染大气,NH3极易溶于水,该装置的不足之处是没有尾气吸收装置、通NH3时可能产生倒吸;根据上述分析作答。
(1)广口瓶中间那根玻璃管的作用是:平衡压强,使甲、乙中的气体可顺利进入BaCl2溶液。
(2)为了防止BaCl2溶液中溶解的O2与SO2作用产生的SO42-干扰实验的判断,实验前需要将BaCl2溶液煮沸,其目的是:排除溶解的O2,防止将SO2在溶液中氧化为SO42-而对实验产生干扰。
(3)甲中Na2SO3与浓H2SO4反应生成Na2SO4、H2O和SO2,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体,该碱性气体为NH3,获得NH3的常用氧化物为CaO、无色液体为氨水,两者反应的化学方程式为:CaO+NH3·H2O=Ca(OH)2+NH3↑。
(5)实验时,将甲中产生的足量SO2通入BaCl2溶液中,始终无沉淀生成,由此说明:酸性条件下SO2不能与BaCl2反应生成BaSO3沉淀。
(6)向上述(5)实验所得溶液中通入NH3,产生白色沉淀,反应的化学方程式为SO2+2NH3+H2O+BaCl2=BaSO3↓+2NH4Cl,反应的离子方程式为SO2+2NH3+H2O+Ba2+=BaSO3↓+2NH4+。
(7)SO2、NH3都能污染大气,该装置的不足之处是没有尾气吸收装置;NH3极易溶于水,该装置的不足之处是装置中d导管插入BaCl2溶液中,通NH3时可能产生倒吸。


科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一密闭容器中进行,下列条件的改变能使反应速度变快的是①体积不变,增加Fe的量; ②体积不变,增加H2O的量;③体积不变,充入N2使压强增大;④压强不变,充入N2使体积增大
Fe3O4(s)+4H2(g)在一密闭容器中进行,下列条件的改变能使反应速度变快的是①体积不变,增加Fe的量; ②体积不变,增加H2O的量;③体积不变,充入N2使压强增大;④压强不变,充入N2使体积增大
A. ①②③B. ②④C. ②③D. ②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HCO3﹣+AlO2﹣+H2O═CO32﹣+Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为( )
A. 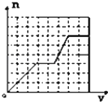 B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,相关示意图错误的是( )
A | B | C | D |
将二氧化硫通入到一定量氯水中 | 将NaHCO3溶液滴入到一定量Ba(OH)2溶液中 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)在量取浓盐酸时宜选用下列量筒中的________。
A.5 mL B.10 mL
C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面最低处与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】党的十九大强调树立“社会主义生态文明观”。下列做法不应该提倡的是( )
A.研发可降解高分子材料,缓解白色污染问题
B.扩大铅蓄电池、含汞干电池的生产,满足消费需求
C.采用碳捕集和封存技术,逐步实现二氧化碳零排放
D.大力发展太阳能、风能等清洁能源,减少对化石燃料的依赖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中正确的是( )
A. 钠原子的结构示意图: 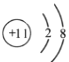
B. 过氧化钠的电子式:![]()
C. 碳酸氢钠的电离方程式:NaHCO3= Na++ H+ + CO32-
D. 中子数为12的钠的核素符号为: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸铝溶液为原料之一,在实验室里制取少量氢氧化铝,并且容易分离,最好向溶液中加入是( )
A.氢氧化钠溶液
B.氢氧化钡溶液
C.稀盐酸
D.氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是__________________________。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。
(二)工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾FeSO4·7H2O的流程如下:
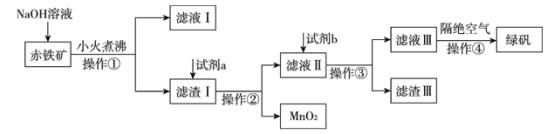
(1)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为____________;_________________。
(2)向滤渣Ⅰ中加入过量的试剂a为___________,过量的试剂b投入到滤液Ⅱ发生的所有反应的离子方程式为______________;_________________;________________。
(3)实验室中操作①②③的名称为_________________________。
(4)操作④隔绝空气的目的是_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com