
【题目】分子式为C8H14O4的有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则符合该条件的有机物有( )(不考虑立体异构)
A.8种B.10种C.13种D.16种
【答案】C
【解析】
该有机物的不饱和度为:![]() ,又知该有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则该有机物含有两个酯基,除酯基以外的烃基应为饱和烃基,水解后得到一分子的二元羧酸,二分子的饱和一元醇,且为同一种醇,则可按照构成酯的二元羧酸和醇的同分异构体确定该酯的同分异构体,据此分析解答。
,又知该有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则该有机物含有两个酯基,除酯基以外的烃基应为饱和烃基,水解后得到一分子的二元羧酸,二分子的饱和一元醇,且为同一种醇,则可按照构成酯的二元羧酸和醇的同分异构体确定该酯的同分异构体,据此分析解答。
该有机物的不饱和度为:![]() ,又知该有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则该有机物含有两个酯基,除酯基以外的烃基应为饱和烃基,水解后得到一分子的二元羧酸,二分子的饱和一元醇,且为同一种醇,则可按照构成酯的二元羧酸和醇的同分异构体确定该酯的同分异构体,
,又知该有机物在酸性条件下水解生成一种酸和一种醇,且酸和醇的物质的量之比为1:2,则该有机物含有两个酯基,除酯基以外的烃基应为饱和烃基,水解后得到一分子的二元羧酸,二分子的饱和一元醇,且为同一种醇,则可按照构成酯的二元羧酸和醇的同分异构体确定该酯的同分异构体,
若酸为乙二酸,那么醇应为丙醇,丙醇有2种,故此酯有2种;
若酸为丁二酸,那么醇应为乙醇,丁二酸相当于乙烷的二元取代物,则丁二酸有2种,故此酯类有2种;
若酸为己二酸,那么醇应为甲醇,己二酸相当于丁烷的二元取代物,则己二酸有9种,故此酯有9种,故总共为2+2+9=13种,故C正确;
故选C。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.漂白粉可以用于生活用水的消毒
B.石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
C.氯气通入水中杀菌消毒,发生了化学变化
D.漂白粉在空气中久置变质,原因是原白粉中的CaCl2与空气中的CO2反应生成CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
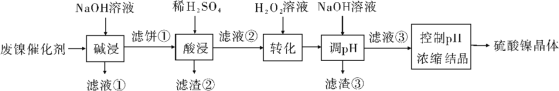
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01 mol·L1)的pH 沉淀完全时(c=1.0×105 mol·L1)的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代H2O2的物质是______________。若工艺流程改为先“调pH”后“转化”,即
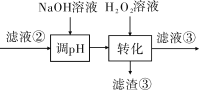
“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=______________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L1,则“调pH”应控制的pH范围是______________。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列物质①过氧化钠、②氧化铝、③硅、④二氧化硅、⑤NaHCO3。请填空:(填序号)
可用来制计算机芯片的是_________。可用于呼吸面具中作为氧气来源的是______。能作光导纤维的是_________。能作耐火材料的是_______。属于电解质的是 _________________。属于盐的是 ______,该盐受热分解的化学方程式为:_____________________________。
(2)除去FeCl2溶液中混有的FeCl3,相应的离子方程式是_______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯乙醛是基本有机合成原料之一,是生产农药、医药的重要中间体。某化学兴趣小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。
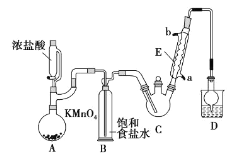
查阅资料,有关信息如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
回答下列问题:
(1)仪器E的名称是____,冷凝水的流向是____口进水(填“a”或“b”)。
(2)有同学认为该装置存在一处缺陷,应在BC之间加一干燥装置,理由是____。
(3)该装置C控制反应温度在70℃左右,可采用____加热的方法;
(4)装置D干燥管的作用为____,装置D烧杯中的试剂是____。
(5)反应结束后,从C中的混合物中分离出Cl3CCOOH的方法是(填名称)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯基环丁烯酮(![]() PCBO)是一种十分活泼的反应物,可利用它的开环反应合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如下:
PCBO)是一种十分活泼的反应物,可利用它的开环反应合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如下:
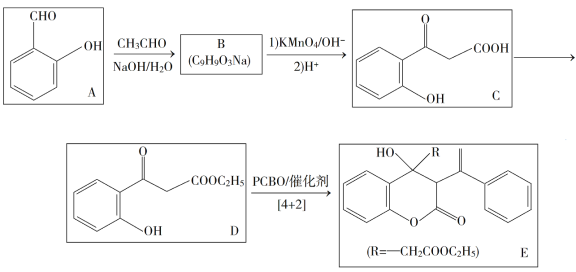
已知如下信息:

回答下列问题:
(1)A的化学名称是___________。
(2)B的结构简式为___________。
(3)由C生成D所用的试别和反应条件为___________;该步反应中,若反应温度过高,C易发生脱羧反应,生成分子式为C8H8O2的副产物,该副产物的结构简式为________。
(4)写出化合物E中含氧官能团的名称__________;E中手性碳(注:连有四个不同的原子或基团的碳)的个数为___________。
(5)M为C的一种同分异构体。已知:1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧化碳;M与酸性高锰酸钾溶液反应生成对苯二甲酸。M的结构简式为__________。
(6)对于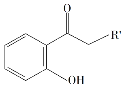 ,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深入研究,R'对产率的影响见下表:
,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深入研究,R'对产率的影响见下表:
R' | —CH3 | —C2H5 | —CH2CH2C6H5 |
产率/% | 91 | 80 | 63 |
请找出规律,并解释原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各实验操作中错误的是![]()
![]() 实验室制乙烯时,温度计水银球应插入混合液中
实验室制乙烯时,温度计水银球应插入混合液中
![]() 配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
![]() 配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
![]() 用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
![]() 做过银镜反应的试管用浓硝酸清洗
做过银镜反应的试管用浓硝酸清洗
![]() 卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
![]() 若苯酚不慎沾到皮肤上,应立即用酒精洗涤
若苯酚不慎沾到皮肤上,应立即用酒精洗涤
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有的油田开采的石油中溶有一种碳氢化合物—金刚烷。金刚烷 是一种环状烃,它的结构高度对称。下图表示金刚烷,图中数字是碳原子编号。碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子。
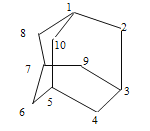
(1)编号1的碳原子上的一个氢原子被氨基(-NH2)取代后,再与盐酸反应生成盐酸盐(1—氨基金刚烷盐酸盐)是一种防治感冒的药物。推断它的化学式是__________。
(2)金刚烷是由 _____ 个六元环构成的笼形结构,其中有 _____ 个碳原子被三个环共有。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com