
| A、氯气通入水中:Cl2+H2O?2H++Cl-+ClO- |
| B、氢氧化铁胶体中加入HI溶液:Fe(OH)3+3H+=Fe3++3H2O |
| C、NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、用稀硝酸除去试管内壁银:3Ag+4H++NO3-=3Ag++NO↑+2H2O |


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
| A、氢气和氧气反应生成水、水电解生成氢气和氧气互为可逆反应 |
| B、既能向正反应方向进行又能向逆反应方向进行的反应叫做可逆反应 |
| C、可逆反应不能完全进行,存在一定的限度 |
| D、对于2SO2+O2?2SO3,增加反应物O2的量,可以使SO2完全转化为SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“碳纳米泡沫”与石墨互为同位素 |
| B、把“碳纳米泡沫”分散到适当的溶剂中,能产生丁达尔现象 |
| C、“碳纳米泡沫”是一种新型的碳化合物 |
| D、“碳纳米泡沫”和金刚石的性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNa2O2固体中含离子总数为4NA | ||||
| B、常温下,5.6gFe与足量稀HNO3反应,转移0.2NA个电子 | ||||
| C、常温常压下,5.6g乙烯与丁烯的混合物中含有的氢原子的数目为0.8NA | ||||
D、5NH4NO3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+1AlO2-+2H2O |
| B、氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2NH4+=Mg2++2NH3?H2O |
| C、磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-=3Fe3++NO↑+4H2O |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
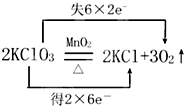 回答下列各题:
回答下列各题:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com