
【题目】普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是

A. 化学式可以表示为KFe2(CN)6
B. 每一个立方体中平均含有24个π键
C. 普鲁士蓝不属于配位化合物
D. 每个Fe3+周围与之相邻的Fe2+离子有12个
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】图表示可逆反应A(s)+B(g) n C(g);ΔH=Q kJ·mol1,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述中一定正确的
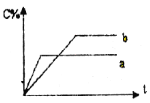
A. 若条件为催化剂,则a表示有催化剂,b表示没有催化剂
B. 只改变温度,则a比b的温度高,且Q>0
C. 只改变压强,则a比b的压强大,n>2
D. 由图象可以作出判断,反应一定从正反应方向开始
查看答案和解析>>
科目:高中化学 来源: 题型:
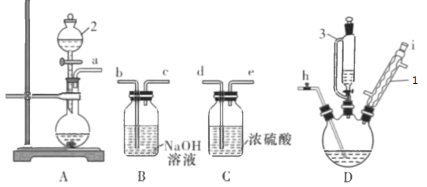
【题目】实验室可用如图装置制得氯气并与铝粉反应制备无水AlCl3。已知AlCl3在183°C升华,遇潮湿空气即反应产生大量白雾。请回答问题:
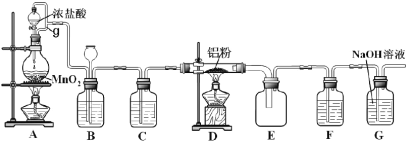
(1)A中反应的化学方程式为_________;HCl在反应中表现出的性质为______(填:酸性、氧化性或还原性)。
(2)A中g管的作用是________。
(3)B中盛放饱和食盐水的作用是________;若D中生成的AlCl3凝华堵塞导管,B中可观察到的现象为________。
(4)C和F所装试剂相同,其中F的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.NaCl(aq) ![]() Na(s)
Na(s) ![]() Na2O2(s)
Na2O2(s)
B.SiO2(s) ![]() Si(s)
Si(s) ![]() SiCl4(l)
SiCl4(l)
C.SO2(g) ![]() NH4HSO3(aq)
NH4HSO3(aq) ![]() (NH4)2SO4(aq)
(NH4)2SO4(aq)
D.Cu2(OH)2CO3(s) ![]() CuO(s)
CuO(s) ![]() Cu(OH)2(s)
Cu(OH)2(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.常温常压下,8gO2含有8NA个质子
B.分子总数为NA的CO2和NO2混合气体中含有的氧原子数为2NA
C.标准状况下,22.4L盐酸含有NA个HC1分子
D.分子总数为NA的CO、N2混合气体体积约为22.4L,质量为28g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)今有五种物质:①铜线 ②熔化的NaCl ③NaCl晶体 ④氨气 ⑤液态氯化氢,其中能导电的物质是__;属于电解质的是___;属于非电解质的是___。
(2)0.5molH2SO4的质量是__g,能中和___molNaOH,该硫酸所含氢元素的质量与___molNH3中所含氢元素的质量相同。
(3)相同质量的CH4和H2S中分子个数比为___。
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为(_____)
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一水硫酸锰(MnSO4H2O)是一种重要的化工中间体,工业上可由高铁菱锰矿(主要成分为MnCO3,含有FeCO3、Al2O3、MgO、CaO、SiO2等杂质)制备,部分工艺流程如下:
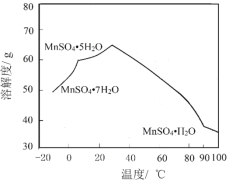
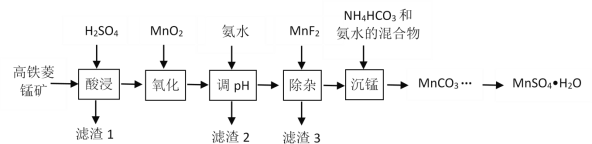
相关金属离子[c(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的 pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“酸浸”时高铁菱锰矿需要粉碎,并进行充分搅拌,为提高锰的浸出率还可采取的措施有_________。(写出其中一种)
(2)“氧化”时发生反应的化学方程式为________。
(3)“调pH”范围至5~6,得到滤渣2的主要成分除MnO2外还有_________。
(4)“除杂”过程中加入MnF2的目的是_________。已知:Ksp(MgF2)=5.16×10-11,Ksp(CaF2)=5.3×10-9。
(5)“沉锰”过程中发生反应的离子方程式为_________。
(6)MnSO4在水中的溶解度与温度关系如图。由MnCO3获得较纯净的MnSO4H2O 晶体的方法是:将MnCO3溶于_________,控制温度为_________以上结晶,得到MnSO4H2O晶体,洗涤、烘干。晶体烘干时温度不能过高的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向50mL 1mol·L-1的盐酸中加入烧碱,水的KW不变
B. NH4Cl和NH3·H2O混合液中,二者对对方的平衡都起了抑制作用
C. 有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+)
D. 常温0.1mol·L-1HA溶液中c(OH-)/ c(H+)=10-8,则0.01mol·L-1 HA溶液中c(H+)=1×10-4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)可用于制备增塑剂,常温下为无色透明液体,密度1.68g/mL,沸点105.8oC,易挥发,易水解。一中化学兴趣小组探究制备POCl3所需的装置如下图所示:
反应原理:![]() (PC13常温下为液态,密度1.57g/mL,沸点75oC,易挥发,易水解)。
(PC13常温下为液态,密度1.57g/mL,沸点75oC,易挥发,易水解)。
(1)仪器3的名称是 ________,仪器2中装入的物质为_______,仪器1的作用是 ___________。
(2)A中发生的反应的离子方程式可能为__________________________________
(3)请组装好上述装置(如有必要可以重复选择),用小写字母连接:_________________。
(4)开始通入氯气,同时慢慢滴加水,控制氯气和水的质量比大于等于3.94,理由是_____________________________________。
(5)准确量取13.75mL PCl3充分反应后经分离提纯得到纯净的POCl3 16.8g,请计算实验的产率为________________________ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com