
【题目】将图Ⅰ所示装置通电10 min后,撤掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左侧铁电极表面析出了白色胶状物质,U形管右侧液面上升。下列说法正确的是( )

A. 同温同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多
B. 装置Ⅱ中铁电极的电极反应式为Fe-2e-+2OH-===Fe(OH)2↓
C. 装置Ⅱ中石墨电极的电极反应式为2H++2e-===H2↑
D. 装置Ⅰ通电10 min后,铁电极附近溶液的pH降低
【答案】B
【解析】
A.装置Ⅰ中石墨电极与电源的正极相连,作阳极,氯离子放电生成Cl2,铁电极是阴极,氢离子放电,生成H2,因Cl2能溶解在水中,且与H2O发生反应:Cl2+H2O=HCl+HClO,而H2不溶于水,故石墨电极上方得到的气体比铁电极上方得到的气体少,A错误;
B.装置Ⅱ是原电池装置,Fe为负极,失去电子产生Fe2+,溶液显碱性,Fe2+再与溶液中的OH-反应生成Fe(OH)2:Fe-2e-+2OH-=Fe(OH)2↓,B正确;
C.装置Ⅱ是原电池装置,石墨为正极,正极为Cl2得到电子:Cl2+2e-=2Cl-,C错误;
D.装置Ⅰ中铁电极是阴极,氢离子放电产生H2:2H2O+2e-=H2↑+2OH-,由于有OH-生成,故溶液的pH升高,D错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】下列化学用语或模型正确的是( )
A. CH4分子的比例模型:![]() B. 乙醇的结构简式:C2H6O
B. 乙醇的结构简式:C2H6O
C. Al3+的结构示意图:![]() D. 氯化钙的电离方程式:CaCl2===Ca2++Cl2-
D. 氯化钙的电离方程式:CaCl2===Ca2++Cl2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知M2On2-可与R2-作用,R2-被氧化为R单质,M2On2-的还原产物中M为+3价;又知c(M2On2-) =0.3mol/L的溶液100mL 可与c(R2-)=0.6mol/L的溶液150mL恰好完全反应,则n值为()
A.4 B.5 C.6 D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.0.01molNH4+含有质子数为0.1NA
B.4.48 L N2与CO的混合物所含分子数为0.2NA
C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2NA
D.10.0mL 12 mol·L-1浓盐酸与足量二氧化锰反应,转移电子数为0.06NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S![]() 6Cu+SO2↑,对于该反应,下列说法正确的是
6Cu+SO2↑,对于该反应,下列说法正确的是
A. 该反应的氧化剂只有Cu2O B. Cu既是氧化产物,又是还原产物
C. Cu2S既是氧化剂又是还原剂 D. 还原产物与氧化产物的物质的量之比为1∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
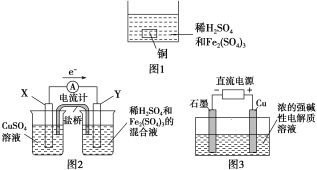
A. 如图1所示将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO![]() )为0.5 mol/L
)为0.5 mol/L
B. 如图2所示的装置中发生Cu+2Fe3+===Cu2++2Fe2+的反应,X极是负极,Y极的材料可以是铜
C. Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应
D. 如图3所示当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为0.65mol / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O,该反应中被氧化的元素是 __________(写元素符号),氧化产物为_____________(写化学式)。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气(2KOCN+4KOH+3Cl2=2CO2↑+N2↑+6KCl+2H2O)。若反应转移120mol电子,则消耗0.1mol / LKOH_________L 。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解不生成O2只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,写出该反应的化学方程式_____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含Fe3+的S2O82-和I-的混合溶液中,反应S2O82-(aq)+2I-(aq)=2SO42-(aq)+I2(aq)的分解机理及反应进程中的能量变化如下:
步骤①:2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+(aq)
步骤②:2Fe2+(aq)+S2O82-(aq)=2Fe3+(aq)+2SO42-(aq)
下列有关该反应的说法正确的是
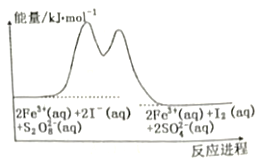
A. 化学反应速率与Fe3+浓度的大小有关
B. 该反应为吸热反应
C. Fe2+是该反应的催化剂
D. 若不加Fe3+,则正反应的活化能比逆反应的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有________(填字母)。
A 烧杯 B 500 mL容量瓶 C 漏斗 D 胶头滴管 E 玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为________ g。
(3)下列主要操作步骤的正确顺序是________(填序号)。
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度_______(填“偏高、偏低”或“不变”)。
Ⅱ.如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
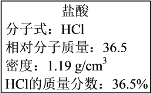
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。
A 溶液中HCl的物质的量 B 溶液的浓度
C 溶液中Cl-的数目 D 溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。该学生需要量取______mL上述浓盐酸进行配制。
Ⅲ.现有0.27Kg质量分数为10%的CuCl2溶液,则溶液中CuCl2的物质的量为___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com