
【题目】人体血液存在H2CO3/HCO3-、HPO42-/H2PO4-等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lg x[x表示c(H2CO3)/c(HCO3-)或c(HPO42-)/c(H2PO4-)]与pH的关系如图所示。已知碳酸pKal=6.4、磷酸pKa2=7.2(pKa= -lgKa)。则下列说法正确的是
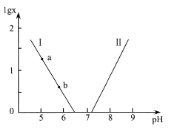
A. 曲线I表示lg c(HPO42-)/c(H2PO4-)与pH的变化关系
B. a-b的过程中,水的电离程度逐渐减小
C. 当c(H2CO3)=c(HCO3-)时,c(HPO42-)=c(H2PO4-)
D. 当pH增大时,c(HCO3-)c(H2PO4-)/c(HPO42-)逐渐减小
【答案】D
【解析】
H2CO3![]() HCO3-+H+的电离平衡常数Kal=c(H+)·c(HCO3-)/c(H2CO3),所以lgc(H2CO3)/c(HCO3-)=pKal-pH=6.4-pH,H2PO4-
HCO3-+H+的电离平衡常数Kal=c(H+)·c(HCO3-)/c(H2CO3),所以lgc(H2CO3)/c(HCO3-)=pKal-pH=6.4-pH,H2PO4-![]() HPO42-+H+的电离平衡常数Ka2=c(H+)·c(HPO42-)/c(H2PO4-),所以lgc(HPO42-)/c(H2PO4-)=pH-pKa2=pH-7.2,
HPO42-+H+的电离平衡常数Ka2=c(H+)·c(HPO42-)/c(H2PO4-),所以lgc(HPO42-)/c(H2PO4-)=pH-pKa2=pH-7.2,
A.当lgx=0时,pH分别为6.4、7.2;
B.酸对水的电离有抑制作用,酸性越强即pH越小,抑制作用越大,水的电离程度越小;
C.当c(H2CO3)=c(HCO3-)时,即lgc(H2CO3)/c(HCO3-)=0,溶液中pH=6.4,则lgc(HPO42-)/c(H2PO4-)=pH-7.2=6.4-7.2=-0.8;
D.c(HCO3-)·c(H2PO4-)/c(HPO42-)=c(HCO3-)·c(H+)/Ka2=Ka1×c(H2CO3)/Ka2,pH增大则H2CO3![]() HCO3-+H+正向进行,使c(H2CO3)减小。
HCO3-+H+正向进行,使c(H2CO3)减小。
A.当lgx=0时,pH分别为6.4、7.2,所以曲线I表示lgc(H2CO3)/c(HCO3-)=pKal-pH=6.4-pH,曲线II表示lgc(HPO42-)/c(H2PO4-)=pH-pKa2=pH-7.2,故A错误;
B.酸对水的电离有抑制作用,酸性越强即pH越小,抑制作用越大,水的电离程度越小,a-b的过程中pH增大,溶液酸性减弱,水的电离程度增大,故B错误;
C.当c(H2CO3)=c(HCO3-)时,即lgc(H2CO3)/c(HCO3-)=0,溶液中pH=6.4,则lgc(HPO42-)/c(H2PO4-)=pH-7.2=6.4-7.2=-0.8<0,即c(HPO42-)<c(H2PO4-),故C错误;
D、c(HCO3-)·c(H2PO4-)/c(HPO42-)=c(HCO3-)·c(H+)/Ka2=Ka1×c(H2CO3)/Ka2,pH增大则H2CO3![]() HCO3-+H+正向进行,使c(H2CO3)减小,Ka1、Ka2不变,所以pH增大时,c(HCO3-)c(H2PO4-)/c(HPO42-)逐渐减小,故D正确;
HCO3-+H+正向进行,使c(H2CO3)减小,Ka1、Ka2不变,所以pH增大时,c(HCO3-)c(H2PO4-)/c(HPO42-)逐渐减小,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】氯化铁是一种常见的水处理剂,无水氯化铁遇潮湿空气,极易吸水生成![]() 。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。

(1)实验开始时,先点燃______处的酒精灯![]() 填A或
填A或![]() 。A中发生反应的化学方程式为______。
。A中发生反应的化学方程式为______。
(2)![]() 装置中盛放的是饱和食盐水,其作用为______。
装置中盛放的是饱和食盐水,其作用为______。
(3)![]() 装置中的试剂为浓硫酸,其作用是______。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为______。
装置中的试剂为浓硫酸,其作用是______。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,
时,![]() 的
的![]() 溶液
溶液![]() ,
,![]() 的HCN溶液
的HCN溶液![]() 下列说法正确的是
下列说法正确的是
A.![]() 与HCN均为弱酸,酸性:
与HCN均为弱酸,酸性:![]()
B.![]() 时,水电离出来的
时,水电离出来的![]() 均为
均为![]() 的两种酸,酸的浓度:
的两种酸,酸的浓度:![]()
C.![]() 时,浓度均为
时,浓度均为![]() 的
的![]() 和NaCN溶液中,pH大小:
和NaCN溶液中,pH大小:![]()
D.![]() 时,量取100m
时,量取100m![]() 的
的![]() 溶液加水稀释到1000mL,所得溶液由水电离的
溶液加水稀释到1000mL,所得溶液由水电离的![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.次氯酸的电离方程式为:HClO = H+ + ClO-
B.c(H+)等于1×10-7mol·L-1的溶液一定是中性溶液
C.在CH3COONa溶液中,c(CH3COO-) < c(Na+)
D.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1 HCl溶液中的c(H+)的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)![]() NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)![]() H2(g)+HI(g)
H2(g)+HI(g)
达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下,反应①的平衡常数为
A.9B.16C.20D.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1molL、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法正确的是( )

A. Ka(HX)>Kb(NH3·H2O)
B. b点时c(NH4+)>c(HX)>c(OH—)=c(H+)
C. a、b、d几点中,水的电离程度d>b>a
D. a →b点过程中,可能存在c(X—)<c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 molA气体和2mol B气体在2L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g),若经2s后测得C的浓度为0.6mol·L-1,则
2C(g),若经2s后测得C的浓度为0.6mol·L-1,则
(1)用物质A表示的反应速率为____。
(2)用物质B表示的反应速率为____。
(3)2s时物质B的转化率为_____。
(4)2s时物质A的浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示。
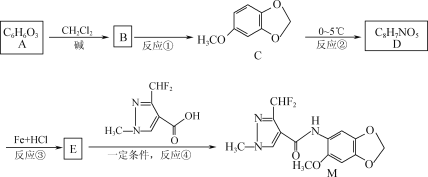
已知:
![]()
回答下列问题:
(1)化合物C中的含氧官能团为____________,反应④的反应类型为____________。
(2)写出E的结构简式:________________________。
(3)写出反应②的化学方程式:_____________________________________________。
(4)写出化合物C满足下列条件的一种同分异构体的结构简式:_________________。
① 含苯环结构,能在碱性条件下发生水解;
② 能与FeCl3发生显色反应;
③ 分子中含有4种不同化学环境的氢。
(5)已知CH3CH2CN![]() CH3CH2COOH。请以
CH3CH2COOH。请以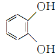 、CH2==CHCN和乙醇为原料合成化合物
、CH2==CHCN和乙醇为原料合成化合物 ![]() ,写出制备的合成路线流程图(无机试剂任用)_____。
,写出制备的合成路线流程图(无机试剂任用)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com