
【题目】(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。

(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。

【答案】P4(白磷,s)+3O2(g)=P4O6(g)△H= -1638kJ/mol 2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H= -1048.9kJ/mol N2(g)+3H2(g)![]() 2NH3(I) △H=2(a-b-c)kJ/mol
2NH3(I) △H=2(a-b-c)kJ/mol
【解析】
(1)白磷燃烧生成P4O6的合成方程式为P4(白磷)+3O2= P4O6,根据白磷和P4O6的分子结构,结合放出的热量=生成物的键能-反应物的键能计算;
(2)根据盖斯定律分析计算△H;
(3)根据反应热等于反应物总能量减去生成物总能量,结合图示计算反应热,并书写热化学方程式,注意反应物的物质的量和生成物的聚集状态。
(1)白磷燃烧生成P4O6的合成方程式为P4(白磷)+3O2= P4O6,根据白磷和P4O6的分子结构,放出的热量=生成物的键能-反应物的键能=12×360kJ-[(6×198)kJ+(3×498)kJ]=1638kJ,反应的焓变是-1638kJ/mol,则反应P4(白磷)燃烧生成P4O6的热化学方程式为:P4(白磷,s)+3O2(g)=P4O6(g)△H=-1638kJ/mol;故答案为:P4(白磷,s)+3O2(g)=P4O6(g) △H=-1638kJ/mol;
(2)肼和N2O4反应的化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g),①N2(g)+2O2(g)═N2O4(l) △H1═ -19.5kJmol-1,②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJmol-1,根据盖斯定律,②×2-①得到2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H=(-534.2kJmol-1)×2-(-19.5kJmol-1)=-1048.9kJ/mol,故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H=-1048.9kJ/mol;
(3)根据反应热等于反应物总能量减去生成物总能量计算反应热。由图可以看出,![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H=(a-b)kJ/mol,而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,所以有
H2(g)=NH3(g) △H=(a-b)kJ/mol,而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,所以有![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) △H=(a-b-c)kJ/mol,故热化学方程式为N2(g)+3H2(g)=2NH3(1) △H=2(a-b-c)kJmol-1,故答案为:N2(g)+3H2(g)=2NH3(1) △H=2(a-b-c)kJmol-1。
H2(g)=NH3(l) △H=(a-b-c)kJ/mol,故热化学方程式为N2(g)+3H2(g)=2NH3(1) △H=2(a-b-c)kJmol-1,故答案为:N2(g)+3H2(g)=2NH3(1) △H=2(a-b-c)kJmol-1。


科目:高中化学 来源: 题型:
【题目】在水溶液中,重铬酸钾K2Cr2O7存在以下平衡:Cr2O72-+H2O![]() 2CrO42-+2H+,下列说法正确的是( )
2CrO42-+2H+,下列说法正确的是( )
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大
D.该反应的平衡常数表达式是K=c2(CrO42-)c2(H+)/c(Cr2O72-)c(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将 0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ·mol-1 ,则H2SO4和Ba(OH)2反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在101kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1) △H =-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个1.0 L的恒容密闭容器中分别进行反应2X(g)+Y(g)![]() Z(g) ΔH,达到平衡。相关数据如下表。
Z(g) ΔH,达到平衡。相关数据如下表。
容器 | 温度/K | 物质的起始浓度/ mol·L-1 | 物质的平衡浓度/ mol·L-1 | ||
c(X) | c(Y) | c(Z) | c(Z) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | a |
III | 500 | 0.20 | 0.10 | 0 | 0.025 |
下列说法不正确的是
A. 平衡时,X的转化率:II>I
B. 平衡常数:K(II)>K(I)
C. 达到平衡所需时间:III<I
D. 反应的ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体,图 1 表示各物质浓度随时间的变化,图 2 表示速率随时间的变化,t2、t3、t4、t5 时刻各改变一种条件,且改变的条件均不同。若t4时刻 改变的条件是压强,则下列说法错误的是

A.若 t1=15 s,则前 15 s 的平均反应速率 v(C)=0.004 mol·L-1·s-1
B.该反应的化学方程式为 3A(g)![]() B(g)+2C(g)
B(g)+2C(g)
C.t2、t3、t5 时刻改变的条件分别是升高温度、加入催化剂、增大反应物浓度
D.若 t1=15 s,则 B 的起始物质的量为 0.04 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气已成为城市空气的主要污染源之一,其中的氮氧化物是重要污染物。
(1)汽车内燃机工作时产生NO的原理如图1所示:
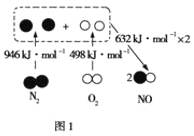
该反应的热化学方程式为______。
(2)治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0。若在一定温度下将2mol NO、1mol CO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图2所示。
N2(g)+2CO2(g) ΔH<0。若在一定温度下将2mol NO、1mol CO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图2所示。
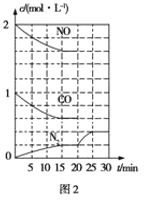
①则从开始到达到平衡状态的过程中,平均反应速率υ(CO2)=____,该温度下反应的平衡常数K=____(结果保留两位有效数字)
②20min时改变的条件可能是____
A.增大压强 C.减小CO2浓度且改用更高效的催化剂
B.降低温度 D.在恒温恒容条件下,充入He气体
③若保持温度不变,20min时向容器中充入CO、N2各0.6mol,平衡将____(填“正向”“逆向”或“不”)移动。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,向1L密闭容器中加入不同物质的量的NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压强的关系如图3所示。
N2(g)+2CO2(g),在恒温条件下,向1L密闭容器中加入不同物质的量的NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压强的关系如图3所示。
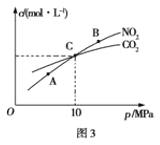
①下列不能说明该反应已达到平衡状态的是_____
a.C的质量不变 b. 混合气体的密度不再发生改变
c. v正(N2)=υ逆(CO2) d.混合气体的颜色不再改变
②计算C点时该反应的平衡常数Kp(C)=___(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.9g水中含有的原子总数为1.5×6.02×1023
B.1.0mol·L-1氯化镁溶液中含有Cl-数为2.0×6.02×1023
C.标准状况下,11.2L四氯化碳中含有的分子数为0.5×6.02×1023
D.钠与水反应时,每反应0.1mol钠,转移电子数为0.2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某测定O2含量的传感器工作原理如图所示。O2通过聚四氟乙烯膜进入传感器只与AlI3反应生成Al2O3和I2,RbAg4I5固体只传导Ag+,E为电位计。下列说法错误的是
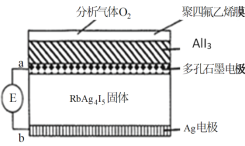
A.电子由a极移动到b极
B.RbAg4I5质量不发生变化
C.b极的电极反应式为:Ag+I--e-=AgI
D.该传感器协同总反应方程式为:3O2+4AlI3+12Ag=2Al2O3+12AgI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验“操作和现象”与“结论”对应且正确的是( )
操作和现象 | 结论 | |
A | 向盛有浓硫酸的试管中加入铜片,铜片很快开始溶解,并放出刺激性气味的气体 | 浓硫酸具有强氧化性 |
B | 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和硝酸银溶液,前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在平衡:I |
C | 向一定量的硝酸银溶液中先滴加KCl溶液,再滴加KI溶液,先出现白色沉淀,后出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 室温下,用pH试纸分别测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com