
【题目】下列说法正确的是( )
A.9g水中含有的原子总数为1.5×6.02×1023
B.1.0mol·L-1氯化镁溶液中含有Cl-数为2.0×6.02×1023
C.标准状况下,11.2L四氯化碳中含有的分子数为0.5×6.02×1023
D.钠与水反应时,每反应0.1mol钠,转移电子数为0.2×6.02×1023
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化关系:
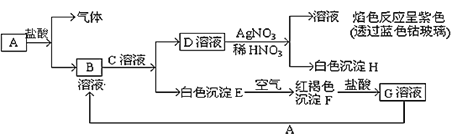
试回答:
(1)写出各物质的化学式A________________、D___________、F_______ 。
(2)检验G溶液中阳离子所选用的试剂是_______(写化学式),实验现象是______。
(3)写出B溶液与C溶液反应的化学方程式___________________________ 。
(4)写出G溶液与A反应的离子反应方程式___________________________ 。
(5)上图中共有6个化学反应,其中属于氧化还原反应的有几个?________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,科学家成功研制出一种电源,该电源在消耗二氧化碳的同时,还可释放电能。电源电极为铝电极和多孔碳电极,电解质溶液为草酸盐溶液,放电过程中草酸盐浓度基本不变,电源示意图如图所示。下列有关该电源的说法正确的是

A.铝电极电势高于多孔碳电极
B.用该电源电解饱和食盐水,理论上,每消耗1mol二氧化碳可收集到标准状况下 11.2L 氢气
C.若生成0.5 mol 草酸铝,有3mol电子通过电解质溶液
D.正极的电极反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。

(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择合适的完成指定转化。
试剂:S、CO2、Na2CO3溶液、Na3PO4溶液、K2SO4溶液、浓硝酸、浓盐酸
①K2O(一种碱性氧化物)K2CO3的化学方程式:___;
②PH3PO4的化学方程式:___;
③浓硫酸SO2的化学方程式:___。
(2)根据如图所示物质的转化信息书写相应的反应方程式。

①“反应Ⅱ”为复分解反应,写出该反应的化学方程式:___;
②“反应Ⅰ”的产物之一为NaCl,写出该反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镁(Mg3N2)是一种高强度钢冶炼的添加剂,现某学习小组利用下列装置制备少量氮化镁。
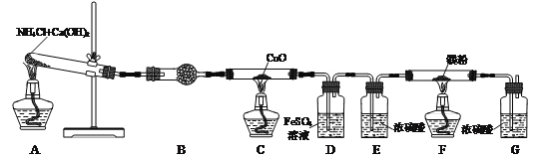
已知:Ⅰ.3Mg+N2![]() Mg3N2;Ⅱ.Mg3N2+6H2O=3Mg(OH)2+2NH3↑
Mg3N2;Ⅱ.Mg3N2+6H2O=3Mg(OH)2+2NH3↑
(1)检查该装置气密性的方法是___。
(2)写出装置A中发生反应的化学方程式:___,装置B中试剂的名称是___。
(3)反应一段时间后装置C中黑色固体变为红色,并有水珠出现。装置C中发生反应的化学方程式为___。
(4)装置D中FeSO4溶液的作用是___。
(5)实验过程中装置A和F应该先加热的是___处。
(6)装置F中有氮化镁生成,写出通过实验验证氮化镁生成的操作及现象:取少量装置F反应后的固体于试管中,___,说明其中含氮化镁。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素,只有W为金属元素。甲、乙、丙分别为X、Z、W三种元素所对应的单质。A、B、C、D均为由X、Y、Z三种元素组成的化合物,化合物B的稀溶液常用于保存动物标本。它们的转化关系如图所示。下列说法错误的是

A.X与Z可组成非极性分子
B.原子半径大小关系是:r(X)<r(Z)<r(Y)<r(W)
C.四种化合物中B的沸点最低
D.四种化合物中Y原子的杂化方式有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸被称为“国防化工之母”,某化学兴趣小组对浓硝酸与铜片的反应进行探究,请完成下列问题。
(1)写出反应刚开始阶段化学方程式,并用“双线”桥表达电子转移的方向和数目______________,该阶段反应现象为_________。
(2)最终铜有剩余,则反应将要结束时的离子方程式是________;待反应停止时,再加入稀硫酸,这时铜片上又有气泡产生,其原因是_______。
(3)用试管将反应产生的NO2收集满并倒立在足量的水中,待试管中液面不再上升时,试管中剩余气体的体积约为原气体体积的________(相同条件下)
(4)若12.8g铜与一定质量的浓硝酸反应,铜完全溶解时,产生NO和NO2混合气体共5.6L(标准状况),则反应中转移的电子的物质的量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知101kPa时的辛烷的燃烧热为5518kJ/mol,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ/mol,则下列热化学方程式书写正确的是
①C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l);△H=+5518kJ/mol;
O2(g)=8CO2(g)+9H2O(l);△H=+5518kJ/mol;
②C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/mol;
O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/mol;
③![]() H2SO4(aq)+Ba(OH) 2(aq)=
H2SO4(aq)+Ba(OH) 2(aq)=![]() BaSO4(s)+H2O(l);△H=﹣57.3kJ/mol;
BaSO4(s)+H2O(l);△H=﹣57.3kJ/mol;
④H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol.
A.①③B.②③C.②④D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com