
【题目】某小组同学以不同方案探究Cu粉与FeCl3溶液的反应。
(1)甲同学向FeCl3溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,由此证明发生了反应,其离子方程式是______________________________________________。
(2)乙同学通过反应物的消耗证明了上述反应的发生:将Cu粉加入到滴有少量KSCN的FeCl3溶液中,观察到溶液红色褪去,有白色沉淀A产生。
① 针对白色沉淀A,查阅资料:A可能为CuCl和CuSCN(其中硫元素的化合价为-2价)中的一种或两种。实验过程如下:

请回答:
Ⅰ. 根据白色沉淀B是__________________(填化学式),判断沉淀A中一定存在CuSCN。
Ⅱ. 仅根据白色沉淀A与过量浓HNO3反应产生的实验现象,不能判断白色沉淀A中一定存在CuSCN,从氧化还原角度说明理由:_______________________________________________________。
Ⅲ. 向滤液中加入a溶液后无明显现象,说明A不含CuCl,则a是________________(填化学式)。
根据以上实验,证明A仅为CuSCN。
② 进一步查阅资料并实验验证了CuSCN的成因,将该反应的方程式补充完整:
_______Cu2+ + _______SCN![]() = _______CuSCN↓ + _______ (SCN)2
= _______CuSCN↓ + _______ (SCN)2
③ 结合上述过程以及Fe(SCN)3 Fe3+ + 3SCN![]() 的平衡,分析(2)中溶液红色褪去的原因:_________________。
的平衡,分析(2)中溶液红色褪去的原因:_________________。
(3)已知(SCN)2称为拟卤素,其氧化性与Br2相近。将KSCN溶液滴入(1)所得的溶液中,观察到溶液变红色,则溶液变红的可能原因是_______________________________________________。
【答案】Cu + 2Fe3+ = Cu2+ + 2Fe2+ BaSO4 +1价铜也可将浓HNO3还原 AgNO3 2Cu2+ + 4SCN- = 2CuSCN↓ + (SCN)2 Cu和Fe3+反应生成Cu2+使c(Fe3+)减小 ![]() 和
和![]() 反应生成
反应生成![]() 和
和![]() 使
使![]() 减小,Cu2+和SCN-反应生成CuSCN沉淀使c(SCN-)减小,均使该平衡正向移动,导致Fe(SCN)3浓度减小,溶液红色褪去 Fe3+有剩余 空气中的O2将Fe2+氧化 (SCN)2将Fe2+氧化
减小,Cu2+和SCN-反应生成CuSCN沉淀使c(SCN-)减小,均使该平衡正向移动,导致Fe(SCN)3浓度减小,溶液红色褪去 Fe3+有剩余 空气中的O2将Fe2+氧化 (SCN)2将Fe2+氧化
【解析】
(1)向![]() 溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,说明生成了铜离子;
溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,说明生成了铜离子;
(2)①Ⅰ.根据流程图沉淀B不溶于酸,故该沉淀是硫酸钡;
Ⅱ. ![]() 中铜元素显+1价,也具有还原性,能够还原硝酸;
中铜元素显+1价,也具有还原性,能够还原硝酸;
Ⅲ.用硝酸银溶液检验滤液中是否含有氯离子即可;
②根据氧化还原规律和元素守恒配平;
③![]() 和
和![]() 反应生成
反应生成![]() 和
和![]() 使
使![]() 减小,
减小,![]() 和
和![]() 反应生成
反应生成![]() 沉淀使
沉淀使![]() 减小;
减小;
(3)溶液变红色,说明溶液中含有![]() 。
。
(1)向![]() 溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,说明生成了铜离子,离子方程式为:
溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,说明生成了铜离子,离子方程式为:![]() ,
,
故答案为:![]() ;
;
(2)①Ⅰ.根据流程图,溶液中含有过量的硝酸,即沉淀B不溶于酸,故该沉淀是硫酸钡,
答案为:![]() ;
;
Ⅱ. ![]() 中铜元素显+1价,也具有还原性,能够还原硝酸,故仅根据白色沉淀A与过量浓
中铜元素显+1价,也具有还原性,能够还原硝酸,故仅根据白色沉淀A与过量浓![]() 反应产生的实验现象,不能判断白色沉淀A中一定存在
反应产生的实验现象,不能判断白色沉淀A中一定存在![]() ,
,
答案为:+1价铜也可将浓![]() 还原;
还原;
Ⅲ.若白色沉淀A中含有![]() ,则滤液中含有氯离子,故用硝酸银溶液检验滤液中是否含有氯离子即可,
,则滤液中含有氯离子,故用硝酸银溶液检验滤液中是否含有氯离子即可,
答案为:![]() ;
;
②根据氧化还原规律,一个![]() 转移1个电子,生成一个
转移1个电子,生成一个![]() 转移2个电子,故
转移2个电子,故![]() 和
和![]() 的系数比为2:1,根据元素守恒配平即可,
的系数比为2:1,根据元素守恒配平即可,
答案为:![]() ;
;
③![]() 和
和![]() 反应生成
反应生成![]() 和
和![]() 使
使![]() 减小,
减小,![]() 和
和![]() 反应生成
反应生成![]() 沉淀使
沉淀使![]() 减小,均使
减小,均使![]() 正向移动,导致
正向移动,导致![]() 浓度减小,溶液红色褪去,
浓度减小,溶液红色褪去,
故答案为:![]() 和
和![]() 反应生成
反应生成![]() 和
和![]() 使
使![]() 减小,
减小,![]() 和
和![]() 反应生成
反应生成![]() 沉淀使
沉淀使![]() 减小,均使该平衡正向移动,导致
减小,均使该平衡正向移动,导致![]() 浓度减小,溶液红色褪去;
浓度减小,溶液红色褪去;
(3)将![]() 溶液滴入(1)所得的溶液中,观察到溶液变红色,说明溶液中含有
溶液滴入(1)所得的溶液中,观察到溶液变红色,说明溶液中含有![]() ,
,![]() 有可能是反应剩余的,或空气中的氧气将
有可能是反应剩余的,或空气中的氧气将![]() 氧化生成的,根据题意
氧化生成的,根据题意![]() 也有氧化性,故也有可能是
也有氧化性,故也有可能是![]() 将
将![]() 氧化为
氧化为![]() ,
,
故答案为:![]() 有剩余;空气中的
有剩余;空气中的![]() 将
将![]() 氧化;
氧化;![]() 将
将![]() 氧化。
氧化。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】如图所示是探究铁发生腐蚀的装置图。发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。下列说法中不正确的是( )
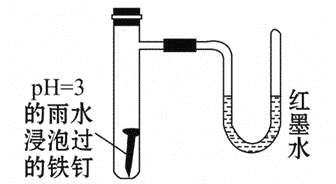
A.开始时发生的是析氢腐蚀
B.一段时间后发生的是吸氧腐蚀
C.两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+
D.析氢腐蚀的总反应式为2Fe+O2+2H2O=2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸可用甲苯为原料合成。已知①苯环上的硝基可被还原为氨基:![]() +3Fe+6HCl→
+3Fe+6HCl→![]() +3FeCl2+2H2O,产物苯胺还原性强,易被氧化;②-CH3为邻、对位取代定位基,而-COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是
+3FeCl2+2H2O,产物苯胺还原性强,易被氧化;②-CH3为邻、对位取代定位基,而-COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是
A.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
B.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
C.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
D.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是
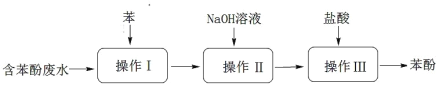
A.操作Ⅰ为萃取、分液,萃取剂也可以用选用 CCl4
B.苯酚钠是离子化合物,在苯中的溶解度比在水中的小
C.通过操作Ⅱ,苯可循环使用,三步操作均需要分液漏斗
D.苯酚沾到皮肤上,需用 NaOH 溶液清洗后,再用大量水不断冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,取一定量冰醋酸,进行如下实验:
① 将冰醋酸配制成0.1 mol·L-1醋酸溶液;
② 取20 mL①所配溶液,加入a mL 0.1 mol·L-1 NaOH溶液,充分反应后,测得溶液pH=7;
③ 向②所得溶液中继续滴加稀盐酸,直至溶液中n(Na+) = n(Cl-)。
下列说法正确的是
A.①中:所得溶液的pH=1
B.②中:a=20
C.③中:所得溶液中c(CH3COO-)<c(H+),且pH<7
D.①与③所得溶液相比,等体积时所含CH3COOH分子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为工业合成氨的流程图。有关说法错误的是

A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是
A.尼龙属于有机高分子材料
B.稻草秸秆和甘蔗渣中富含纤维素,可以用它来制造纸张
C.将大桥钢制构件用导线与石墨相连可以起到防腐的作用
D.刘禹锡![]() 浪淘沙
浪淘沙![]() 诗句“千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”“漉”相当于“过滤”
诗句“千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”“漉”相当于“过滤”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2与CH4可制得合成气:CH4(g)+CO2(g)2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:
容器 | 起始物质的量/mol | CO2平衡转化率(α) | |||||
编号 | 容积/L | 条件 | CH4(g) | CO2(g) | CO(g) | H2(g) | |
Ⅰ | 2 | 恒温恒容 | 2 | 1 | 0 | 0 | 50% |
Ⅱ | 1 | 0.5 | 1 | 0 | 0 | ||
Ⅲ | 1 | 绝热恒容 | 1 | 0.5 | 0 | 0 | - |
下列说法正确的是
A.T K时,反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡常数为1/3
B.容器Ⅱ中反应达到平衡时,α(CO2,Ⅱ)=50%
C.容器Ⅲ中反应达到平衡时反应热在123.5—247 kJ·mol-1范围内
D.容器Ⅱ中反应达到平衡时,再投入0.5 mol CH4、0.25 mol CO,反应达到新平衡前,v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一固定容积的密闭容器中进行如下反应N2+3H2![]() 2NH3,下列情况一定能说明反应已达到平衡的是
2NH3,下列情况一定能说明反应已达到平衡的是
①容器内压强不随时间而变化
②单位时间内,有3molH2反应,同时有2molNH3生成
③气体的密度不随时间而变化
④单位时间内,有1molN2生成,同时有2molNH3生成
⑤用N2、H2、NH3表示的该反应的化学反应速率之比为1∶3∶2
⑥气体的平均摩尔质量不随时间而变化
A.①④⑥ B.①②③ C. ②③⑤ D.①②⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com