
【题目】下图是中学教材中元素周期表的一部分,其中标出A~R 15种元素,试根据它们回答下列问题(填具体元素符号或化学式):
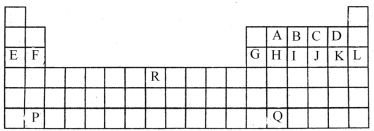
(1)化学性质最不活泼的是____,原子半径最小的是(除稀有气体元素)___属于过渡元素的是____(填A~R中的代号)。
(2)最高价氧化物对应的水化物中酸性最强的是_____,单质中氧化性最强的是________,第三周期元素形成的简单离子中半径最小的是______。
(3)F与K形成的化合物溶于水发生电离,所破坏的化学键为______。
(4)Q在元素周期表中的位置是_____,B、C可形成化合物B2C,该化合物的核外电子总数为_____。
(5)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:____________。
(6)元素E与元素F相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是______(填序号)。
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强
【答案】Ar F R HClO4 F2 Al3+ 离子键 第六周期ⅣA族 22 H++OH-===H2O Na cd
【解析】
根据元素周期表排布规律分析解答;根据元素周期律的表现分析解答;根据金属性、非金属性强弱判断规律分析解答。
根据元素周期表可知,A为C元素,B为N元素,C为O元素,D为F元素,E为Na元素,F为Mg元素,G为Al元素,H为Si元素,I为P元素,J为S元素,K为Cl元素,L为Ar元素,R为Fe元素,P为Ba元素,Q为Pb元素;
(1)化学性质最不活泼的是稀有气体Ar,原子半径最小的是(除稀有气体元素)第二周期最右边的元素F,其中属于过渡元素的是R即Fe元素,故答案为:Ar,F,R;
(2)非金属性越强,对应的最高价氧化物对应的水化物中酸性越强,元素周期表中非金属性最强的是F其次是O,但是F和O元素无正价,其次为Cl,所以最高价氧化物对应的水化物中酸性最强的是HClO4,非金属性越强,氧化性越强,非金属性最强的是F,其氧化性最强的单质为F2,第三周期中形成的简单离子有2个电子层的有Na+、Mg2+、Al3+,其他元素形成的简单离子均为三个电子层,所以第三周期元素形成的简单离子中半径最小的是两个电子层的Al3+,故答案为:HClO4,F2,Al3+;
(3)F是Mg元素与K是Cl元素形成的化合物MgCl2是离子化合物,仅含有离子键,溶于水发生电离,所破坏的化学键为离子键,故答案为:离子键;
(4)Q是Pb元素,根据元素周期表信息可知,Pb在元素周期表中的位置是第六周期ⅣA族,B为N元素、C为O元素,可形成化合物B2C即N2O,该化合物的核外电子总数为7×2+8=22,故答案为:第六周期ⅣA族,22;
(5)P为Ba元素,Ba的最高价氧化物对应的水化物即Ba(OH)2与B即N元素的最高价氧化物对应的水化物即HNO3反应生成硝酸钡和水,离子方程式为H++OH-===H2O;
(6)元素E为Na与元素F为Mg元素,元素周期表中,同周期元素从左向右金属性逐渐减弱,则金属性Na>Mg,金属性越强,对应的最高价氧化物的水化物的碱性越强,则d正确,金属性越强,则其单质与水或酸反应越剧烈,则c正确;金属性不能用氢化物性质比较,故b错误;金属性与单质与酸反应得失电子数无关,故a错误,故答案为:Na,cd。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】为除去括号内的杂质,所选用的试剂或方法不正确的是
A. Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B. NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C. Na2O2粉末(Na2O),将混合物在氧气中加热
D. Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是

A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.鉴别氢氧化铝胶体(无色)和食盐水,可以不用任何试剂
B.鉴别白糖水和食盐溶液,可以不用任何试剂
C.鉴别粉笔末与水、豆油与水组成的浊液,可以不用任何试剂
D.鉴别氯化钠溶液与硫酸铜两种溶液,可以不用任何试剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)下列纯净物中:a.NaOH b.Ar c.MgCl2 d.HCl e.NH3 f.KNO3
①不含化学键的物质是_______(填序号,下同)。
②既含有离子键又含有共价键的物质是______。
③只含有离子键的物质是________。
(2)下列变化中,不需要破坏化学键的是______。
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
(3)实验室盛放碱液的试剂瓶不能用玻璃塞,以氢氧化钠为例,用离子方程式表示其原因:_________,任写一个制造普通玻璃的主要反应的化学方程___________________。
(4)硅是良好的半导体材料,写出工业上生产粗硅的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,俄罗斯科学家再次合成117号元素,其中有5个![]() X,1个
X,1个![]() X。下列关于
X。下列关于![]() X和
X和![]() X的说法不正确的是( )
X的说法不正确的是( )
A. 是两种核素
B. 互为同位素
C. 中子数分别为176和177
D. X元素的相对原子质量一定是176.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 液态HCl不导电,所以HCl是非电解质
B. BaSO4溶于水的部分能够电离,所以BaSO4是电解质
C. 液态Cl2不导电,所以Cl2是非电解质
D. NH3的水溶液能够导电,所以NH3是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)
![]()

(1)甲、乙两仪器的名称是 ______、 _______。
(2)在甲中装入浓硫酸,乙中装入铜片,连接A、C、E进行实验,写出A中发生反应的化学方程式___;若丙中装入的是品红溶液,则反应后的现象是_____;若丙中装入的是酸性高锰酸钾溶液,反应后溶液褪色,说明生成的气体有___性;若丙中装入的是氢硫酸溶液,反应后溶液变浑浊,说明生成气体有____性。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(铜片放在有孔塑料板上)可制得NO2并进行有关实验。
①要在丁中收集NO2气体,应采取的操作步骤为:关闭止水夹___,打开止水夹____;
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹ab,再打开止水夹c,使烧杯中的水进入试管丁中的操作是_____。
③试管丁中的NO2与水充分反应后,所得溶液中溶质的物质的量浓度是____(保留2位有效数值,气体按标准状况计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酸异丁酯(isobutyl acetate)具有菠萝香气,主要用作漆类的溶剂和配制香精。实验室制备丙酸异丁酯的反应、装置示意图和有关信息如下:


实验步骤:
在圆底烧瓶中加入3.7g的异丁醇,7.4 g的丙酸、数滴浓硫酸和2~3片碎瓷片,控温106~125℃,反应一段时间后停止加热和搅拌,反应液冷却至室温后,用饱和NaHCO3溶液洗涤分液后加入少量无水硫酸镁固体干燥,静置片刻,过滤除去硫酸镁固体,进行常压蒸馏纯化,收集130~136℃馏分,得丙酸异丁酯3.9 g。
回答下列问题:
(l)装置A的名称是__________。
(2)实验中的硫酸的主要作用是___________。
(3)用过量丙酸的主要目的是______________________。
(4)用饱和NaHCO3溶液洗涤粗酯的目的是____________。
(5)在洗涤、分液操作中,应充分振荡,然后静置,待分层后_________(填字母)。
A.直接将丙酸异丁酯从分液漏斗上口倒出
B.直接将丙酸异丁酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将丙酸异丁酯从上口倒出
D.先将水层从分液漏斗的下口放出,再将丙酸异丁酯从下口放出
(6)本实验丙酸异丁酯的产率是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com