
【题目】某溶液中含有两种溶质 NaCl 和 H2SO4,它们的物质的量之比为 3∶1。用石墨作电极电 解该混合溶液时,根据电极产物,可明显分为三个阶段。下列叙述不正确的是
A. 阴极自始至终只逸出 H2 B. 阳极先逸出 Cl2,后逸出 O2
C. 溶液 pH 不断增大,最后为 7 D. 电解最后阶段为电解水
【答案】C
【解析】
根据电解原理:阳极离子的放电顺序:银离子>铜离子>氢离子,阴极离子的放电顺序:氯离子>氢氧根离子,溶液中含有两种溶质NaCl和H2SO4,根据电解原理判断放电的离子.
可以将溶质看成3molNaCl和1molH2SO4,再转化一下思想,可以看成2molHCl,1molNa2SO4,1molNaCl,由于1molNa2SO4自始至终无法放电,且其溶液pH=7,暂时可以忽略,则电解过程可先看成电解HCl,再电解NaCl,最后电解水,
即2HCl![]() H2↑+Cl2↑,2NaCl+2H2O
H2↑+Cl2↑,2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,2H2O
2NaOH+H2↑+Cl2↑,2H2O![]() 2H2↑+O2↑,生成的NaOH为碱性,pH大于7。
2H2↑+O2↑,生成的NaOH为碱性,pH大于7。
A、阴极自始自终是氢离子放电,只析出H2,故A正确;
B、阳极氯离子先于氢氧根离子放电,先析出Cl2,后析出O2,故B正确;
C、溶液pH不断增大,最后生成的NaOH为碱性,pH大于7,故C错误;
D、电解最后阶段为电解水,故D正确;
故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 足量的KI溶液与FeCl3溶液反应后,用CCl4萃取其中的I2,分液,在水溶液中滴加KSCN溶液仍呈血红色,说明该反应有一定的限度
B. 在一定条件下,一份双氧水样品经过2 h,H2O2的浓度从0.05 mol·L-1下降到0.03 mol·L-1,H2O2在这2 h中分解的平均反应速率约为0.015 mol·L-1·h-1
C. 其他条件相同时,反应温度升高,对于吸热反应,反应速率加快,对于放热反应,反应速率减慢
D. 一定条件下,固定体积的容器中发生反应A(g)+B(g) ![]() 2C(g),当容器内A、B、C的浓度之比为1∶1∶2时,该反应处于平衡状态
2C(g),当容器内A、B、C的浓度之比为1∶1∶2时,该反应处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中,加入2molA和1molB发生下列反应并且达到化学平衡状态,2A(g)+B(g) ![]() 3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
A.4molA+2molB B.3molC+1molB+1molD+1molA
C.2molA+1molB+1molD D.1molA+0.5molB + 1.5molC+0.5molD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)草酸的组成用H2C2O4表示,为了测定某草酸溶液的浓度,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液,取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amolL﹣1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O.
试回答:
(1)实验中,标准液KMnO4溶液应装在_____式滴定管中,因为______________;
(2)实验中眼睛注视_____________________,直至滴定终点.判断到达终点的现象是_________;
(3)实验中,下列操作(其它操作均正确),会对所测草酸浓度有什么影响?(填偏大、偏小、无影响)
A.滴定前仰视刻度,滴定后俯视刻度_________;
B.锥形瓶在盛放待测液前未干燥,有少量蒸馏水_________;
C.滴定过程中摇动锥形瓶,不慎将瓶内的溶液溅出一部分_________;
(II)用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_________.
(2)烧杯间填满碎纸条的作用是_________________________________.
(3)依据该学生的实验数据计算,该实验测得的中和热△H=___________;(结果保留一位小数)
序号 | 起始温度t1℃ | 终止温度t2℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究原电池原理,设计如图装置。下列叙述正确的是( )
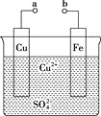
A. a和b不连接时,铁片上会有![]() 产生
产生
B. a和b用导线连接时,铁片上发生的反应为![]()
C. a和b用导线连接时,电子由a流向b
D. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律的表述正确的是( )
A.原子序数为15的元素的最高化合价为+3
B.ⅦA族元素是同周期中非金属性最强的元素
C.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
D.I A族元素的金属性一定比ⅡA族元素的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状 况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不符合第三周期主族元素性质特征的是
A. 从左到右原子半径逐渐减小
B. 从左到右非金属性逐渐增强
C. 从左到右金属元素的最高价氧化物的水化物的碱性逐渐减弱
D. 从左到右非金属元素的氧化物的水化物的酸性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com