
ΓΨΧβΡΩΓΩΕΧ÷ήΤΎ÷ςΉε‘ΣΥΊ XΓΔYΓΔZΓΔWΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§ΥΡ÷÷‘ΣΥΊ–Έ≥…ΒΡΒΞ÷ “ά¥ΈΈΣmΓΔnΓΔpΓΔqΘΜrΓΔtΓΔu «’β–©‘ΣΥΊΉι≥…ΒΡΕΰ‘ΣΜ·ΚœΈοΘ§Τδ÷–uΈΣΤœΧ―ΨΤ÷–ΒΡ“÷Ψζ≥…Ζ÷ΘΜ25 ΓφΘ§0.01 mol/LΒΡv»ή“Κ÷–ΘΚ  = 1.0ΓΝ10-10ΓΘ…œ ωΈο÷ ΒΡΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
= 1.0ΓΝ10-10ΓΘ…œ ωΈο÷ ΒΡΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «

A. ΦρΒΞάκΉ”ΑκΨΕΘΚW>Y>Z>X
B. WΘ§YΖ÷³e”κX‘ΣΥΊ–Έ≥…ΒΡΦρΒΞΜ·ΚœΈοΒΡΖ–ΒψΘΚ Y> W
C. Z2YΚΆZXΕΦ÷Μ¥φ‘ΎάκΉ”Φϋ
D. vΡή“÷÷ΤΥ°ΒΡΒγάκΘ§uΡή¥ΌΫχΥ°ΒΡΒγάκ
ΓΨ¥πΑΗΓΩD
ΓΨΫβΈωΓΩ25 ΓφΘ§0.01 mol/LΒΡv»ή“Κ÷–ΘΚ 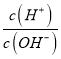 = 1.0ΓΝ10-10Θ§ΥΒΟςv «“Μ‘Σ«ΩΦνΘ§v «NaOHΘΜuΈΣΤœΧ―ΨΤ÷–ΒΡ“÷Ψζ≥…Ζ÷Θ§u «SO2ΘΜXΓΔYΓΔZΓΔWΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Υυ“‘XΓΔYΓΔZΓΔWΖ÷±π «HΓΔOΓΔNaΓΔSΥΡ÷÷‘ΣΥΊΘΜΦρΒΞάκΉ”ΑκΨΕΘΚS2->O2->Na+>H+Θ§Ι A’ΐ»ΖΘΜH2OΒΡΖ–Βψ¥σ”ΎH2SΘ§Ι B’ΐ»ΖΘΜNa2OΓΔNaH÷Μ¥φ‘ΎάκΉ”ΦϋΘ§Ι C’ΐ»ΖΘΜΕΰ―θΜ·ΝρΒΡΥ°»ή“Κ «―«ΝρΥαΘ§Ρή“÷÷ΤΥ°ΒΡΒγάκΘ§Ι D¥μΈσΓΘ
= 1.0ΓΝ10-10Θ§ΥΒΟςv «“Μ‘Σ«ΩΦνΘ§v «NaOHΘΜuΈΣΤœΧ―ΨΤ÷–ΒΡ“÷Ψζ≥…Ζ÷Θ§u «SO2ΘΜXΓΔYΓΔZΓΔWΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Υυ“‘XΓΔYΓΔZΓΔWΖ÷±π «HΓΔOΓΔNaΓΔSΥΡ÷÷‘ΣΥΊΘΜΦρΒΞάκΉ”ΑκΨΕΘΚS2->O2->Na+>H+Θ§Ι A’ΐ»ΖΘΜH2OΒΡΖ–Βψ¥σ”ΎH2SΘ§Ι B’ΐ»ΖΘΜNa2OΓΔNaH÷Μ¥φ‘ΎάκΉ”ΦϋΘ§Ι C’ΐ»ΖΘΜΕΰ―θΜ·ΝρΒΡΥ°»ή“Κ «―«ΝρΥαΘ§Ρή“÷÷ΤΥ°ΒΡΒγάκΘ§Ι D¥μΈσΓΘ


 –Γ―ßΩΈ ±Ής“Β»ΪΆ®ΝΖΑΗœΒΝ–¥πΑΗ
–Γ―ßΩΈ ±Ής“Β»ΪΆ®ΝΖΑΗœΒΝ–¥πΑΗ ΫπΑφΩΈΧΟΩΈ ±―ΒΝΖœΒΝ–¥πΑΗ
ΫπΑφΩΈΧΟΩΈ ±―ΒΝΖœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬±μ «Ρ≥Ά§―ßΧΫΨΩNa2SO3»ή“ΚΚΆΗθ(VI)―Έ»ή“ΚΖ¥”ΠΙφ¬…ΒΡ Β―ιΦ«¬ΦΘ§“―÷ΣΘΚCr2O72-(≥»…Ϊ)+ H2O![]() 2CrO42-(ΜΤ…Ϊ)+ 2H+
2CrO42-(ΜΤ…Ϊ)+ 2H+
–ρΚ≈ | a | b | œ÷œσ | |
| 1 | 2 mL 0.05 molΓΛL1 K2Cr2O7»ή“Κ(pH = 2) | 3ΒΈ±ΞΚΆNa2SO3»ή“Κ(pH = 9) | »ή“Κ±δ¬Χ…Ϊ(Κ§Cr3+) |
2 | 2 mL 0.1 molΓΛL1 K2CrO4»ή“Κ(pH = 8) | 3ΒΈ±ΞΚΆNa2SO3»ή“Κ | »ή“ΚΟΜ”–Οςœ‘±δΜ· | |
3 | 2 mL±ΞΚΆNa2SO3»ή“Κ | 3ΒΈ0.05 molΓΛL1 K2Cr2O7»ή“Κ | »ή“Κ±δΜΤ…Ϊ | |
4 | 2 mL’τΝσΥ° | 3ΒΈ0.05 molΓΛL1 K2Cr2O7»ή“Κ | »ή“Κ±δ≥…«≥≥»…Ϊ |
œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A. Β―ι1÷–ΒΡ¬Χ…Ϊ»ή“Κ÷–Κ§”–SO42-
B. Β―ι1ΓΔ2ΒΡa»ή“Κ÷–ΥυΚ§ΒΡάκΉ”÷÷άύœύΆ§
C. œρ Β―ι3»ή“Κ÷–ΦΧ–χΒΈΦ”ΙΐΝΩΝρΥαΩ… Ι»ή“Κ±δΈΣ«≥≥»…Ϊ
D. Β―ι4ΒΡΡΩΒΡ «≈≈≥ΐœΓ ΆΕ‘»ή“Κ―’…Ϊ±δΜ·‘λ≥…ΒΡ”Αœλ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σ“ΜΕ®Έ¬Ε»œ¬Θ§X(g)+2Y(g) ![]() mZ(g)ΘΜΓςH=-akJ/mol(aΘΨ0)Θ§œ÷”–ΦΉΓΔ““ΝΫ»ίΜΐœύΒ»«“ΙΧΕ®ΒΡΟή±’»ίΤςΘ§‘Ύ±Θ≥÷ΗΟΈ¬Ε»œ¬Θ§œρΟή±’»ίΤςΦΉ÷–Ά®»κ1molXΚΆ2molYΘ§¥οΒΫΤΫΚβΉ¥Χ§ ±Θ§Ζ≈≥ω»»ΝΩbkJΘΜœρΟή±’»ίΤς““÷–Ά®»κ2molXΚΆ4molYΘ§¥οΒΫΤΫΚβΉ¥Χ§ ±Θ§Ζ≈≥ω»»ΝΩckJΘ§«“2bΘΦcΘ§‘ρœ¬Ν–Ης÷ΒΙΊœΒ’ΐ»ΖΒΡ «
mZ(g)ΘΜΓςH=-akJ/mol(aΘΨ0)Θ§œ÷”–ΦΉΓΔ““ΝΫ»ίΜΐœύΒ»«“ΙΧΕ®ΒΡΟή±’»ίΤςΘ§‘Ύ±Θ≥÷ΗΟΈ¬Ε»œ¬Θ§œρΟή±’»ίΤςΦΉ÷–Ά®»κ1molXΚΆ2molYΘ§¥οΒΫΤΫΚβΉ¥Χ§ ±Θ§Ζ≈≥ω»»ΝΩbkJΘΜœρΟή±’»ίΤς““÷–Ά®»κ2molXΚΆ4molYΘ§¥οΒΫΤΫΚβΉ¥Χ§ ±Θ§Ζ≈≥ω»»ΝΩckJΘ§«“2bΘΦcΘ§‘ρœ¬Ν–Ης÷ΒΙΊœΒ’ΐ»ΖΒΡ «
A. a=b B. 2aΘΦc C. mΘΦ3 D. mΘΨ3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν––π ω÷–Θ§¥μΈσΒΡ «(ΓΓΓΓ)
A.±Ϋ”κ≈®œθΥαΓΔ≈®ΝρΥαΙ≤»»≤Δ±Θ≥÷55-60ΓφΖ¥”Π…ζ≥…œθΜυ±Ϋ
B.““±ΫΡήΖΔ…ζ―θΜ·Ζ¥”ΠΘ§ΒΪ≤ΜΡήΖΔ…ζΜΙ‘≠Ζ¥”Π
C.““œ©”κδεΒΡΥΡ¬»Μ·ΧΦ»ή“ΚΖ¥”Π…ζ≥…1Θ§2-Εΰδε““Άι
D.±Ϋ““œ©‘ΎΚœ ΧθΦΰœ¬¥ΏΜ·Φ”«βΩ……ζ≥…““ΜυΜΖΦΚΆι
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥ΙΛ“ΒΖœΥ°Κ§”–![]() ΚΆ
ΚΆ![]() Β»άκΉ”Θ§–ηΨ≠ΈέΥ°¥Πάμ¥ο±ξΚσ≤≈Ρή≈≈Ζ≈Θ§ΈέΥ°¥ΠάμΡβ”Ο»γΆΦΝς≥ΧΫχ––¥ΠάμΘΚ
Β»άκΉ”Θ§–ηΨ≠ΈέΥ°¥Πάμ¥ο±ξΚσ≤≈Ρή≈≈Ζ≈Θ§ΈέΥ°¥ΠάμΡβ”Ο»γΆΦΝς≥ΧΫχ––¥ΠάμΘΚ
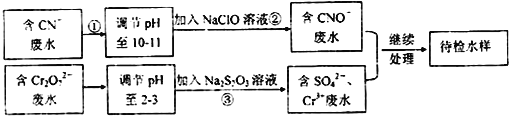
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
![]() ≤Ϋ÷η
≤Ϋ÷η![]() ÷–Θ§
÷–Θ§![]() ±Μ
±Μ![]() ―θΜ·ΈΣ
―θΜ·ΈΣ![]() ΒΡάκΉ”ΖΫ≥Χ ΫΈΣ ______ Θ°
ΒΡάκΉ”ΖΫ≥Χ ΫΈΣ ______ Θ°
![]() ≤Ϋ÷η
≤Ϋ÷η![]() ΒΡΖ¥”ΠΖΫ≥Χ ΫΈΣ
ΒΡΖ¥”ΠΖΫ≥Χ ΫΈΣ![]() Έ¥≈δΤΫ
Έ¥≈δΤΫ![]() Θ§‘ρΟΩœϊΚΡ
Θ§‘ρΟΩœϊΚΡ![]()
![]() Θ§Ζ¥”Π÷–
Θ§Ζ¥”Π÷–![]() ß»Ξ
ß»Ξ![]() ______ mo1Θ°
______ mo1Θ°
![]() Κ§
Κ§![]() ΖœΥ°Ω…“‘Φ”»κ λ ·Μ“Ϋχ“Μ≤Ϋ¥ΠάμΘ§ΡΩΒΡ « ______ Θ°
ΖœΥ°Ω…“‘Φ”»κ λ ·Μ“Ϋχ“Μ≤Ϋ¥ΠάμΘ§ΡΩΒΡ « ______ Θ°
![]() ‘Ύ
‘Ύ![]() œ¬Θ§ΫΪa
œ¬Θ§ΫΪa![]() ΒΡNaCN»ή“Κ”κ
ΒΡNaCN»ή“Κ”κ![]() ΒΡ―ΈΥαΒ»ΧεΜΐΜλΚœΘ§Ζ¥”ΠΚσ≤βΒΟ»ή“Κ
ΒΡ―ΈΥαΒ»ΧεΜΐΜλΚœΘ§Ζ¥”ΠΚσ≤βΒΟ»ή“Κ![]() Θ§”ΟΚ§aΒΡ¥ζ ΐ Ϋ±μ Ψ
Θ§”ΟΚ§aΒΡ¥ζ ΐ Ϋ±μ Ψ![]() ΒΡΥ°Ϋβ≥Θ ΐ
ΒΡΥ°Ϋβ≥Θ ΐ![]() ______
______ ![]() »τ
»τ![]() ±ΫΪ≈®Ε»ΨυΈΣ
±ΫΪ≈®Ε»ΨυΈΣ![]() ΒΡNaCNΓΔHCN»ή“ΚΒ»ΧεΜΐΜλΚœΚσΘ§»ή“Κ≥ Φν–‘Θ§‘ρΙΊ”ΎΗΟ»ή“ΚΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ « ______
ΒΡNaCNΓΔHCN»ή“ΚΒ»ΧεΜΐΜλΚœΚσΘ§»ή“Κ≥ Φν–‘Θ§‘ρΙΊ”ΎΗΟ»ή“ΚΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ « ______ ![]() ΧνΉ÷ΡΗ
ΧνΉ÷ΡΗ![]() Θ°
Θ°
![]() ¥Υ»ή“Κ“ΜΕ®”–
¥Υ»ή“Κ“ΜΕ®”–![]()
![]() ¥Υ»ή“Κ“ΜΕ®”–
¥Υ»ή“Κ“ΜΕ®”–![]()
C ΜλΚœ»ή“Κ÷–Υ°ΒΡΒγάκ≥ΧΕ»“ΜΕ®¥σ”ΎΗΟΈ¬Ε»œ¬¥ΩΥ°ΒΡΒγάκ≥ΧΕ»
![]() ¥Υ»ή“ΚΦ”»κ…ΌΝΩ«β―θΜ·ΡΤΜρ―ΈΥαΘ§»ή“ΚΒΡpH±δΜ·≤Μ¥σ
¥Υ»ή“ΚΦ”»κ…ΌΝΩ«β―θΜ·ΡΤΜρ―ΈΥαΘ§»ή“ΚΒΡpH±δΜ·≤Μ¥σ
![]() άϊ”Ο
άϊ”Ο![]() Ά®Ιΐœ¬Ν–ΖΫΖ®≤βΕ®Ρ≥ΈΐΖέΒΡ¥ΩΕ»
Ά®Ιΐœ¬Ν–ΖΫΖ®≤βΕ®Ρ≥ΈΐΖέΒΡ¥ΩΕ»![]() ‘”÷ ≤Μ≤Έ”κΖ¥”Π
‘”÷ ≤Μ≤Έ”κΖ¥”Π![]() ΘΚ»ΓagΈΐΖέ»ή”Ύ―ΈΥα÷–Θ§œρ…ζ≥…ΒΡ
ΘΚ»ΓagΈΐΖέ»ή”Ύ―ΈΥα÷–Θ§œρ…ζ≥…ΒΡ![]() ÷–Φ”»κΙΐΝΩΒΡ
÷–Φ”»κΙΐΝΩΒΡ![]() »ή“ΚΘ§”Οb
»ή“ΚΘ§”Οb![]()
![]() ΒΈΕ®…ζ≥…ΒΡ
ΒΈΕ®…ζ≥…ΒΡ![]() “―÷ΣΥα–‘ΜΖΨ≥œ¬Θ§
“―÷ΣΥα–‘ΜΖΨ≥œ¬Θ§![]() Ω…±ΜΜΙ‘≠ΈΣ
Ω…±ΜΜΙ‘≠ΈΣ![]() Θ§Ι≤”Ο»Ξ
Θ§Ι≤”Ο»Ξ![]() »ή“Κm
»ή“Κm![]() ‘ρΈΐΖέ÷–ΈΐΒΡ÷ ΝΩΖ÷ ΐ « ______
‘ρΈΐΖέ÷–ΈΐΒΡ÷ ΝΩΖ÷ ΐ « ______ ![]() ΒΡΡΠΕϊ÷ ΝΩΈΣM
ΒΡΡΠΕϊ÷ ΝΩΈΣM![]() Θ§”ΟΚ§aΓΔbΓΔmΓΔMΒΡ¥ζ ΐ Ϋ±μ Ψ
Θ§”ΟΚ§aΓΔbΓΔmΓΔMΒΡ¥ζ ΐ Ϋ±μ Ψ![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ≥ΘΈ¬≥Θ―Ιœ¬Θ§»Γœ¬Ν–Β»÷ ΝΩ4÷÷ΤχΧ§ΧΰΖ÷±π‘ΎΉψΝΩΒΡ―θΤχ÷–»Φ…’Τδ÷–œϊΚΡ―θΤχΉνΕύΒΡ «(ΓΓ)
A.CH4B.C2H6C.C3H8D.C4H10
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A.ΔΌ2NO2![]() N2O4 ΔΎN2O4
N2O4 ΔΎN2O4![]() 2NO2Θ§Ζ¥”ΠΔΌΒΡΜ·―ßΤΫΚβ≥Θ ΐ «Ζ¥”ΠΔΎΒΡΜ·―ßΤΫΚβ≥Θ ΐΒΡΒΙ ΐ
2NO2Θ§Ζ¥”ΠΔΌΒΡΜ·―ßΤΫΚβ≥Θ ΐ «Ζ¥”ΠΔΎΒΡΜ·―ßΤΫΚβ≥Θ ΐΒΡΒΙ ΐ
B.“―÷ΣH+(aq)+OH-(aq)=H2O(l) ΓςH=-57.3kJ/molΘ§ΫΪ0.05mol/LBa(OH)2»ή“Κ100.0mL”κ0.05mol/LH2SO4»ή“Κ100.0mLΜλΚœΘ§‘Ύ298KΓΔ101kPaΧθΦΰœ¬Ζ≈»»ΝΩΈΣ0.573kJ
C.“―÷Σ298K ±Θ§0.10mol/L HAcΒΡΒγάκΕ»ΈΣ1.32%ΓΘ‘Ύ0.10mol/L HAcΚΆ0.10mol/LNaAcΒΡΜλΚœ»ή“Κ20.00mL÷–Θ§”–»γœ¬±δΜ·ΘΚΔΌHAc![]() H++Ac-Θ§ΔΎNaAc=Na++Ac-Θ§ΔέAc-+H2O
H++Ac-Θ§ΔΎNaAc=Na++Ac-Θ§ΔέAc-+H2O![]() HAc+OH-Θ§œρΗΟ»ή“Κ÷–ΒΈ»κΦΗΒΈœΓ―ΈΥαΘ§»ή“ΚΒΡpH±Θ≥÷œύΕ‘Έ»Ε®
HAc+OH-Θ§œρΗΟ»ή“Κ÷–ΒΈ»κΦΗΒΈœΓ―ΈΥαΘ§»ή“ΚΒΡpH±Θ≥÷œύΕ‘Έ»Ε®
D.ΫΪΟςΖ·”κ¥ΩΦν»ή“ΚΜλΚœΘ§”–≥ΝΒμ≤ζ…ζΘ§ΗΟ≥ΝΒμΒΡ≥…Ζ÷ΈΣΧΦΥα¬Ν
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ιΐ≥ΧΜρœ÷œσ”κ―ΈάύΥ°ΫβΈόΙΊΒΡ «(ΓΓΓΓ)
A. ¥ΩΦν»ή“Κ»Ξ”ΆΈέ B. Φ”»»¬»Μ·Χζ»ή“Κ―’…Ϊ±δ…ν
C. Χζ‘Ύ≥± ΣΒΡΜΖΨ≥÷–…ζ–β D. ≈®ΝρΜ·ΡΤ»ή“Κ”–≥τΈΕ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ηςœν±μ ω”κ Ψ“βΆΦ“Μ÷¬ΒΡ «ΘΚ

AΘ°ΆΦΔΌ÷–aΓΔb«ζœΏΖ÷±π±μ ΨΖ¥”ΠCH2=CH2(g)ΘΪH2(g) Γζ CH3CH3(g)ΠΛHΘΦ0ΘΜ Ι”ΟΚΆΈ¥ Ι”Ο¥ΏΜ·ΦΝ ±Θ§Ζ¥”ΠΙΐ≥Χ÷–ΒΡΡήΝΩ±δΜ·
BΘ°ΆΦΔΎ±μ Ψ25 Γφ ±Θ§”Ο0Θ°01 molΓΛLΘ≠1―ΈΥαΒΈΕ®“ΜΕ®ΧεΜΐΒΡ0Θ°01 molΓΛLΘ≠1 NaOH»ή“ΚΘ§»ή“ΚΒΡpHΥφΦ”»κΥαΧεΜΐΒΡ±δΜ·
CΘ°ΆΦΔέ±μ ΨCH4(g)ΘΪH2O(g) ![]() CO(g)ΘΪ3H2(g)ΠΛHΘ§Ζ¥”ΠCH4ΒΡΉΣΜ·¬ ”κΈ¬Ε»ΓΔ―Ι«ΩΒΡΙΊœΒΘ§«“p1ΘΨp2,ΠΛHΘΦ0
CO(g)ΘΪ3H2(g)ΠΛHΘ§Ζ¥”ΠCH4ΒΡΉΣΜ·¬ ”κΈ¬Ε»ΓΔ―Ι«ΩΒΡΙΊœΒΘ§«“p1ΘΨp2,ΠΛHΘΦ0
DΘ°ΆΦΔή ÷–«ζœΏ±μ ΨΖ¥”Π2SO2(g)ΘΪO2(g) ![]() 2SO3(g) ΠΛH ΘΦ0ΘΜ’ΐΓΔΡφΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΥφΈ¬Ε»ΒΡ±δΜ·
2SO3(g) ΠΛH ΘΦ0ΘΜ’ΐΓΔΡφΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΥφΈ¬Ε»ΒΡ±δΜ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com