
【题目】下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+
2CrO42-(黄色)+ 2H+
序号 | a | b | 现象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴饱和Na2SO3溶液(pH = 9) | 溶液变绿色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴饱和Na2SO3溶液 | 溶液没有明显变化 | |
3 | 2 mL饱和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变黄色 | |
4 | 2 mL蒸馏水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变成浅橙色 |
下列说法不正确的是
A. 实验1中的绿色溶液中含有SO42-
B. 实验1、2的a溶液中所含的离子种类相同
C. 向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色
D. 实验4的目的是排除稀释对溶液颜色变化造成的影响
【答案】C
【解析】
由4个实验结果对比可知,K2Cr2O7与Na2SO3在酸性条件下发生氧化还原反应,在碱性条件下不发生氧化还原反应;由平衡Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+可知,溶液的碱性增强,平衡正向移动,以此分析。
2CrO42-(黄色)+ 2H+可知,溶液的碱性增强,平衡正向移动,以此分析。
A. 实验1中K2Cr2O7与Na2SO3发生了氧化还原反应,Na2SO3被氧化为Na2SO4,K2Cr2O7被还原为Cr3+,溶液呈绿色,故A正确;
B. 实验1、2中的a溶液中都存在平衡:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+,故溶液中所含的离子种类相同,故B正确;
2CrO42-(黄色)+ 2H+,故溶液中所含的离子种类相同,故B正确;
C.Na2SO3溶液呈碱性,滴加3滴0.05 mol·L1 K2Cr2O7溶液,平衡Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+向正向移动,溶液呈黄色;若向实验3溶液中继续滴加过量硫酸,则在酸性条件下,K2Cr2O7与Na2SO3发生氧化还原反应,溶液变绿色,故C错误;
2CrO42-(黄色)+ 2H+向正向移动,溶液呈黄色;若向实验3溶液中继续滴加过量硫酸,则在酸性条件下,K2Cr2O7与Na2SO3发生氧化还原反应,溶液变绿色,故C错误;
D. 实验4和实验3相比,b溶液相同,a为等体积的蒸馏水,溶液由黄色变成浅橙色,颜色反而加深,故可排除稀释对溶液颜色变化造成的影响,故D正确。
故选C。


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.邻二甲苯只有一种结构,能证明苯环中不存在碳碳单键和碳碳双键交替的结构
B.高聚物![]() 的单体可以通过乙烯和HCl加成制得
的单体可以通过乙烯和HCl加成制得
C.(CH3)2CH﹣CH=CH﹣C(CH3)3与氢气加成后的产物用系统命名法命名为2,2,5﹣三甲基己烷
D.完全燃烧一定质量的冰醋酸、葡萄糖混合物(以任意质量比混合),生成CO2和H2O的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,铅蓄电池在放电过程中,负极质量增加,正极质量也增加
B.金属铝的冶炼流程为: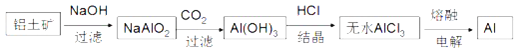
C.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D.一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器里,发生反应2A(g)+B(g)![]() 2C(g)。下列条件不能说明该反应达到平衡的是
2C(g)。下列条件不能说明该反应达到平衡的是
A.2υ正(B)=υ逆(C)
B.该体系的密度不随时间而变化
C.该体系的温度不随时间而变化
D.1molA的化学键断裂,同时1molC的化学键也断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对在密闭容器中进行的可逆反应:4NH3(g)+5O2![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3)∶n(O2)=1∶1
B.反应达到平衡后,再向体系中充入O2,将提高NH3的转化率
C.反应达到平衡时,若向体系中充入稀有气体,速率增大
D.当v正(NH3):v正(NO)=1∶1时,说明该化学反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式书写或离子共存说法正确的是( )
A.在0.1molL-1 Na2CO3溶液中:Al3+、NH4+、SO42-、NO3-一定能大量共存
B.常温下,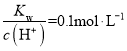 的溶液中,下列离子一定能大量共存:K+、Cl-、NO3-、Fe2+
的溶液中,下列离子一定能大量共存:K+、Cl-、NO3-、Fe2+
C.清洗锅炉时先用纯碱溶液浸泡的主要原因:CaSO4(s) + CO32-(aq)![]() CaCO3(s) + SO42-(aq)
CaCO3(s) + SO42-(aq)
D.向Al2(SO4)3溶液中加入少量Ba(OH)2溶液:Ba2+ + Al3+ + SO42- + OH- = BaSO4↓+ Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=﹣Q1kJmol﹣1
2H2(g)+O2(g)=2H2O(g)ΔH=﹣Q2kJmol﹣1,
2H2(g)+O2(g)=2H2O(l) ΔH2=﹣Q3kJmol﹣1
常温下,取体积比2∶3的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
A.0.4Q1+0.15Q2B.0.2Q1+0.05Q2C.0.2Q1+0.15Q3D.0.2Q1+0.3Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W的原子序数依次增大,四种元素形成的单质依次为m、n、p、q;r、t、u 是这些元素组成的二元化合物,其中u为葡萄酒中的抑菌成分;25 ℃,0.01 mol/L的v溶液中:  = 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是
= 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是

A. 简单离子半径:W>Y>Z>X
B. W,Y分別与X元素形成的简单化合物的沸点: Y> W
C. Z2Y和ZX都只存在离子键
D. v能抑制水的电离,u能促进水的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com