
【题目】某化学小组为探究草酸的性质并制备草酸钠及其用途,查阅到如下信息:

探究草酸部分性质并制备草酸钠的生产流程如下:
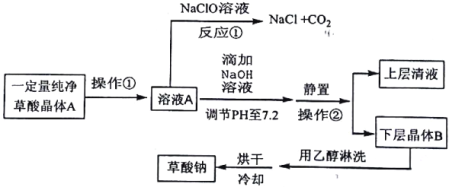
请回答下列问题:
(1)写出反应①的化学方程式__________。表明草酸具有__________性。
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是__________。该反应达到终点时的化学方程式为__________。
(3)操作②的名称是__________。用乙醇淋洗晶体B的目的是__________
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会__________:操作中需用__________滴定管(填“酸式”或“碱式”),当达到反应终点时的现象是__________;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为__________mol/L。
【答案】(1)H2C2O4+NaC1O=NaC1+2CO2↑+H2O;还原
(2)利用中和反应放热,升温促进反应(或增大反应速率);H2C2O4+2NaOH=Na2C2O4↓+2H2O
(3)过滤;除去晶体表面水分减少损失
(4)草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率;酸式滴定管;溶液呈现浅紫色且30s内不褪色;0.0200mol/L
【解析】
试题分析:(1)反应①是次氯酸钠将草酸氧化的过程,反应的化学方程式为H2C2O4+NaC1O=NaC1+2CO2↑+H2O,表明草酸具有还原性,故答案为:H2C2O4+NaC1O=NaC1+2CO2↑+H2O;还原
(2)向溶液A中加入NaOH溶液,发生中和反应,开始滴加速度要尽量快些,可以利用中和反应放热,升温促进反应(或增大反应速率),生成的草酸钠微溶于水,反应达到终点时的化学方程式为H2C2O4+2NaOH=Na2C2O4↓+2H2O,故答案为:利用中和反应放热,升温促进反应(或增大反应速率);H2C2O4+2NaOH=Na2C2O4↓+2H2O
(3) 生成的草酸钠微溶于水,形成沉淀,操作②为过滤。用乙醇淋洗晶体B可以除去晶体表面水分,同时防止洗涤时草酸钠的损失,故答案为:过滤;除去晶体表面水分减少损失
(4)用高锰酸钾溶液滴定草酸钠溶液时发生反应5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率;高锰酸钾溶液检验腐蚀性,能够腐蚀乳胶管,操作中应选用酸式滴定管,当达到反应终点时溶液呈现浅紫色且30s内不褪色;n(Na2C2O4)=![]() n(MnO4-)=
n(MnO4-)=![]() ×0.01000mol/L×0.0200L=0.0005mol,c(Na2C2O4)=
×0.01000mol/L×0.0200L=0.0005mol,c(Na2C2O4)=![]() = 0.0200mol/L,故答案为:草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率;酸式滴定管;溶液呈现浅紫色且30s内不褪色;0.0200mol/L。
= 0.0200mol/L,故答案为:草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率;酸式滴定管;溶液呈现浅紫色且30s内不褪色;0.0200mol/L。


科目:高中化学 来源: 题型:
【题目】DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3)。名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂。DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因。因此从70年代后滴滴涕逐渐被世界各国明令禁止生产和使用。其结构为: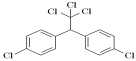 ,下列有关说法正确的是 ( )
,下列有关说法正确的是 ( )
(手性碳原子为饱和碳原子所连的4个原子或原子团不同)
A.属于烃类 B.DDT完全燃烧后只产生CO2和H2O两种物质
C.分子无手性碳 D.氢核磁共振谱图中有5种位置峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验Ⅰ. 制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。现利用下图所示装置进行实验。
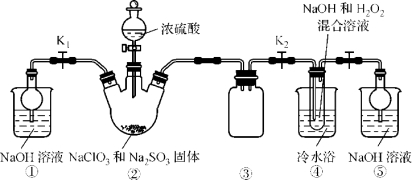
(1)装置③的作用是 。
(2)装置②中产生ClO2的化学方程式为 ;装置④中制备NaClO2的化学方程式为 。
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤如下:
①减压,55 ℃蒸发结晶;②趁热过滤;③ ;④低于60 ℃干燥,得到成品。
实验Ⅱ. 测定某亚氯酸钠样品的纯度
设计如下实验方案,并进行实验:
①确称取所得亚氯酸钠样品m g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-);将所得混合液配成250 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
(4)达到滴定终点时的现象为 。
(5)该样品中NaClO2的质量分数为 (用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质:

(1)实验室制备乙炔的化学方程式是_______________________________;
(2)实验过程中,为减缓生成乙炔的速率,通常采取的措施是:___________________________________________________________;
(3)B中试剂是 ;
(4)若C中试剂是溴水,可以观察到的现象是_________________。
Ⅱ.利用上述装置还可以验证醋酸、苯酚、碳酸的酸性强弱。
(1)A中固体试剂是 (选填序号);
A.醋酸钠 B.碳酸氢钠 C.苯酚钠
(2)C中反应的化学方程式是____________________________________;
(3)有同学认为没有B装置,也可以验证酸性的强弱,你认为合理吗?
_____(填“合理”或“不合理”);若不合理,原因是:
______________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期元素X形成的单质A与NaOH溶液反应,有如下转化关系![]() ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。
(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为 ;
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为 ;
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟
用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下:
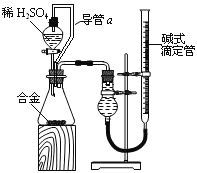
①装置中导管a的作用是平衡分液漏斗上下管口的压强,有利于液体滴下和 ;
②实验中准确测得4个数据:实验前该合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL;则通常状况时气体摩尔体积Vm=_____L·moL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生:一段时间后,断开K1,闭合K2,发现电流表A指针偏转。下列有关描述正确的是( )
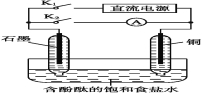
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl-![]() Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-![]() 2Cl-
2Cl-
D.断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为____ ,基态Cu3+的核外电子排布式为_ _______。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A.V2O5 | B.CrO2 | C.PbO | D.ZnO |
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;碳原子的杂化方式有____ 。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为 。
②H2O的VSEPR模型为 ,比较键角的大小:H2O CH4(填“>”“<”或“=”),原因为 。
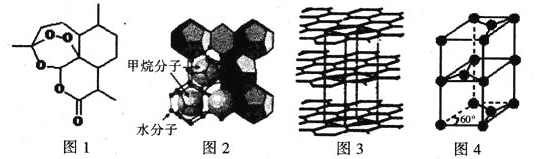
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为 g·cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途。

(1)写出Se的基态原子的外围电子排布式 。
(2)酒石酸钛配合物广泛应用于药物合成。酒石酸(结构如下图所示)中羧基氧原子的轨道杂化类型分别是 ,1 mol酒石酸中π键的数目是 。
(3)TiCl4熔点是—25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于 晶体;
NO3-离子的空间构型为 。
(4)主族元素A和钛同周期,具有相同的最外层电子数,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键。元素A、元素B和钛三者形成的晶体的晶胞如图所示,写出该晶体的化学式 (用元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】
X、Y、Z、R为前四周期原子序数依次增大的元素。X的单质与氢气可化合生成气体G.,其水溶液pH>7;Y的原子中最外层电子数是内层电子数的3倍;Z的单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。
请回答下列问题:
(1)Z元素在周期表中的位置________________;其单质的晶体类型是________________;X和Y元素的第一电离能较小的是___________(填元素名称);
(2)在Y、 Z的简单氢化物中,Y的氢化物更易溶于乙醇,其原因是_____________;G在一定条件下可与CO2反应生成一种最常见的氮肥M,M中所含元素原子的杂化方式为_____________;
(3) R单质与Z单质化合的产物J中,R离子的核外电子排布式是_____________;己知J与足量强碱性的NaC1O溶液在一定条件下反应,生成一种具有强氧化性的R的含氧酸根,该反应的离子方程式为_____________;
(4) G分子的立体构型为_______;R可形成化合物R(CO)5,该化合物中所含化学键的类型为_______;
(5) X与硼元素形成的化合物BX,其晶胞结构如图所示,该晶胞中含有的X原子数目为_____________;若最近的X、B原子之间的距离为anm,NA代表阿伏加德罗常数,则该晶体的密度为_____________g/cm
3(列式表示,不必化简)。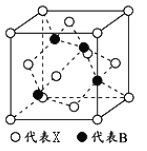
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com