
【题目】I.亚硫酸钠的氧化反应:2Na2SO3 (aq) +O2(aq)=2Na2SO4(aq) H=x kJ/mol。其反应速率受溶解氧浓度影响,分为富氧区和贫氧区两个阶段。
(1)已知O2(g) ![]() O2(aq) H=y kJ/mol,Na2SO3 溶液与O2(g)反应的热化学方程式为___________________。
O2(aq) H=y kJ/mol,Na2SO3 溶液与O2(g)反应的热化学方程式为___________________。
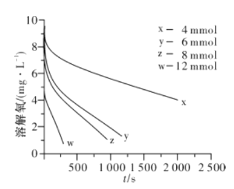
(2)291.5 K时,1.0 L溶液中Na2SO3初始量分别为4、6、8、12 mmol,溶解氧浓度初始值为9.60 mg/L,每5 s记录溶解氧浓度,实验结果如图所示。当Na2SO3初始量为12 mmol,经过20 s溶解氧浓度降为6.40 mg/L,则0~20s内Na2SO3的平均反应速率为_______mol/(L·s)。
(3)为确定贫氧区速率方程v=k·ca(SO32-)·cb(O2)中的a、b的值(取整数),分析实验数据。
c(Na2SO3)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
v×106 | 10.2 | 24.4 | 44.7 | 103.6 |
①当溶解氧浓度为4.0 mg/L时,c(SO32-)与速率数值关系如表(甲)所示,则a=____。
②当溶解氧浓度小于4.0mg/L时,图中曲线皆为直线,Na2SO3氧化速率与溶解氧浓度无关,则b=_______。
(4)两个阶段不同温度的速率常数之比如表(乙)所示。已知![]() ,R为常数。Ea(富氧区)_____ (填“>”或“<”)Ea(贫氧区)。
,R为常数。Ea(富氧区)_____ (填“>”或“<”)Ea(贫氧区)。
反应阶段 | 速率方程 |
|
富氧区 | v=k·c (SO32-)·c (O2) | 1.47 |
贫氧区 | v=k·ca (SO32-)·cb(O2) | 2.59 |
II. (5)在容积固定的密闭容器中,起始充入0.2 mol SO2和0.1 mol O2,反应体系起始总压强0.1MPa。反应在一定温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=________ ( 分压=总压×物质的量分数)(写单位)。
(6)利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极反应式_________________________。
【答案】2Na2SO3(aq) +O2(g)=2Na2SO4(aq) H=(x+y)kJ/mol 1×10-5 2 0 < 24300MPa-1 ![]()
【解析】
(1) 2Na2SO3(aq) +O2 (aq)=2Na2SO4(aq) H=x kJ/mol ①;
O2(g) ![]() O2(aq) H=y kJ/mol②;
O2(aq) H=y kJ/mol②;
将方程式①+②得2Na2SO3 (aq) +O2 (g)=2Na2SO4(aq) H=(x+y)kJ/mol;
(2) 0~20s内溶解氧浓度变化量=(9.60-6.40)mg/L=3.20mg/L=3.20×10-3g/L,则△c(O2)=![]() =10-4mol/L,根据方程式得△c(Na2SO3)=2△c(O2)=2×10-4mol/L,0~20s内Na2SO3的平均反应速率v=
=10-4mol/L,根据方程式得△c(Na2SO3)=2△c(O2)=2×10-4mol/L,0~20s内Na2SO3的平均反应速率v=![]() =1×10-5molL-1s-1;
=1×10-5molL-1s-1;
(3)①当溶解氧浓度为4.0 mg/L时,c(SO32-)与速率数值关系如表(甲)所示,v1:v2=c1a(SO32-):c2a(SO32-),![]() ,解得a=2;
,解得a=2;
②当溶解氧浓度小于4.0mgL-1时,图中曲线皆为直线,说明该方程为一次函数,k为常数,v与c(SO32-)有关,溶解氧浓度对v无影响,所以b=0;
(4) ln![]() 随着Ea的增大而增大,富氧区的ln
随着Ea的增大而增大,富氧区的ln![]() 较小,故Ea(富氧区)<Ea(贫氧区);
较小,故Ea(富氧区)<Ea(贫氧区);
(5)
设平衡时的总压强P,![]() ,P=0.07 MPa,Kp=
,P=0.07 MPa,Kp=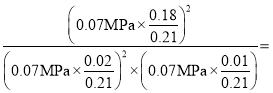 24300MPa-1;
24300MPa-1;
(6)SO2和O2来制备硫酸,硫元素化合价升高,负极为SO2失电子生成硫酸根离子,反应的离子方程式是![]() 。
。


科目:高中化学 来源: 题型:
【题目】室温下,H2C2O4的电离平衡常数Ka1= 5.9 ×10 -2,K a2= 6.4 ×10 -5,用0.100 0 molL-1 NaOH溶液滴定20.00 mL 0.100 0 molL-1H2C2O 4溶液的曲线如图所示(体积变化忽略不计)。下列说法正确的是
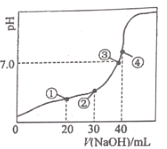
A.滴定过程中,当 pH=4 时,存在:c(H+)+c(Na+ )=c(OH- )+c(![]() )+c(
)+c(![]() )
)
B.点①、③、④所示溶液中,点③所示溶液水的电离程度最大
C.点③所示溶液:3c(![]() )+2c(
)+2c(![]() )+c(H2C2O4)=0.l molL-1
)+c(H2C2O4)=0.l molL-1
D.滴定过程中可能出现:c(Na+)>c(![]() )= c(
)= c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6 ;E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能________B(填“<”“>”或“=”),A、B、C三种元素电负性由小到大的顺序为________(用元素符号表示)。
(2)D元素原子的价电子排布式是________。
(3)C元素的电子排布图为________________;E3+的离子符号为________________。
(4)F元素位于元素周期表的________区,其基态原子的电子排布式为________________。
(5)G元素可能的性质________。
A.其单质可作为半导体材料
B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于水解应用的说法,错误的是
A.草木灰(主要含K2CO3)与铵态氮肥最好不混用
B.明矾用于净水
C.向CuCl2溶液中加入Cu(OH)2,调节pH可除去溶液中混有的少量Fe3+
D.将AlCl3、Al2(SO4)3溶液分别加热、蒸发、浓缩、结晶、灼烧,所得固体成分相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
B.常温下,1L pH=10的氨水溶液中,发生电离的水分子数为1×10-10NA
C.电解精炼铜时,阴极增重3.2g,电路中转移电子数为0.05NA
D.将0.1mol O2与0.2mol NO在密闭容器中充分反应,反应后容器内分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(2 Na2CO3·3 H2O2)广泛用于化工、造纸、纺织、食品等行业,一种以芒硝(Na2SO4·10 H2 O)、H2O2等为原料制备过碳酸钠的工艺流程如下:
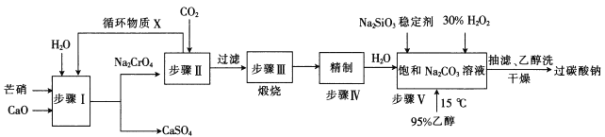
已知2CrO42-+2H+=Cr2O72-+H2O , pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。
回答下列问题:
(1)Na2CrO4中Cr元素的化合价为___
(2)Ksp(CaCrO4)___(填“>”或“<”)Ksp(CaSO4)。
(3)流程中循环物质X为___(填化学式)。
(4)步骤II中发生反应的化学方程式为_________
(5)步骤I一III是为了制得纯碱,从环境保护的角度看,可能的不足之处是___
(6)步骤V合成时,加入95%的乙醇的目的是___
(7)测定产品活性氧的实验步骤如下:准确称取mg产品,用硫酸溶解后,用c mol·L-1的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V mL。
①滴定到终点时,溶液呈___(填“无色”或“浅红色”)。
②过氧化物的活性氧是指过氧化物单独用催化剂催化分解时放出氧气的质量与样品的质量之比。该实验测得的产品中活性氧为___(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于一定条件下的化学平衡H2(g)+I2(g)![]() 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
A.恒温恒容,充入H2,v(正)增大,平衡右移
B.恒温恒容,充入He,v(正)增大,平衡右移
C.加压,v(正),v(逆)不变,平衡不移动
D.升温,v(正)减小,v(逆)增大,平衡左移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1mol·L-1的KMnO4溶液:Na+、Cl-、SO32-
B.使紫色石蕊试液显蓝色的溶液:K+、AlO2-、NO3-
C.0.1mol·L-1FeCl3溶液:NH4+、SCN-、SO42-
D.![]() =1×1012的溶液:Na+、SO42-、HCO3-
=1×1012的溶液:Na+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用SiHCl3在加热条件下与过量H2反应制备纯硅的装置如图(热源及夹持装置略去):
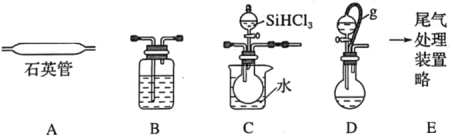
已知:SiHCl3沸点为33℃,能与和H2O强烈反应,在空气中易自燃;
请问答:
(1)依次连接的合理顺序为__。
(2)操作时应先打开装置__(选填“C”或“D”)中分液漏斗的旋塞,理由是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com