
【题目】下列反应的反应热△H>0的是( )
A. 铝与稀硫酸反应 B. 加热氧化银冶炼银
C. 醋酸与氨水反应 D. 液化石油气燃烧
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】复分解反应是中学化学中常见的一种反应类型。复分解反应中,元素的化合价都没发生变化,都不属氧化还原反应。
(1)复分解反应存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐。已知相同物质的量浓度的溶液,pH大小关系是pH(Na2CO3)>pH(NaClO)>pH(NaHCO3)>pH(NaHS O3)。
①写出向NaClO溶液中通入少量CO2的化学方程式______________________。
②将混有CO2气体的SO2气体,通入NaHSO3饱和溶液,___________(填“能”或“不能”)除去CO2气体。
(2)复分解反应从形式上看,是一种相互交换成分的反应,在有机反应中,也存在类似形式的反应——“烯烃的复分解”反应。

如果用重氢(D)标记过的烯烃CD3CD![]() CDCD3和烃CH3CH
CDCD3和烃CH3CH![]() CHCH3进行反应,其化学方程式是______________________。
CHCH3进行反应,其化学方程式是______________________。
(3)复分解反应的发生还遵循向生成沉淀、气体、难电离物质的方向进行。
①甲同学认为CuSO4+H2S![]() H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
②乙同学认为,BaSO3可溶于酸,SO2通入Ba(NO3)2溶液中不发生化学反应,但经过实验探究发现,有白色沉淀生成,请你写出相关反应的离子方程式_____________。
(4)电解是一种在通电作用下的氧化还原反应。用电解法可将某工业废水中的CN-转变为N2,装置如上图所示。电解过程中,阴极区电解质溶液的pH将_____________(填“增大”“减小”或“不变”)。阳极的电极反应式为______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属或氧化物可以完全溶解的是
A、1molZn与含1molHCl的稀盐酸共热
B、1molCu与含2molH2SO4的浓硫酸共热
C、1molCu与含4molHNO3的浓硝酸
D、1molMnO2与含4molHCl的浓盐酸共热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用,实验小组进行碘单质的制备。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。

(1)将海带灼烧成灰后再用水浸取,目的是_______________。
(2)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填编号),反应中I-转化为I2 的离子反应方程式为_______________。
(3)步骤C中使用的起到分离作用的仪器是_____________,使用该仪器时,第一步操作是_______________。
(4)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是_______________。
【碘的分离】得到含I2的CCl4溶液后,利用右图装置进行碘的提取并回收溶剂。

(5)图中有两处明显错误,分别是①_________;②_________。
(6)对实验装置的错误改正之后进行分离操作。预期锥形瓶中得到无色的CCl4,实验结果锥形瓶中得到紫红色液体,请分析出现该实验结果的原因____________,为了保证实验成功,请提出改进方案:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读明代爱国诗人于谦的诗《石灰吟》,回答问题: 千锤万凿出深山,烈火焚烧若等闲.粉身碎骨浑不怕,要留清白在人间
(1)整首诗蕴含着石灰的来源、生产、性质、用途等多种化学事实,诗中所描述的变化共涉及到下列物质:①石灰石(主要成分CaCO3)②CaO③CO2④H2O⑤Ca(OH)2悬浊液⑥CaCO3 , 其中属于电解质的是(填序号)
(2)下列工业生产中一般不用石灰石作为原料的是(填序号) ①用海水为原料生产镁 ②制硅酸盐水泥 ③制普通玻璃 ④制漂白粉⑤制陶瓷
(3)零食包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰,生石灰属于氧化物(填“酸性”或“碱性”),用方程式说明你的理由 .
(4)某兴趣小组同学对碳酸钙的制备进行了以下探究,该组同学使用大理石(含少量的Fe2O3杂质)等物质制备碳酸钙的实验流程如图: 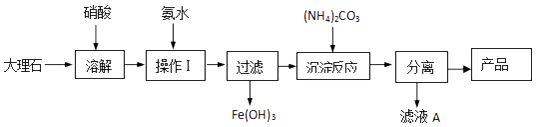 溶解大理石时,用硝酸而不用硫酸的原因是 , “滤液A”中除H+离子外,还含有的阳离子是;检验该阳离予的实验操作是 .
溶解大理石时,用硝酸而不用硫酸的原因是 , “滤液A”中除H+离子外,还含有的阳离子是;检验该阳离予的实验操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在 5L 的密闭容器中发生如下反应:N2 (g)+3H2 (g)2NH3(g),起初充入的 3.0mol N2 和 6.0mol H2 , 5 分钟后达到平衡,此时容器内压强是开始时的 ![]() ,问:
,问:
(1)氢气的平衡转化率为;
(2)用氨气表示 5min 内的反应速率为
(3)若要使氮气和氢气的平衡转化率相等,起始投料要求 n(H2 ):n(N2 )为
(4)以下措施能加快反应速率的是
A.缩小体积,使压强增大
B.恒温恒容充入 He 使压强增大
C.恒温恒压充入 He
D.平衡后加入催化剂
(5)如果利用此反应设计成原电池,并用稀硫酸做电解液,分别写出正、负极的电极反应 式:、 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com