
【题目】固体A的化学式为NH5 , 它的所有原子的最外层都符合相应稀有气体的最外电子层结构,则下列有关说法不正确的是( )
A.NH5中既有共价键又有离子键
B.NH5的电子式为 ![]()
C.1 mol NH5中含有5NA个N﹣H键(NA表示阿伏加德罗常数)
D.它与水反应的离子方程式为NH4++H﹣+H2O═NH3H2O+H2↑
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。请回答下列问题:
(1)Ti的基态原子价电子排布式为______。
(2)纳米TiO2常用作下述反应的催化剂。

化合物甲的分子中采取sp2方式杂化的碳原子有_____个,化合物乙中采取sp3方式杂化的原子对应元素的电负性由大到小的顺序为_____。
(3)某含Ti3+配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配合物离子中含有的化学键类型是_____,1 mol该配合物中含有的σ键数目是_____。
(4)通过x-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且知三种离子晶体的晶格能数据如下:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3401 |
KCl、MgO、CaO、TiN四种离子晶体熔点由高到低的顺序为_____。
(5)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a=0.469 nm,c=0.295 nm,则该钛晶体的密度为______g·cm-3(用NA 表示阿伏加德罗常数的值,列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用,反应条件(温度或者反应物用量)改变,不会引起产物种类改变的是
A. Na和O2 B. Na2O2和H2O C. NaOH和CO2 D. Na2CO3和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“反向燃烧”可将二氧化碳变燃料。回答下列问题:
(1)CO2的电子式为________________.
(2)美国橡树岭国家实验室成功利用表面成钉状材料的纳米碳及钠米铜,通电时可将温室气体二氧化碳与水直接转化为酒精。该反应的化学方程式为____________________________。
(3)Zn/ZnO热化学循环还原CO2制CO的原理如下图:
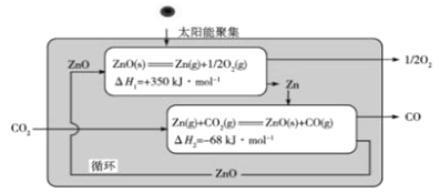
①从循环结果看,能量主要转化方式是________________________________。
②反应![]() △H= _______________kJ·mol-1。
△H= _______________kJ·mol-1。
(4)利用CO2与H2可直接合成二甲醚: ![]() ,当
,当![]() 时,实验测得CO2的平衡转化率随温度及压强变化如图1所示,二甲醚的产率随温度及压强变化如图2所示。
时,实验测得CO2的平衡转化率随温度及压强变化如图1所示,二甲醚的产率随温度及压强变化如图2所示。
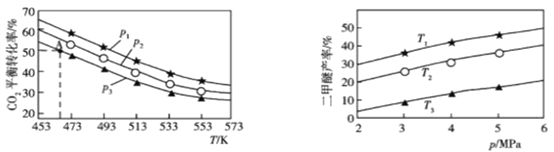
图1 图2
①该反应的△H________0(填“>”或“<”)。
②图1中压强(p)由大到小的顺序为______________________________。
③图2中温度(T)由大到小的顺序为______________________________。
④若在1L密闭容器中充入0.2mol CO2和0.6mol H2,平衡转化率对应图1中A点,则在此温度下该反应的平衡常数为________________________(保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 HBr溶液滴定15.00 mL 0.1000 mol·L-1 NaHCO3溶液,滴定曲线如下图所示:
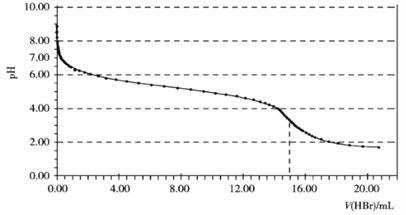
下列说法错误的是
A. 可用甲基橙作指示剂
B. 当V(HBr)=0.00 mL 时,溶液中c(OH-)>c(CO32-)
C. 当 V(HBr)=15.00mL 时,溶液中c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D. 当溶液的pH=7.00时,溶液中c(Na+)=c(Br-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com