
【题目】CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。

①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。

①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
【答案】 CH4(g)+H2O(g)=CO(g)+3H2(g) △H= + 206 kJ/mol 0.016mol/(L·min) C 小于 大于 1.6384 mol2/L2 c(NH4+)>c(HS—)>c(OH—)>c(H+)>c(S2—) 有副反应发生 < 平衡后,升高温度,甲醚的产率降低
【解析】试题分析:本题考查热化学方程式的书写,化学平衡的图像分析,化学平衡的标志,化学平衡常数的计算,溶液中离子浓度大小的比较。
(1)0.25molCH4与水蒸气完全反应制备“合成气”时吸收51.5kJ的热量,则1mol CH4与水蒸气完全反应制备“合成气”时吸收![]() =206kJ的热量,反应的热化学方程式为CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206kJ/mol。
=206kJ的热量,反应的热化学方程式为CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206kJ/mol。
(2)CH4和CO2反应制备合成气的反应为CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
①由图像知1100℃、P2时CH4的转化率为80%,则转化CH4物质的量为1mol![]() 80%=0.8mol,根据方程式知生成CO物质的量为1.6mol,υ(CO)=1.6mol
80%=0.8mol,根据方程式知生成CO物质的量为1.6mol,υ(CO)=1.6mol![]() 10L
10L![]() 10min=0.016mol/(L·min)。
10min=0.016mol/(L·min)。
② A,υ(H2)逆=3υ(CO)正表明逆反应速率大于正反应速率,反应没有达到平衡状态;B,该反应中所有物质都是气态,根据质量守恒定律,混合气体的质量始终不变,容器的容积不变,混合气体的密度始终不变,密闭容器中混合气体的密度不变不能说明反应达到平衡状态;C,该反应的正反应是气体分子数增大的反应,建立平衡过程中气体分子物质的量增大,密闭容器中总压强增大,平衡时气体分子物质的量不变,密闭容器中总压强不变,密闭容器中总压强不变能说明反应达到平衡状态;D,达到平衡时各物质的浓度保持不变,不一定相等,c(CH4)=c(CO)不能说明反应达到平衡状态;能说明反应达到平衡状态的是C项,答案选C。
③该反应的正反应为气体分子数增大的反应,增大压强平衡向逆反应方向移动,CH4的转化率减小,由图知在相同温度下P1时CH4的转化率大于P2,则P1小于P2。由图知,y点CH4转化率小于平衡时CH4的转化率,反应正向进行,υ(正)大于υ(逆)。y点的温度与x点的温度相同,y点平衡常数与x点相等,用三段式
CH4(g) + CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
c(起始)(mol/L)0.1 0.1 0 0
c(转化)(mol/L)0.1![]() 0.8=0.08 0.08 0.16 0.16
0.8=0.08 0.08 0.16 0.16
c(平衡)(mol/L)0.02 0.02 0.16 0.16
K=![]() =
=![]() =1.6384(mol/L)2。
=1.6384(mol/L)2。
(3)HS-在溶液中既存在电离平衡又存在水解平衡,HS-的水解离子方程式为HS-+H2O![]() H2S+OH-,HS-的水解平衡常数Kh=
H2S+OH-,HS-的水解平衡常数Kh=![]() =
=![]() =
=![]() =
=![]() =7.69
=7.69![]() 10-8
10-8![]() Ka2(H2S),HS-的水解程度大于HS-的电离程度;由于K(NH3·H2O)
Ka2(H2S),HS-的水解程度大于HS-的电离程度;由于K(NH3·H2O)![]() Ka1(H2S),NH4+的水解程度小于HS-的水解程度,溶液呈碱性,则NH4HS溶液中离子浓度由大到小的顺序为c(NH4+)
Ka1(H2S),NH4+的水解程度小于HS-的水解程度,溶液呈碱性,则NH4HS溶液中离子浓度由大到小的顺序为c(NH4+)![]() c(HS-)
c(HS-)![]() c(OH-)
c(OH-)![]() c(H+)
c(H+)![]() c(S2-)。
c(S2-)。
(4)①290℃前,CO转化率和甲醚产率的变化趋势不一致,说明在290℃前有副反应发生。
②由图可见升高温度,CO转化率减小,甲醚产率减小,升高温度平衡向逆反应方向移动,逆反应为吸热反应,正反应为放热反应,ΔH![]() 0,即b
0,即b![]() 0。
0。


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】CaSO4·2H2O受热会逐步失去结晶水。取纯净的CaSO4·2H2O固体3.44 g进行加热,测定固体质量随温度的变化情况如右图所示。C点固体的化学式是________________。T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的说法中,正确的是( )
A.硅是常用的半导体材料,可用于制造光导纤维B.二氧化硅是酸性氧化物,故不与任何酸反应
C.硅酸是一种二元弱酸,其酸性强于碳酸D.制造普通玻璃的主要原料是纯碱、石灰石和石英
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用锌片和稀硫酸反应制取氢气时,为加快生成氢气的速率,下列措施不适宜的是
A. 对该反应体系加热 B. 加入硝酸铜固体
C. 改用粗锌 D. 不用锌片,改用锌粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品安全已成为近几年来社会关注的热点问题之一。下列有关食品添加剂使用的说法正确的是( )
A. 为了调节食品色泽,改善食品外观,使用工业色素苏丹红
B. 为了提高奶粉中的氮含量,加入适量的三聚氰胺
C. 为了防止食品腐败,加入适量苯甲酸钠以达到阻抑细菌繁殖的作用
D. 食盐是咸味剂,无防腐作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分析正确的是
A. 异丁烷的二氯代物有4种
B. 区别蛋白质和淀粉可用浓硝酸做颜色反应
C. 石蜡油分解产物均能使酸性KMnO4溶液褪色
D. 甲苯的硝化反应方程式为: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3广泛用于染料等工业。某化学学习小组借助拉瓦锡研究空气成分的曲颈甑(装置甲)合成PC13,并采取PCl3氧化法制备POCl3。
已知:(1)PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;
(2)2PCl3+O2==2POCl3。
【实验Ⅰ】制备PCl3
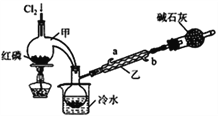
(1)实验室制备Cl2的原理是________________________。
(2)碱石灰的作用除了处理尾气外还有________________________。
(3)装置乙中冷凝水从_____(选填a或b)进入。
【实验Ⅱ】制备POCl3
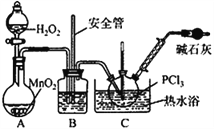
(4)实验室常用有微孔的试剂瓶保存H2O2,“微孔”与上述装置中的___________(仪器名称)目的是一致的。
(5)C中反应温度控制在60~65℃,其原因是________________________。
【实验Ⅲ】测定POCl3含量
①准确称取30.70gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+ 为指示剂,用0.2000mol/LKSCN 溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN 溶液。
已知:Ag++SCN-==AgSCN↓ Ksp(AgCl)>Ksp(AgSCN )。
(6)POC13水解的化学反应方程式为________________________。
(7)滴定终点的现象为____________,用硝基苯覆盖沉淀的目的是________________________。
(8)反应中POC13的百分含量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列仪器使用前必须检查是否漏水的有_________(填序号)。
A.容量瓶 B.蒸馏烧瓶 C.分液漏斗 D.量筒 E.蒸发皿
(2)实验室用Na2CO3·10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格___________,应称量多少克Na2CO3·10H2O晶体_____。
(3)某学生欲用10mol·L-1浓盐酸和蒸馏水配制500mL物质的量浓度为5mol·L-1的稀盐酸。则所需要浓盐酸体积为___mL,配制过程中正确的操作顺序是(字母表示,每个字母只能用一次)_________
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制一定体积、一定物质的量浓度的溶液,实验结果偏高影响的是_______
A.容量瓶中原有少量水 B.溶解所用烧杯未洗涤 C.定容时仰视观察刻度线 D.定容时俯视观察刻度线
(5)下图是某同学在实验室配制该NaCl溶液的过程示意图,其中有错误的是______(填操作序号)。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如下:


(1)A的名称是_______________,A分子中最多有_____个原子共平面。
(2)B生成A的化学方程式______________________。
(3)D生成E的反应类型为_________,试剂a是_________。
(4)F的结构简式_____________________。
(5)J是一种酯,分子中除苯环外还含有一个五元环。写出H生成J的化学方程式_____(注明反应条件)。
(6)![]() ,X的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有______种,写出其中核磁共振氢谱有五组吸收峰的结构简式___________________。
,X的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有______种,写出其中核磁共振氢谱有五组吸收峰的结构简式___________________。
(7)利用题中信息和所学知识,写出以甲烷和化合物D为原料,合成 ![]() 的路线流程图____________________(其它试剂自选)。
的路线流程图____________________(其它试剂自选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com