
【题目】CaSO4·2H2O受热会逐步失去结晶水。取纯净的CaSO4·2H2O固体3.44 g进行加热,测定固体质量随温度的变化情况如右图所示。C点固体的化学式是________________。T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为____________。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组中化合物的性质比较,正确的是( )
A.酸性:HClO>HBrO4>HIO4
B.碱性:Al(OH)3>Mg(OH)2>NaOH
C.稳定性:PH3>H2S>HCl
D.非金属性:F>O>S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家在1965年9月首先用人工方法合成牛胰岛素。为了证实人工合成的胰岛素与天然的是否是同一物质,在人工合成牛胰岛素过程中掺入了放射性14C,然后将人工合成的牛胰岛素与天然的混合得到了放射性14C分布均匀的结晶物,从而证明了两者都是同一种物质,为我国在国际上首先合成具有生物活性牛胰岛素提供了有力证据。在人工合成过程中掺入放射性14C的用途是 ( )
A. 催化剂 B. 媒介质 C. 组成元素 D. 示踪原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的产物中,存在同分异构体的是( )
A. CH3CH2CH2Br在碱性溶液中水解
B. 甲苯在催化剂(FeBr3)作用下与Br2发生苯环上的取代反应
C. ![]() 与NaOH的醇溶液共热反应
与NaOH的醇溶液共热反应
D. ![]() 在催化剂存在下与H2完全加成
在催化剂存在下与H2完全加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,0.1mol·L-1的HNO2、HCOOH、HCN、H2CO3的溶液,它们的电离平衡常数分别为4.6×10-4、1.8×10-4、4.9×10-10、K1=4.3×10-7和K2=5.6×10-11,其中氢离子浓度最小的是
A. HNO2 B. HCOOH
C. HCN D. H2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种由KCl、NaCl组成的混合物中,钾、钠离子的物质的量之比是1:2,则此混合物中,KCl的质量分数是___________.如果该混合物中含6molCl-,那么,此混合物中有NaCl__________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳生活”是生态文明的前提和基础,减少二氧化碳的排放是“低碳”的一个重要方面,因此,二氧化碳的减排已引起国际社会的广泛关注。请回答下面二氧化碳回收利用的有关问题:
I.利用太阳能等可再生能源,通过光催化、光电催化或电解水制氢来进行二氧化碳加氢制甲醇时发生的主要反应是:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)若二氧化碳加氢制甲醇反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到1,时刻达到平衡状态的是____________(填字母编号)
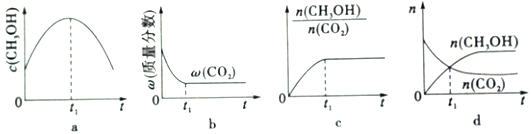
(2)常压下,二氧化碳加氢制甲醇反应时的能量变化如图1所示,则该反应的△H=_____。
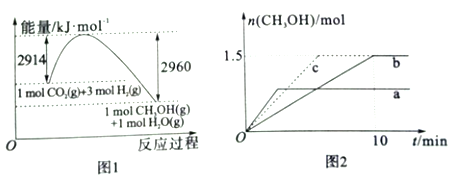
(3)在2L恒容密闭容器a和b中分别投入2molCO2和6molH2在不同温度下进行二氧化碳加氢制甲醇反应,各容器中甲醇的物质的量与时间关系如图2所示:
①若实验a、实验b的反应温度分别为T1、T2,则判断T1_____T2 (选填”>”、“<”或“=”)。若实验b中改变条件时,反应情况会由曲线b变为曲线c,则改变的条件是________。
②计算实验b条件下,0--10min段氢气的平均反应速率v(H2)=_____mol/(L·min)。
③在实验b条件下,该反应的平衡常数为_________。若平衡时向容器再充入1molCO2和3molH2,重新达平衡时,混合气体中甲醇的物质的量分数______30%(选填“>”“<”或“=”)。
II.右图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。
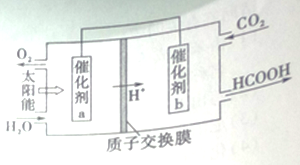
(4)催化剂a表面发生的电极反应式_________。
(5)标准状况下每回收44.8LCO2转移的的电子数为_______个。
(6)常温下,0.1mol/L的HCOONa溶液的pH为10,则常温下,HCOOH的电离常数Ka约为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。

①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。

①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com