
【题目】“低碳生活”是生态文明的前提和基础,减少二氧化碳的排放是“低碳”的一个重要方面,因此,二氧化碳的减排已引起国际社会的广泛关注。请回答下面二氧化碳回收利用的有关问题:
I.利用太阳能等可再生能源,通过光催化、光电催化或电解水制氢来进行二氧化碳加氢制甲醇时发生的主要反应是:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)若二氧化碳加氢制甲醇反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到1,时刻达到平衡状态的是____________(填字母编号)
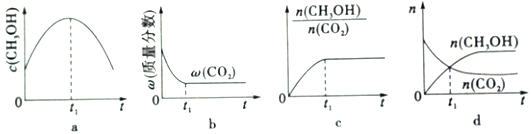
(2)常压下,二氧化碳加氢制甲醇反应时的能量变化如图1所示,则该反应的△H=_____。
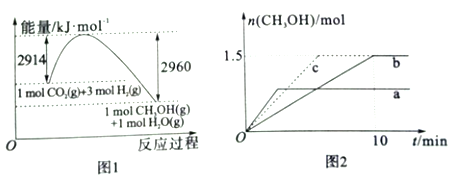
(3)在2L恒容密闭容器a和b中分别投入2molCO2和6molH2在不同温度下进行二氧化碳加氢制甲醇反应,各容器中甲醇的物质的量与时间关系如图2所示:
①若实验a、实验b的反应温度分别为T1、T2,则判断T1_____T2 (选填”>”、“<”或“=”)。若实验b中改变条件时,反应情况会由曲线b变为曲线c,则改变的条件是________。
②计算实验b条件下,0--10min段氢气的平均反应速率v(H2)=_____mol/(L·min)。
③在实验b条件下,该反应的平衡常数为_________。若平衡时向容器再充入1molCO2和3molH2,重新达平衡时,混合气体中甲醇的物质的量分数______30%(选填“>”“<”或“=”)。
II.右图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。
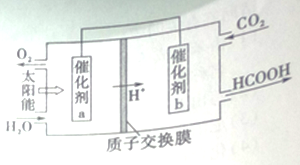
(4)催化剂a表面发生的电极反应式_________。
(5)标准状况下每回收44.8LCO2转移的的电子数为_______个。
(6)常温下,0.1mol/L的HCOONa溶液的pH为10,则常温下,HCOOH的电离常数Ka约为__________。
【答案】 bc -46kJ·mol-1 > 加入催化剂 0.225 ![]() (或5.33) > 2H2O - 4e- == O2↑+4H+ 2.408×1024(或4NA) 10-7
(或5.33) > 2H2O - 4e- == O2↑+4H+ 2.408×1024(或4NA) 10-7
【解析】(1)a、t1甲醇的溶液仍在变小,故错误;b、t1时二氧化碳的质量分数保持恒定,说明反应达到平衡,故正确;c、t1时,甲醇与二氧化碳的物质的量之比保持恒定,达到平衡,故正确;d、t1时二氧化碳在减小,甲醇在增加,故末达到平衡,故错误,故选bc。(2)常压下,二氧化碳加氢制甲醇反应时的能量变化,该反应的△H= 2914kJ·mol-1-2960kJ·mol-1=-46kJ·mol-1 ;(3)①若实验a、实验b的反应温度分别为T1、T2,a先达到平衡,对应的温度高,则判断T1>T2 ;若实验b中改变条件时,反应情况会由曲线b变为曲线c,平衡不移动,则改变的条件是加入催化剂;②计算实验b条件下,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),平衡时甲醇的物质的量为1.5mol,氢气的变化量为4.5mol,0--10min段氢气的平均反应速率v(H2)=
CH3OH(g)+H2O(g),平衡时甲醇的物质的量为1.5mol,氢气的变化量为4.5mol,0--10min段氢气的平均反应速率v(H2)=![]() = 0.225mol/(L·min)。③在实验b条件下,
= 0.225mol/(L·min)。③在实验b条件下,
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
n始/mol 2 6
n变/mol 1.5 4.5 1.5 1.5
n平/mol 0.5 1.5 1.5 1.5
c平/mol·L-1 0.25 0.75 0.75 0.75
该反应的平衡常数为![]() =5.33。若平衡时向容器再充入1molCO2和3molH2,相当于加压,平衡正向移动,重新达平衡时,混合气体中甲醇的物质的量分数>30%。(4)催化剂a表面由图可知水失电子生成氧气,发生的电极反应式: 2H2O - 4e- == O2↑+4H+ ;(5)HCOOH中碳为+2价,CO2中碳为+4价,标准状况下每回收44.8LCO2转移的的电子数为
=5.33。若平衡时向容器再充入1molCO2和3molH2,相当于加压,平衡正向移动,重新达平衡时,混合气体中甲醇的物质的量分数>30%。(4)催化剂a表面由图可知水失电子生成氧气,发生的电极反应式: 2H2O - 4e- == O2↑+4H+ ;(5)HCOOH中碳为+2价,CO2中碳为+4价,标准状况下每回收44.8LCO2转移的的电子数为![]() =2.408×1024个。(6)常温下,0.1mol·L-1的HCOONa溶液pH为10,溶液中存在HCOO-水解HCOO-+H2O
=2.408×1024个。(6)常温下,0.1mol·L-1的HCOONa溶液pH为10,溶液中存在HCOO-水解HCOO-+H2O![]() HCOOH+OH-,故Kh=
HCOOH+OH-,故Kh=![]() =10-7,则HCOOH的电离常数Ka=Kw/Kh=10-14/10-7=10-7。
=10-7,则HCOOH的电离常数Ka=Kw/Kh=10-14/10-7=10-7。


科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HClO |
|
|
电离平衡常数 |
|
|
|
|
(1)室温下![]()
![]()
![]()
![]()
![]() 溶液的pH由大到小的关系为______.
溶液的pH由大到小的关系为______.
(2)浓度均为![]() 的
的![]() 和
和![]() 的混合溶液中,
的混合溶液中, ![]() 、
、![]() 、
、![]() 、
、![]() 浓度从大到小的顺序为______.
浓度从大到小的顺序为______.
(3)少量![]() 通入到过量的NaClO溶液中发生反应的离子方程式______.
通入到过量的NaClO溶液中发生反应的离子方程式______.
(4)常温下, ![]() 的HCOOH溶液与
的HCOOH溶液与![]() 的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为______.
的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaSO4·2H2O受热会逐步失去结晶水。取纯净的CaSO4·2H2O固体3.44 g进行加热,测定固体质量随温度的变化情况如右图所示。C点固体的化学式是________________。T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A. ρ=![]() B. w=
B. w=![]()
C. w=![]() D. c=
D. c=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.甘肃马家密遗址出土的青铜刀是我国最早治炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜録”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
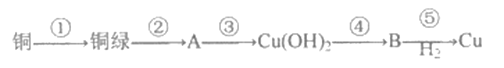
(1)从物质分类标准看,“铜绿”属于______(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:____________。
(3)请写出铜録与盐酸反应的化学方程式:________________________。
(4)上述转化过程中属于化合反应的是_______________(填序号)
II.胶体是一种常见的分散系,回答下列问题。用Fe(OH)3胶体进行下列实验:
(5)将其装入U型管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色_______,这说明_________,这种现象称为____________________________。
(6)向其中滴入过量稀硫酸,现象是___________,其原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液,溶液中含碳微粒的物质的量分数随溶液pH的变化如下图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是
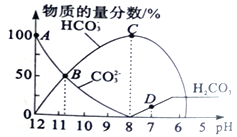
A. A点时,溶液中c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B. B点时,溶液中c(Na+)>c(CO32-)=c(HCO3-)>(H+)>c(OH-)
C. C点时,溶液中浓度最大的离子是 Na+
D. D点时,溶液的pH为7,溶液的总体积为20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的说法中,正确的是( )
A.硅是常用的半导体材料,可用于制造光导纤维B.二氧化硅是酸性氧化物,故不与任何酸反应
C.硅酸是一种二元弱酸,其酸性强于碳酸D.制造普通玻璃的主要原料是纯碱、石灰石和石英
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用锌片和稀硫酸反应制取氢气时,为加快生成氢气的速率,下列措施不适宜的是
A. 对该反应体系加热 B. 加入硝酸铜固体
C. 改用粗锌 D. 不用锌片,改用锌粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列仪器使用前必须检查是否漏水的有_________(填序号)。
A.容量瓶 B.蒸馏烧瓶 C.分液漏斗 D.量筒 E.蒸发皿
(2)实验室用Na2CO3·10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格___________,应称量多少克Na2CO3·10H2O晶体_____。
(3)某学生欲用10mol·L-1浓盐酸和蒸馏水配制500mL物质的量浓度为5mol·L-1的稀盐酸。则所需要浓盐酸体积为___mL,配制过程中正确的操作顺序是(字母表示,每个字母只能用一次)_________
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制一定体积、一定物质的量浓度的溶液,实验结果偏高影响的是_______
A.容量瓶中原有少量水 B.溶解所用烧杯未洗涤 C.定容时仰视观察刻度线 D.定容时俯视观察刻度线
(5)下图是某同学在实验室配制该NaCl溶液的过程示意图,其中有错误的是______(填操作序号)。


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com