
【题目】有下列六种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3。
(1)25℃时,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是______________________________________(用离子方程式表示);
(2)常温下,浓度均为0.1mol/L的③和⑥的溶液中离子种类________(填“相同”或是“不相同”);
(3)将④溶液加热蒸干并灼烧最终得到的物质是____________(填化学式);
(4)常温下0.1 mol/L的⑤溶液加水稀释过程中,下列表达式的数据一定变大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
【答案】 < NH4++H2O![]() NH3·H2O+H+ 相同 Al2(SO4)3 B
NH3·H2O+H+ 相同 Al2(SO4)3 B
【解析】(1)氯化铵是强酸弱碱盐,铵根水解;
(2)碳酸根水解,碳酸氢根既水解又电离;
(3)硫酸铝水解生成氢氧化铝和硫酸;
(4)醋酸是一元弱酸,存在电离平衡,根据外界条件对电离平衡的影响分析。
(1)铵根水解,则0.1mol·L-1氯化铵溶液的pH<7,铵根水解的离子方程式为NH4++H2O![]() NH3·H2O+H+;
NH3·H2O+H+;
(2)碳酸钠中碳酸根水解,且水解分步进行,碳酸氢钠中的碳酸氢根离子存在水解平衡和电离平衡,则浓度均为0.1mol/L的两溶液中离子种类相同;
(3)铝离子水解,水解吸热,但由于生成的硫酸是难挥发性酸,则将硫酸铝溶液加热蒸干并灼烧最终得到的物质仍然是Al2(SO4)3;
(4)醋酸是弱酸,存在电离平衡:CH3COOH![]() CH3COO-+H+,稀释促进电离,则A.氢离子的物质的量增加,但c(H+)降低,A错误;B.稀释过程中氢离子的物质的量增加,醋酸的物质的量减少,则比值c(H+)/c(CH3COOH)增大,B正确;C.温度不变,水的离子积常数不变,即c(H+)·c(OH-)不变,C错误。答案选B。
CH3COO-+H+,稀释促进电离,则A.氢离子的物质的量增加,但c(H+)降低,A错误;B.稀释过程中氢离子的物质的量增加,醋酸的物质的量减少,则比值c(H+)/c(CH3COOH)增大,B正确;C.温度不变,水的离子积常数不变,即c(H+)·c(OH-)不变,C错误。答案选B。


科目:高中化学 来源: 题型:
【题目】已知乙醇、石墨和氢气的燃烧热分别为a、b、c(均为正值,单位均为kJ·mol-1)。则反应2C(s,石墨)+2H2(g)+H2O(l)==C2H5OH(l)的焓变为( )
A. (2b+2c-a) kJ·mol-1 B. (b+c-a) kJ·mol-1
C. (a-2b-2c) kJ·mol-1 D. (a-2b-c) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某种酶生物燃料电池的工作原理示意图。下列说法中不正确的是
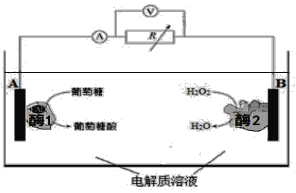
A. 葡萄糖是还原剂
B. 外电路中电子由A极移向B极
C. 溶液中H+ 由B极区移向A极区
D. B极电极反应式为:H2O2 +2H++2e-=== 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,在充电和放电时,其电池反应为Mg+2MnF3![]() 2MnF2+MgF2。下列说法不正确的是( )
2MnF2+MgF2。下列说法不正确的是( )
A. 放电时,镁为负极材料
B. 放电时,电子从镁极流出,经电解质流向正极
C. 充电时,阳极的电极反应式为:MnF2+F--e-=MnF3
D. 充电时,外加直流电源负极应与原电池的Mg极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比是重要的学习方法,类比pH的定义可定义pOH和pKW。在某弱酸HX及其盐NaX的混合溶液中(HX和NaX的含量不确定),c(H+)和c(OH-)存在如图所示的关系,则下列说法不正确的是
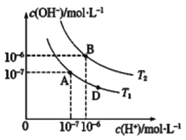
A. 图中温度T2>25℃
B. 若此混合溶液呈酸性且c(HX)=c(NaX),则HX电离能力大于NaX的水解能力
C. 位于AB线段上任意点的溶液均有pH=pOH=![]()
D. 图中D点处溶液中离子浓度:c(Na+)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某温度(t℃)时,水的Kw=10-13,则该温度(填 “大于”“小于”或“等于”)_________ 25℃,理由是_________,将此温度下pH =11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合液为中性,则a∶b_________;
(2)若所得混合液的pH=2,则a∶b_________。
Ⅱ.25℃时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,下列说法不正确的是(_____)
A.该溶液pH=4 B.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
C.此酸的电离平衡常数约为1×10-7 D.升高温度,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用下列4种物质的序号填空:①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有极性键的是___________。(填序号)
(2)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃(2.02×105 Pa),但在180 ℃就开始升华。据此判断,氯化铝是___________(填“共价化合物”或“离子化合物”),设计实验证明你的判断正确的实验依据是________________。
(3)现有a~g7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:
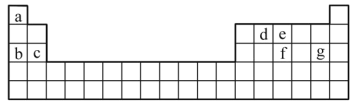
①元素的原子间反应最容易形成离子键的是___________。
A.c和f B.b和g C.d和g D.b和e
②d与g元素形成的分子中所有原子___________(填“是”或“不是”)都满足最外层为8电子结构。
(4)A、B、C、D四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素,已知B、D两元素间可形成DB2和DB3两种化合物,两者相对分子质量相差16;又如A、C两元素原子序数之和是B、D两元素原子序数之和的1/2。请回答下列问题:
①写出由B、C两种元素形成的原子个数比为1:1的化合物的电子式:________,其晶体中所含化学键的类型有________。
②A2B与A2D的沸点:A2B________A2D(填“高于”或“低于”),其原因是____________。
③由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式:____________________________。
④碳元素的一种同位素可测定文物年代,这种同位素的符号是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com