
 压强(Mpa) 压强(Mpa) 氨的平 氨的平衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 9 5.4 5.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
| | 反应速率 | 平衡常数K | 氨的体积分数 |
| 变化情况 | | | |
| A.0.3mol | B.0.15mol | C.小于0.15mol | D.大于0.15mol,小于0.3mol |
科目:高中化学 来源:不详 题型:单选题
 软锰矿制备高锰酸钾的一种工艺流程。
软锰矿制备高锰酸钾的一种工艺流程。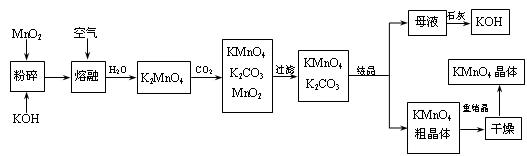
| A.75%酒精 | B.双氧水 | C.苯酚 | D.84消毒液(NaClO溶液) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾净水与液氯净水的原理相同 |
| B.镀层破损后,镀铜铁板比镀锌铁板更耐腐蚀 |
| C.必要时向空中播撒碘化银微粒,可达到人工降雨的目的 |
| D.碳酸钠可用于焙制糕点,也可用于治疗胃酸过多症 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
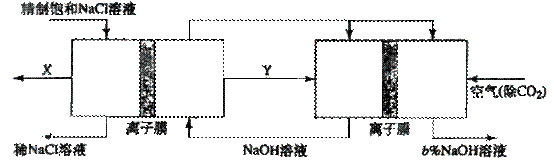
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
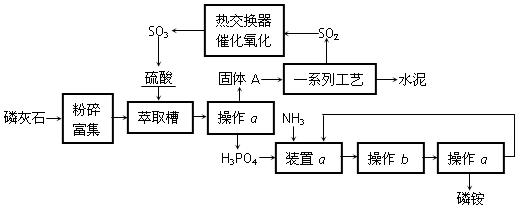
| A.NaOH溶液、酚酞试液 | B.KMnO4溶液、稀H2SO4 |
| C.碘水、淀粉溶液 | D.氨水、酚酞试液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
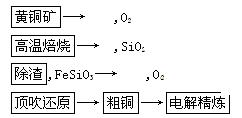
 到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
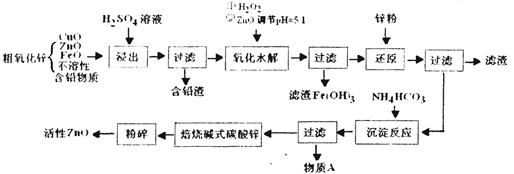
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:
后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将氯气通入澄清石灰水制取漂白粉 |
| B.电解饱和食盐水溶液制取金属钠 |
| C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
| D.用98.3%的浓H2SO4吸收SO3,目的是防止形成酸雾,使SO3吸收完全 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com