
| A、反应混合物中各组分的浓度相等 |
| B、正逆反应都还在继续进行 |
| C、正逆反应的速率均为零 |
| D、化学平衡理论是研究怎样使原料尽可能多地转化为产品 |


科目:高中化学 来源: 题型:
| A、在含等物质的量的AlO2-、OH-、CO32-混合溶液中,逐滴加入盐酸:OH-、AlO2-、CO32-、HCO3- |
| B、在含等物质的量的NH4+、Al3+、H+的溶液中,逐滴加入氢氧化钠溶液:H+、NH4+、Al3+ |
| C、在含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ |
| D、在含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
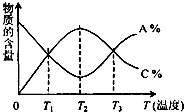 已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )
已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )| A、该反应在T1、T3温度时达到过化学平衡 |
| B、该反应在T2温度时达到过化学平衡 |
| C、该反应的逆反应是吸热反应 |
| D、升高温度,平衡会向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2可与水反应 |
| B、Al(OH)3是既能与强酸反应又能与强碱反应,是两性氢氧化物 |
| C、金属钠投入硫酸铜溶液中可置换出金属铜 |
| D、NaHCO3俗称是小苏打,可用作食用碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 恒温下,a mol A和b mol B在如图所示活塞可自由滑动的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )
恒温下,a mol A和b mol B在如图所示活塞可自由滑动的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )| A、物质A、B的转化率之比为a:b |
| B、起始时刻和达平衡后容器中的压强比为(a+b):(a+b-n/2) |
| C、平衡时C的体积分数为n/(a+b-n/2) |
| D、当v正(A)=2v逆(B)时,可判定反应达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、溶液中c(NH3?H2O)?
| ||||
| B、NH3?H2O的电离程度增大,c(OH-)也增大 | ||||
| C、溶液中导电微粒数目减少 | ||||
| D、再加20mL pH=3的盐酸,混合溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中始终有:c(Na+)+c(H+)═2c(S2-)+c(HS-)+c(OH-) |
| B、t溶液呈中性时:c(Na+)═c(HS-)+c(S2-) |
| C、等体积混合后溶液中一定有:c(H2S)+c(H+)═c(S2-)+c(OH-) |
| D、恰好完全中和后的溶液中:c(Na+)>2c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com