
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 足量铜片与含0.2mol H2SO4的浓硫酸共热,反应生成的SO2的分子数为0.1NA
B. 室温下,0.3molL-1的Na2SO4溶液中含Na+ 数目为0.6NA
C. 标准状况下,NA个SO3分子所占的体积约为22.4L
D. NO2和N2O4的混合物共9.2g,其中所含氧原子数一定为 0.4NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】把下列物质分别加入盛水的锥形瓶,立即塞紧带U形管的塞子。已知U形管内预先装有少量水且液面相平(为便于观察,预先染成红色),加入下列哪些物质后,发生如如图所示变化( )

① NH4NO3晶体 ② 浓H2SO4 ③ NaOH粉末
④ NaCl晶体 ⑤ Na2O2固体 ⑥ 生石灰
A. ①②④⑤ B. ①②③
C. ③④⑤ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验(夹持仪器省略)。将液体A逐滴加入到固体B中,回答下列问题:
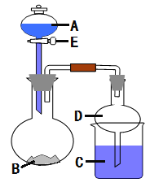
(1)图中盛放液体A的仪器名称为_________________,D装置在实验中的作用是_______________________。
(2)若A为浓盐酸,B为KMnO4,C中盛有KI-淀粉溶液,旋开E后,C中的现象为____________;C中发生反应的离子方程式为__________;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的化学方程式: ______。
(3)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是__________,C中发生反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中的浓硫酸滴入②中,预测的现象与结论相符的是( )

A. 若②为浓盐酸;产生大量气体产生;说明硫酸的酸性比盐酸强
B. 若②为铜片;有气泡产生,底部生成灰白色固体;说明浓硫酸有强氧化性
C. 若②为蓝色硫酸铜晶体;蓝色晶体变为白色;说明浓硫酸有吸水性,发生物理变化
D. 若②为蔗糖;白色固体变为黑色海绵状,有气体放出;说明浓硫酸有脱水性、氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2CrO4溶液,发生的两个化学反应为SO2+2Fe3++2H2O=SO42-+2Fe2++W ①,Cr2O72-+aFe2++bH+![]() Cr3++Fe3++H2O ②,下列有关说法正确的是
Cr3++Fe3++H2O ②,下列有关说法正确的是
A. 还原性:Cr3+>SO2 B. 配平后方程式②中,a=6,b=7
C. Cr2O72-能将Na2SO3氧化成Na2SO4 D. 方程式①中W为OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。在下图所示物质转化关系中,e是由该四种元素组成的离子化合物,m是Y的单质,n是Z的单质,m、n均为空气的主要成分,p是W的单质,其余为由上述的两种或三种元素组成的化合物;u的水溶液具有漂白性;t和v均为一元强酸。下列说法正确的是
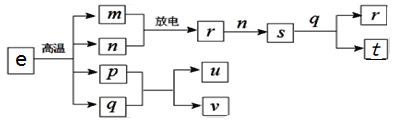
A. 物质u中既含共价键又含离子键
B. 常温常压下,r与s均为无色气体
C. 简单气态氢化物的热稳定性:Z<Y
D. X、Y、Z三种元素形成化合物的水溶液可能呈酸性,也可能呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冶炼金属一般有下列4种方法:①焦炭法;②水煤气法(或氢气、或一氧化碳)法;③活泼金属置换法;④电解法。4种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜。现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁。对它们的冶炼方法的分析不正确的是
A. (Ⅰ)用① B. (Ⅱ)用② C. (Ⅲ)用③ D. (Ⅳ)用④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L固定容积的密闭容器中,800 ℃时发生反应2NO(g)+O2(g)![]() 2NO2(g)。该体系中,n(NO)随时间的变化如下表:
2NO2(g)。该体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.012 | 0.009 | 0.008 | 0.0075 | 0.0075 |

反应过程如上图所示,a、b、c、d其中只有3条曲线是正确的。请回答:
(1)图中表示NO2的变化的曲线是________,A点时,v(正)______v(逆) (填“大于”“小于”或“等于”,下同)。用O2表示从0~3 s内该反应的平均速率v=____________。
(2)能说明该反应已经达到平衡状态的是________ (填字母)。
a.混合气体的平均摩尔质量不变 b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
e.相同时间内,每消耗2a mol的NO同时生成等量的NO2
f.混合气体中O2和NO2物质的量之比为1∶2的状态
(3)已知上述反应为放热反应,达平衡后改变条件继续进行。在t1~t6内反应速率与时间图像如图,在每一时刻均只改变一个影响反应速率的因素,则下列说法正确的是__________。

A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t0~t1时X的转化率最高
(4)能使该反应的反应速率增大的是________(填字母)。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com