
【题目】已知98%的浓硫酸密度为1.84g/cm3。
(1)该硫酸的物质的量浓度为________mol·L-1。
(2)①用该浓度的硫酸配制500 mL 0.1 mol·L-1硫酸时,需该浓度的硫酸的体积为____mL,用到的玻璃仪器有量筒、烧杯、玻璃棒、_________________________________。
②下列操作会使所配硫酸浓度偏高的是________。
A.未洗涤烧杯和玻璃棒 B.定容时,加水超过刻度线后,吸出多余部分
C.定容时,俯视刻度线 D.容量瓶洗净后未干燥
(3)取稀释后的适量硫酸与足量的锌粒反应,生成标准状况下11.2 L H2,则反应中转移的电子数为________个。
【答案】 18.4 2.7 500 mL容量瓶, 胶头滴管 C NA (6.02×1023)
【解析】(1)c =(1000ρω)/M=![]() molL-1=18.4 molL-1。
molL-1=18.4 molL-1。
(2)①根据稀释定律:c1V1=c2V2得,18.4 molL-1×V mL×10-3LmL-1=0.1molL-1×500 mL×10-3LmL-1,解得V≈2.7;用浓硫酸配制500 mL 0.1 molL-1硫酸用到的玻璃仪器除了量筒、烧杯、玻璃棒外,还有500 mL容量瓶和定容用的胶头滴管。②根据c=n/V,误差分析时主要看操作造成n和V的变化;A项,未洗涤烧杯和玻璃棒会使n偏小,则c偏低;B项,定容时,加水超过刻度线,会使V偏大,则c偏低,即使吸出多余部分,也不会改变浓度偏低的事实(因为吸出的是溶液);C项,定容时俯视刻度线,会使V偏小,则c偏高;D项,容量瓶洗净后未干燥不影响实验结果。综上,选C。
(3)标准状况下11.2LH2的物质的量是:11.2L÷22.4Lmol-1=0.5mol,根据反应化学方程式:Zn+H2SO4=ZnSO4+H2↑,H元素化合价由0升为+1,若生成1molH2则转移2mol电子,所以生成0.5molH2则转移1mol电子,即生成标准状况下11.2LH2转移电子数为NA(6.02×1023)。


科目:高中化学 来源: 题型:
【题目】甲,乙两同学用图所示装置进行实验探究硝酸与铁反应的产物。

文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、﹣3价等氮的化合物。
Ⅱ.FeSO4+NOFe(NO)SO4(棕色)△H<0.
Ⅲ.NO2和NO都能被KMnO4氧化吸收
Ⅳ.铁氰化钾化学式为K3[Fe(CN)6]:亚铁氰化钾化学式为K4[Fe(CN)6]
3Fe2++2[Fe(CN)6]3﹣═Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4﹣═Fe4[Fe(CN)6]3↓(蓝色沉淀)
甲的实验操作和现象记录如下:
实验操作 | 实验现象 |
打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余,得100mL的溶液 |
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是____________。
A.常温下铁和浓硝酸不反应
B. 铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生
C.反应需要催化剂
(2)甲的实验操作中通入CO2的主要目的是__________。
A. 排除反应体系中的空气 ,防止干扰
B. 将产生的气体压入后续装置吸收
C.维持系统内压强平衡
(3)甲取少量B中溶液,加热,现象是_________。
A.棕色溶液变浅绿色 B.棕色溶液变无色 C.有红棕色气体逸出
D.有无色气体逸出 E.产生红褐色沉淀
(4)乙认为有NO生成的证据不足.乙仍采用该装置和操作进行对照实验,浓硝酸换成稀硝酸,证明有NO生成的实验现象是A中___________________B中。
(5)将A所得溶液稀释至500mL,取少量稀释后的溶液调节pH后,滴加铁氰化钾溶液有蓝色沉淀生成。另取稀释后的溶液25.00mL加入过量的KI固体,充分反应后pH至7左右,滴入几滴淀粉溶液做指示剂,用0.25mo1/L Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3溶液16.00mL.(己知:I2+2S2O32﹣=2I﹣+S4O62﹣),则A中所得溶液的c(Fe3+)=______mo1/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C. 离子Y2-和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到cmolNH3,则原溶液中Al3+的浓度(mol/L)为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【衡阳市2017届下学期第三次联考】石油分馈得到的轻质油可通过Pt催化重整脱氢环化,逐步转化为芳香烃。以链烃A为原料合成两种髙分子材料的路线如下:
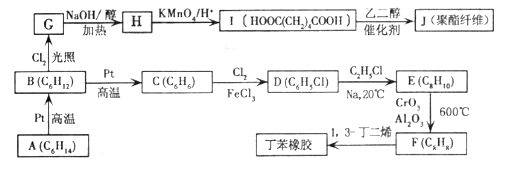
已知以下信息:
①B的核磁共振氢谱中只有一组峰;G为一氯代烃。
②R—X+R′—X![]() R—R′(X为卤素原子,R、R'为烃基)
R—R′(X为卤素原子,R、R'为烃基)
回答以下问题:
(1)B的名称为_______;由F生成丁苯橡胶的反应类型是______________。
(2)E分子中最多有____个原子共面;J的结构简式为_______。
(3)由G生成H的化学方程式为___________________。
(4)I的同分异构体中,能同时满足下列条件的结构共有____种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;
②既能发生银镜反应,又能发生水解反应。
其中核磁共振氢谱为4组峰,且面积比为6: 2:1:1的是_____ (写出其中一种的结构简式)。
(5)参照上述合成路线,以2 -甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应其△H= -122 kJ/mol,△S=231J/(mol·K),则下列哪种情况下该反应可自发进行( )
A. 仅在低温下可以自发进行 B. 在任何温度下都不能自发进行
C. 仅在高温下可以自发进行 D. 在任何温度下都能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】凡有一个手性碳原子的物质一定具有光学活性,物质B有光学活性,其发生下列反应后生成的产物有光学活性的是( )
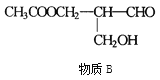
A. 与NaOH水溶液共热 B. 与乙酸发生酯化反应
C. 与银氨溶液作用 D. 在催化剂存在下与H2作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com