
【题目】A—F 6种有机物,在一定条件下,按下图发生转化。
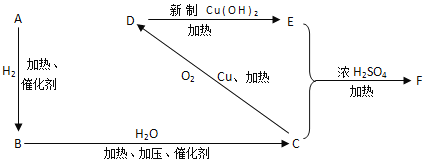
又知烃A与氢气的相对密度是13,试回答下列问题:
(1)有机物的名称:A._______,B._________,D.___________。
(2)有机物的结构简式:E._____________,F.____________。
(3)反应BC的化学方程式是___________,反应类型属于__________反应
CD的反应方程式是_____________________反应类型属于__________反应。
C + E→F的反应化学方程式______________________反应类型属于__________反应。
【答案】乙炔 乙烯 乙醛 CH3COOH CH3COOC2H5 CH2=CH2+H2O![]() CH3CH2OH 加成 2CH3CH2OH+O2
CH3CH2OH 加成 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化 CH3COOH+CH3CH2OH
2CH3CHO+2H2O 氧化 CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O 酯化或取代
CH3COOC2H5+H2O 酯化或取代
【解析】
烃A与氢气的相对密度是13,其摩尔质量为13×2g/mol=26g/mol,故A为CH≡CH,乙炔与氢气发生加成反应生成B,B与水反应生成C,C可以连续发生氧化反应,故C为醇,则B为CH2=CH2,乙烯与水发生加成反应生成C为CH3CH2OH,乙醇发生催化氧化生成D为CH3CHO,乙醛进一步氧化生成E为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3,据此解答。
烃A与氢气的相对密度是13,其摩尔质量为13×2g/mol=26g/mol,故A为CH≡CH,乙炔与氢气发生加成反应生成B,B与水反应生成C,C可以连续发生氧化反应,故C为醇,则B为CH2=CH2,乙烯与水发生加成反应生成C为CH3CH2OH,乙醇发生催化氧化生成D为CH3CHO,乙醛进一步氧化生成E为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3。
(1)由上述分析可知,A为乙炔,B为乙烯,D为乙醛;
(2)由上述分析可知,E的结构简式为CH3COOH,F的结构简式为CH3COOCH2CH3;
(3)B→C是乙烯与水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O![]() CH3CH2OH;反应类型属于加成反应;
CH3CH2OH;反应类型属于加成反应;
(4)C→D是乙醇发生氧化反应生成乙醛,反应方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,反应类型属于氧化反应;
2CH3CHO+2H2O,反应类型属于氧化反应;
C+E→F是乙酸与乙醇发生酯化反应生成乙酸乙酯CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O;反应类型属于酯化反应或取代反应。
CH3COOC2H5+H2O;反应类型属于酯化反应或取代反应。


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】铅蓄电池的示意图如图所示.已知:2PbSO4+2H2O![]() Pb+PbO2+2H2SO4
Pb+PbO2+2H2SO4

下列说法正确的是( )
A. 放电时,N 为负极,其电极反应式为:PbO2+SO42﹣+4H++2e﹣=PbSO4+2H2O
B. 放电时,c(H2SO4)不变,两极的质量增加
C. 充电时,阳极反应式为:PbSO4+2e﹣=Pb+SO42﹣
D. 充电时,若 N 连电源正极,则该极生成 PbO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学欲完成两个实验,涉及到下列有关实验操作。甲实验为食盐的精制,乙实验通过精制的食盐来配制0.4mol·L-1的氯化钠溶液。

(1)甲实验中除去难溶性杂质的操作步骤是___________(填写上述序号),其中关键实验操作名称是___________。
(2)甲实验中,为有效除去粗盐中的Ca2+、Mg2+、SO42-杂质,精制过程中加入试剂:
①NaOH溶液②Na2CO3溶液③BaCl2溶液④盐酸,合理的加入顺序为____(填序号)。其中加入NaOH溶液所发生反应的离子方程式为________________。
(3)乙实验,使用仪器③前必须进行的一步操作是______。配制时,除了上述仪器外,还可能用到的玻璃仪器是_____________。
(4)乙实验称量的NaCl质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为_____________mol·L-1.
(2)达到滴定终点的标志是_______________________________________________________
(3)以下操作造成测定结果偏高的原因可能是__________________。
A. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 未用标准液润洗碱式滴定管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如下图所示。下列有关叙述正确的是
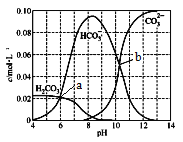
A. b点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)
B. 随pH增大,![]() 数值先减小后增大
数值先减小后增大
C. 25℃时,碳酸的第一步电离常数Ka1=10-6
D. 溶液呈中性时:c(HCO3- )>c(Cl-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年我国科研人员研制出一种室温“可呼吸”NaCO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是:

A.“吸入”CO2时,钠箔为正极
B.“呼出”CO2时,Na+向多壁碳纳米管电极移动
C.“吸入”CO2时的正极反应:4Na+ + 3CO2 + 4e—= 2Na2CO3 + C
D.标准状况下,每“呼出”22.4LCO2,转移电子数为0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的 SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(1)为加快工业废碱渣中 Na2CO3 的溶解,可采取的措施是_____(写出一种即可)。
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为_____。
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是_____。
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4 的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,_____,出现白色沉淀,则证明含有 Na2SO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通电条件下,用如图所示装置由乙二醛(OHC-CHO)制备乙二酸(H00C-COOH)。其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl。下列说法正确的是( )

A. 盐酸是起提供Cl-和增强导电性的作用
B. Pt1的电极反应为:4OH--4e-=2H2O+O2↑
C. 每消耗0.1mol乙二醛在Pt1极放出2.24L气体(标准状况)
D. 每得到lmol乙二酸将有2molH+从右室迁移到左室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如装置简图:

请你参与分析讨论:
(1)图中仪器B的名称:____________________。
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_____________。
(3)实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:_________________________________________________。
(4)C中液体产物颜色为___________________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行分离的操作是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com