
苯是重要的化工原料,请回答以下制备中的有关问题:
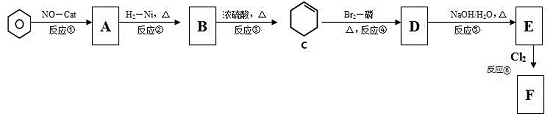
已知:I.CH3CH=CH2 + Cl2  ClCH2CH=CH2 + HCl
ClCH2CH=CH2 + HCl
Ⅱ. F的结构简式为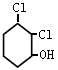
(1)指出反应类型。反应①是氧化反应,反应③是 。
(2)写出结构简式:B ;D 。
(3)C生成D时还可能生成另一种有机物,分离D和该有机物的方法是
。
(4)检验A是否全部转化为B可用的试剂是 。
(5)写出F与NaOH水溶液共热的反应方程式 。
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
已知H2A在水中存在以下平衡:H2A===H++HA-,HA-H++A2-。
(1)常温下NaHA溶液的pH________(填序号,下同),原因是_____________。
A.大于7 B.小于7
C.等于7 D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1 KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是________。
A.c(H+)·c(OH-)=1.0×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________。
A.升高温度 B.降低温度
C.加入NH4Cl晶体 D.加入Na2A固体
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,回答有关问题:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑴ | ⑵ | ||||||
| 三 | ⑶ | ⑷ | ⑸ | ⑹ | ⑺ | ⑻ | ⑼ | |
| 四 | ⑽ | ⑾ | ⑿ |
(1)写出下列元素符号:⑴ ,⑹
(2)在这些元素中,最不活泼的元素的结构示意图是 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为 ;碱性最强的与呈两性的发生反应的离子方程式为 .
(4)在⑵⑶⑻⑽这些元素简单离子中,离子半径由大到小的顺序是 (填离子符号)
(5)元素⑻、⑾和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有 。(2分)
(6)用电子式表示由元素(8)和(10)形成化合物的过程: 。(2分)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计能够成功的是
| 实验目的 | 实验步骤及现象 | |
| A | 检验亚硫酸钠试样是否变质 |
|
| B | 检验某盐是否为铵盐 |
|
| C | 证明酸性条件H2O2氧化性比I2强 |
|
| D | 除去氯化钠晶体中少量硝酸钾 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,属于水解反应的是( )
A.CH3COOH +H2O  CH3COO- + H3O+
CH3COO- + H3O+
B.SO2 + H2O  HSO3- + H+
HSO3- + H+
C.HS- + H2O  S2- + H3O+
S2- + H3O+
D.CO32- + H2O  HCO3- + OH-
HCO3- + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
取五等份NO2,分别通入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)  N2O4(g) ,△H<0,反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随温度(T)变化关系图。下列示意图中,最可能与实验结果相符的是( )
N2O4(g) ,△H<0,反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随温度(T)变化关系图。下列示意图中,最可能与实验结果相符的是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是
A.R一定是共价化合物 B.R一定是离子化合物
C.R可能是共价化合物,也可能是离子化合物
D.R可能是气态物质,也可能是固态物质
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列操作中,一般情况下不能相互接触的是( )
A.过滤时,玻璃棒与三层滤纸
B.分液时,分液漏斗下端与烧杯内壁
C.过滤时,烧杯内壁与漏斗下端
D.用胶头滴管向试管内滴加液体时,胶头滴管尖端与试管内壁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com