
【题目】下列说法正确的是
A. 25 ℃时,向水中加入少量固体NaHSO4,c(H+)增大,Kw不变
B. 向0.1 mol·L-1CH3COOH溶液中加入少量的CH3COONa晶体,  减小
减小
C. 常温下,向BaCO3饱和溶液中加入Na2CO3固体,c(Ba2+)减小,BaCO3的Ksp减小
D. 一定条件下,将一定浓度的CH3COONa溶液加水稀释,溶液中所有离子的浓度都减小
科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式中,不正确的是( )
A.向FeCl2溶液中通入氯气,溶液变为黄色:2Fe2++Cl2=2Fe3++2Cl-
B.向铜粉中滴加稀硝酸,产生气体:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C.向CuSO4溶液中滴加NaOH溶液,产生蓝色沉淀:Cu2++2OH-=Cu(OH)2↓
D.Na2O2是重要的供氧剂:2Na2O2+2H2O=4Na++4OH-+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为_____。
(2)A中的碳原子是否都处于同一平面?_____(填“是”或“不是”)。
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
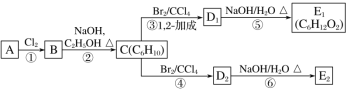
C的化学名称是______;反应⑤的化学方程式为______;E2的结构简式是___________;④、⑥的反应类型依次_______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) + O2(g) ![]() 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中,正确的是
甲 | 乙 | 丙 | ||
起始物质的量 | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2的平衡转化率 / % | 80 | α1 | α2 | |
A. 甲中反应的平衡常数小于乙
B. 平衡时,丙中c(SO3)是甲中的2倍
C. 该温度下,平衡常数值为400
D. 平衡时,甲中O2的转化率大于乙中O2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工光合系统装置(如图)可实现以CO2和 H2O 合成CH4。下列有关说法不正确的是()

A. 该装置中铜为正极
B. 电池工作时H+向Cu电极移动
C. GaN 电极表面的电极反应式为: 2H2O-4e-═O2+4H+
D. 反应CO2+2H2O═CH4+2O2中每消耗 1mol CO2转移 4mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 强电解质溶液的导电能力一定比弱电解质溶液的强
B. 一定温度下,可逆反应2X(g)+Y(g)![]() 2Z(g)达到平衡的标志是:容器内X、Y、Z的物质的量之比为2:1:2
2Z(g)达到平衡的标志是:容器内X、Y、Z的物质的量之比为2:1:2
C. 升高温度,AgCl的溶解度增大,Ksp增大
D. FeCl3、KAl(SO4)2、Na2CO3的水溶液均显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯为原料,在一定条件下可以转化为A、B、C,最后合成有果香的D,转化关系如下图所示。
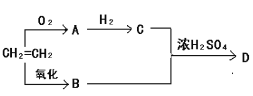
(1)写出物质A中的官能团名称_____;
(2)CH2=CH2与B反应也可以生成D,该反应的反应类型属于_____;
(3)写出B+C→D的方程式___;
(4)下列说法不正确的是____。
A.CH2=CH2能与溴水和酸性高锰酸钾溶液反应,两者的褪色原理不相同
B.物质A与新制Cu(OH)2悬浊液混合后加热,可以出现砖红色沉淀
C.实验室制备物质D时,常用饱和Na2CO3溶液收集产物,且有机层在下层
D.等物质的量的CH2=CH2和C完全燃烧,耗氧量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示有关物质的相互转化关系,其中A是由G和某淡黄色固体组成的混合物,I是常见的无色液体,反应①在化工生产中有着重要应用(部分产物和条件已略去)。

(1)写出以下物质的化学式:B_______、F_______。
(2)反应②的离子方程式为_______。
(3)我国首创的由G、空气和海水组成的电池,在航海领域有着极其重要的作用,其工作时正极反应式为_______,该电池最大的优点是只需补充_______〔填“正极”或“负极”〕材料就可接着使用。
(4)向M的水溶液中加入少量A中的淡黄色固体,反应的化学方程式为_______。
(5)25℃时,pH均为5的盐酸和M的水溶液中,由H2O电离出的H+物质的量浓度之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铁厂的废渣铁矾渣主要含有K2Fe6(SO4)4(OH)12 、ZnO![]() Fe2O3 及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3 及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:

(1)试剂1是过量的______。
(2)试剂2为过量的铁粉,加入后可以观察的现象有 ______________________。
(3)NH4F溶液不能放入玻璃器皿中保存,理由是_____________________________(用离子方程式表示)。已知:25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol L-1,此时Ca2+是否也完全沉淀?写出具体的分析过程:______(若溶液中某离子浓度小于1.0×10-5mol L-1时,说明该离子已沉淀完全)。
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO32Me(OH)2H2O沉淀的化学方程式为 ________________________________.
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矶渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8 ,M=476 g mol -1 )__________万吨。
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式__________ 。
②680 °C时所得固休的化学式为____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com