
ѡ��(12��)����ѧһ���ʽṹ�����ʡ�ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ���Ȼ���д��ڶ���A�Ļ����Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��B��C���γ����������η��ӣ�D�Ļ�̬ԭ�ӵ������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӡ�
��ش��������⣺
��1��������Ԫ���е縺������Ԫ�أ����̬ԭ�ӵļ۵����Ų�ʽΪ_________����һ��������С��Ԫ����__________(��Ԫ�ط���)��
��2��C���������ǰ����Ԫ�طֱ���A�γɵĻ�����е��ɸߵ��͵�˳����________(�ѧʽ)��
��3��BԪ�ؿ��γɶ��ֵ��ʡ�һ�־���ṹ��ͼһ��ʾ����ԭ�ӹ�����ӻ�����Ϊ________����һ�ֵľ�����ͼ����ʾ�����˾����е��ⳤΪ356.6pm����˾������ܶ�Ϊ_________g��cm-3(������λ��Ч����)��(��֪�� )
)

��4��D�Ĵ����ξ���ֲ��ṹ��ͼ�����þ����к��еĻ�ѧ����________(��ѡ�����)��
�ټ��Լ� �ڷǼ��Լ� ����λ�� �ܽ�����
��5����D����������Һ�еμӹ�����ˮ���۲쵽�����γ���ɫ�����������μӰ�ˮ�������ܽ⣬�õ�����ɫ������Һ����д�������ܽ�����ӷ���ʽ��_________________��
 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ��ɽ�и߶���ѧ�ڿ�ѧ���л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��Ȼ�ѧ����ʽ�������У���ȷ����
A����20.0 g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ���������÷�Ӧ���Ȼ�ѧ����ʽ�� NaOH(aq)��HCl(aq)��NaCl(aq)��H2O(l) ��H����57.4 kJ��mol-1
B����֪C(ʯī��s)��C(���ʯ��s) ��H��0������ʯһ����ʯī�ȶ�
C����֪2H2O(g)��2H2(g)��O2(g) ��H����483.6 kJ��mol-1�����ṩ483.6 kJ����ʱ��һ����ʹ2 mol H2O (g)�����ֽ�
D����֪C(s)��O2(g)��CO2(g) ��H��a kJ��mol-1��2C(s)��O2(g)��2CO(g)����H��b kJ��mol-1����2CO(g)��O2(g)��2CO2(g) ��H��(2a��b) kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�˱��и����ڶ�����ϲ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ����pH��Ϊ2��HCl��HX����Һ�ֱ��ˮϡ�ͣ���ҺpH����Һ����仯����������ͼ��ʾ������˵����ȷ����

A��ϡ��ǰ��c(HX)=0.01 mol/L B��ϡ��10����HX��Һ��pH��3
C��a��b���㣺c(X��)>c(Cl��) D����Һ�ĵ����ԣ�a>b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и�����������Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣��輰�仯�����ڹ�ҵ���й㷺��;���Թ�ۡ�þ�۵�ԭ���Ʊ�����Ĺ�ҵ�������£�
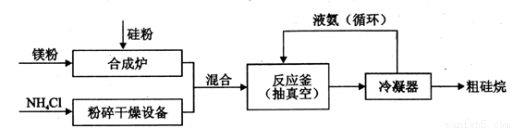
��Ӧ���з�����Ӧ��4NH4Cl+Mg2 Si 4NH3��+SiH4��+2MgCl2 ��H<0
4NH3��+SiH4��+2MgCl2 ��H<0
��1����ҵ�Ͽ��ù���Ͱ�������һ�������µIJ���Si3 N4��Si3 N4Ӧ���� ���壻NH3��Si3 N4��SiH4�������ʵ��۷е��ɸߵ��͵�˳���� ��
��2��������������Ĺ����з�Ӧ������յ�ԭ���� ��
��3��Һ������ѭ���������� ��
��4������Ҳ����Ҫ�Ĺ�ҵԭ�ϣ�1mol������һ���¶��£�T>150�棩������������Ӧ���ͷų�226��5kJ���������÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��5��������þ��Mg2Si3O8��nH2O��������ˮ����ҽҩ�Ͽ�����������������кͶ���θ�ᣨ��Ҫ�ɷ����ᣩ�����ɵ������ﻹ�ɸ������������θ���棬�����䲻���ܴ̼���������þ��θ�ᷴӦ�Ļ�ѧ����ʽ�� ������1��84g������þ�ӵ�50mL 1��0mol/L�����У���ַ�Ӧ����ȥ�������Լ���Ϊָʾ������l��0mol/L NaOH��Һ�ζ�ʣ������ᣬ����NaOH��Һ30mL����Mg2Si3O8��nH2O��n��ֵ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и�����������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ�������ơ������¼�����۽��Ͷ���ȷ����
ʵ�������� | �����¼ | ���۽��� | |
A | ������Ũ������μ���Cu��ϡ����Ļ������ | ��������ɫ���� | ���ᱻ��ԭΪNO2 |
B | ������ǯ��ס�����ھƾ����ϼ��� | �����ۻ����������� | �۵㣺Al2 O3>Al |
C | ��ij�Ȼ�������Һ�м��� Na2O2��ĩ | ���ֺ��ɫ���� | ����Na2O2��ĩǰ��ԭ�Ȼ� ������Һ�Ѿ����� |
D | ����ɫʯ����Һ�г�����ʱ��ͨ������ | ��Һ�ȱ�죬����Ϊ��ɫ | ������Ư���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
N2O5��һ����������������һ���¶��¿ɷ������·�Ӧ��
2 N2O5 (g) 4NO2(g)+O2(g) ��H>0
4NO2(g)+O2(g) ��H>0
T1�¶�ʱ�����ܱ�������ͨ��N2O5������ʵ�����ݼ��±�

����˵���в���ȷ����
A��T1�¶��£�500sʱO2��Ũ��Ϊ0��74mol��L-1
B��ƽ��������������䡣�����������ѹ����ԭ����l��2������ƽ��ʱc(N2O5)> 5��00mol��L-1
C��T1�¶��µ�ƽ�ⳣ��ΪK1��T2�¶��µ�ƽ�ⳣ��ΪK2����T1>T2��K1<K2
D��T1�¶��µ�ƽ�ⳣ��ΪK1=125��ƽ��ʱN2O5��ת����Ϊ0��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ��һģ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
(12��)����ѧ�����л���ѧ���������ʹ�(G)�����������㾫����ϳ�·�����£�


��ش��������⣺
��1��G�������ֹ����ŵ����Ʒֱ���________��__________��
��2��ͬʱ������������������B��ͬ���칹����____________�֡�
i��������Ԫ̼����̼���Ͻ�������ȡ�����ҳʶ�λ��
ii����һ���������ܷ���������Ӧ��ˮ�ⷴӦ����ȥ��Ӧ��
��3��Ϊ�˼���E��F����ѡ�������Լ��е�_______�������Լ�(�����������ĸ)��
a����ˮ b��������Һ c������KMnO4��Һ d��NaHCO3��Һ
��4��C��D�Ļ�ѧ����ʽΪ_________________��
��5������A(����ʽΪC7H10O3)���⻯�õ�H(����ʽΪC7H12O3)��H��һ�������¿������ɸ߾���I��I�Ľṹ��ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ��3��һģ��ѧ�Ծ��������棩 ���ͣ������
��18�֣�X��Y��Z��W��E���ֶ�����Ԫ����Ԫ�����ڱ���λ����ͼ������W��ԭ��������Y��2����

��1����֤��X��Z��Ԫ�طǽ�����ǿ�������ӷ���ʽΪ
��2��һ�������£��ں��������У�����һ������WY2 (g)��XY (g)��������Ӧ��
 ʱ�������ʵ�ƽ��Ũ�����±���
ʱ�������ʵ�ƽ��Ũ�����±���

�����¶����ߵ� T2��ʱ����Ӧ��ƽ�ⳣ��Ϊ6.64����÷�Ӧ���淴ӦΪ______��Ӧ������ȡ����ȡ�����
�������������䣬���÷�Ӧ�ں�ѹ�����½��У�ƽ��ʱXY��ת����a2______a1��T1��ʱ��ת���ʣ����<����>����=����
��3�������£�Mg(OH)2������Һ______����ܡ����ܡ���ʹʯ����Һ������ͨ������˵��ԭ��(��֪�� ����
����
��4����ѧ��Ӧ �ڹ�ҵ����������Ҫ�ĵ�λ����Ҫ���E2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______������ĸ���ţ�
�ڹ�ҵ����������Ҫ�ĵ�λ����Ҫ���E2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______������ĸ���ţ�
a�������¶� b���Ӵ��� c������H2��Ũ�� d�������EH3
һ�������£�1mol E2��3molH2���ܱ������з�Ӧ�ﵽƽ�⣬E2��ת����Ϊ25%�ҷų�23.lkJ��������������·�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ____________________��
��5���绯ѧ���ⷨ����������ˮ�������ε���Ⱦ����ԭ����ͼ��ʾ������BΪ��Դ��______������缫��ӦʽΪ______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳɼס������ݡ����������ͭ�ۣ�������ܽ�9.6gͭ�ۡ��������������ۣ�������ܽ�14.0g���ۡ� (��������ֻ����ԭΪNO����)�����з��������������
A��ԭ�������NO3�����ʵ���Ϊ0.1 mol
B������������������0.2mol
C��ԭ�������HNO3Ũ��Ϊ1.0 mol��L��1
D��ԭ�������H2SO4Ũ��Ϊ2.5 mol��L��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com