
【题目】下列物质属于非电解质的是
A. 氨 B. 硫酸铵 C. 氯气 D. 醋酸
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为![]() 、
、![]() 、
、![]() ,少量
,少量![]() )为原料,生产
)为原料,生产![]() 的部分工艺流程如下:
的部分工艺流程如下:

下列说法错误的是( )
A. 用![]() 溶液吸收焙烧过程产生的
溶液吸收焙烧过程产生的![]() 有利于保护环境和资源再利用
有利于保护环境和资源再利用
B. 从高硫铝土矿中可制得![]() 、
、![]() 的化合物
的化合物
C. 向“过滤”得到的滤液中通入过量![]() ,铝元素存在的形式由
,铝元素存在的形式由![]() 转化为
转化为![]()
D. ![]() 与
与![]() 混合后在无氧条件下焙烧的目的是生成
混合后在无氧条件下焙烧的目的是生成![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为VO2+(蓝色)+H2O+V3+(绿色) ![]() VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是
VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是
A. 充电时,反应每生成2 mol H+时转移的电子的物质的量为1 mol
B. 充电时,阳极附近溶液由绿色逐渐变为紫色
C. 放电时,负极反应为V2+-e-===V3+
D. 放电过程中,正极附近溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3②NO2进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度为( )

A. ①>② B. ①<② C. ①=② D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2。利用催化还原SO2法不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知CH4和S的燃烧热(ΔH)分别为-890.3 kJ/mol和-297.2 kJ/mol,则CH4和SO2反应的热化学方程式为_________________。
(2)在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:

①分析可知X为___________(填化学式),O~t1时间段的温度为_____________,0~t1时间段用SO2表示的化学反应速率为_________________。
②用H2还原SO2生成S的总反应的化学方程式为__________________。
(3)焦炭催化还原SO2生成S2,化学方程式为2C(s)+2SO2(g)![]() S2(g)+2CO2(g),恒容密闭容器中,1 mol/L SO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
S2(g)+2CO2(g),恒容密闭容器中,1 mol/L SO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
①该反应的ΔH_______(填“>”或“<”)0。
②计算a点的平衡常数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子的最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且元素Y的基态原子核外电子p电子比s电子多5个。
(1)Z的基态原子的核外电子排布式为_____________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯()裂化生成苯和丙烯。
①1 mol丙烯分子中含有σ键与π键数目之比为_____________。
②苯分子中碳原子的杂化轨道类型为_____________。
③Z的一种氧化物ZO5中,Z的化合价为+6价,则其中过氧键的数目为_________个。

(3)W、X、Y三种元素的电负性由小到大的顺序为_______(请用元素符号回答)。
(4)ZY3的熔点为1 152 ℃,其在熔融状态下能够导电,据此可判断ZY3晶体属于_________(填晶体类型)。
(5)ZX2晶体的晶胞结构如图所示,每个Z原子周围最近的X原子数目为________。若该化合物的相对分子质量为M,晶胞边长为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味的气体放出,符合这一情况的是
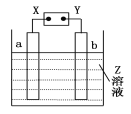
a极板 | b极板 | X电极 | Z | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈碱性的原因是:________________(写离子方程式);灭火器内另有一容器中装有Al2(SO4) 3溶液,该溶液呈酸性的原因是:________(写离子方程式)。当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH)3,阻止火势蔓延。其相关的离子方程式为:______________________________。
(2)碱性锌锰干电池负极的电极反应:_____________________________:甲醇燃料电池在碱性条件下负极的电极反应:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是__________:X与氢元素形成的化合物的电子式是__________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,D与E能形成一种三核分子,该分子的结构式为__________;D所在族元素的氢化物中沸点最低的是__________。
(3)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com