
【题目】下列事实不能用化学平衡移动原理解释的是
A. 光照新制的氯水时,溶液的pH逐渐减小
B. 红棕色的NO2,加压后颜色先变深后变浅,但比原来要深
C. 500℃时比室温更利于合成氨
D. 用排饱和食盐水法收集Cl2
【答案】C
【解析】A. 新制氯水中存在平衡Cl2+H2O![]() HCl+HClO,光照使次氯酸分解,次氯酸浓度减小,平衡正向移动,氢离子浓度增大,溶液的pH减小,能用平衡移动原理解释,故A不选;B. 红棕色的NO2中存在平衡2NO2
HCl+HClO,光照使次氯酸分解,次氯酸浓度减小,平衡正向移动,氢离子浓度增大,溶液的pH减小,能用平衡移动原理解释,故A不选;B. 红棕色的NO2中存在平衡2NO2![]() N2O4,加压后体积减小,混合气体颜色变深,因压强增大平衡正向移动,颜色会逐渐变浅,但NO2的浓度仍比原来大,所以颜色比原来深,能用平衡移动原理解释,故B不选;C. 合成氨的反应为放热反应,升高温度不利于平衡向正反应方向移动,采用500℃主要是考虑催化剂的活性和反应速率,与平衡移动无关,不能用平衡移动原理解释,故C选;D. 氯气与水发生反应:Cl2+H2O
N2O4,加压后体积减小,混合气体颜色变深,因压强增大平衡正向移动,颜色会逐渐变浅,但NO2的浓度仍比原来大,所以颜色比原来深,能用平衡移动原理解释,故B不选;C. 合成氨的反应为放热反应,升高温度不利于平衡向正反应方向移动,采用500℃主要是考虑催化剂的活性和反应速率,与平衡移动无关,不能用平衡移动原理解释,故C选;D. 氯气与水发生反应:Cl2+H2O![]() HCl+HClO,饱和氯化钠中氯离子浓度较大,可抑制氯气和水的反应,使平衡逆向移动,能用平衡移动原理解释,故D不选;答案选C。
HCl+HClO,饱和氯化钠中氯离子浓度较大,可抑制氯气和水的反应,使平衡逆向移动,能用平衡移动原理解释,故D不选;答案选C。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。则坩埚中发生反应的化学方程式为____________________________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是_________________________。
[方案三]按如下图所示装置进行实验:
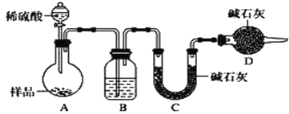
(1)D装置的作用是______________________,分液漏斗中__________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_____。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到实验目的的是
操作 | 目的 | |
A | 称取5.0gCuSO4·5H2O加入27.0g水中,搅拌溶解 | 配制10%CuSO4溶液 |
B | 先用稀盐酸洗涤,再用水清洗 | 洗涤分解KMnO4制O2的试管 |
C | 用玻璃棒蘸取溶液,点在干燥的pH试纸上,片刻后与标准比色卡比较并读数 | 测定0.05mol.L-1NaClO溶液的pH |
D | 将粗碘放入烧杯中,烧杯口放一盛满冷水的烧瓶,隔石棉网对烧杯加热,然后收集烧瓶外壁的固体 | 提纯混有NH4Cl的粗碘 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学链燃烧技术有利于提高燃料利用率。化学链燃烧技术的基本原理是将传统的燃料与空气直接接触反应的燃烧借助于载氧剂(如Fe2O3、FeO等)的作用分解为几个气固反应,燃料与空气无需接触,由载气剂将空气中的氧传递给燃料。回答下列问题:
(1)用Fe2O3作载氧剂的化学链燃烧部分热化学方科式及循环转化的原理如下:
I.C(s)+H2O(g)==CO(g)+H2(g) △H1
II.Fe2O3(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H2
III.Fe2O3(s)+1/3H2(g)=2/3Fe3O4(s)+1/3H2O(g) △H3
IV.Fe3O4(s)+1/4O2(s)=3/2Fe2O3 (s) △H4
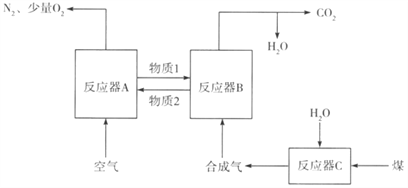
①在反应器B中进行的反应是_______(填反应前面的代号);“物质2”是______(填化学式)。
②反应C(s)+O2(g)=CO2(g)的△H=______(用△H1、△H2、△H3、△H4表示)。
(2)用FeO作载氧剂部分反应的lgKp[Kp是用平衡分压代替平衡浓度(平衡分压=总压×物质的量分数)]与温度的关系如下图所示:
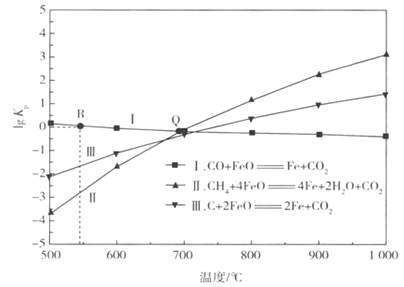
①图中涉及的反应中,属于吸热反应的是______(填反应前面的代号)。
②恒容密闭容器中进行反应:CH4(g) +4FeO(s)=4Fe(s) +2H2O(g)+CO2(g),不能说明该反应已达到化学平衡的标志是______( 填字母)。
a.v正(CH4)=v正(CO2)
b.气体的压强不再随时间变化
c.气体的密度不再随时间变化
d.单位时间内断裂C-H键与断裂H-O键数目相等
③若某恒容密闭容器中只发生反应I和II,平衡时对应上图中Q 处时,容器中气体分压p(X)间应满足的关系是__________。
④在某密闭容器中充入0.8 molCO和0.2 mol CO2 并加入足量的FeO,只发生反应I,在R点(lgKp=0),则CO的平衡转化率为________。
(3)若用CaSO4作载氧剂进行化学链燃烧时,CaSO4与CO发生反应生成CaS,则反应的化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁[(C5H5)2Fe](橙黄色粉末,不溶于水,易溶于乙醚等有机溶剂)及其衍生物在工业、农业、医药、航天、节能、环保等行业具有广泛地应用。某校课外小组依据反应2KOH+2C5H6+FeCl2=(C5H5)2Fe+2KCl+2H2O在绝对无水、无氧的条件下制备二茂铁。
回答下列问题:
(1)甲组同学拟制备无水FeCl2,主要实验流程为:

步骤I用饱和Na2CO3溶液浸泡的目的是_______;步骤II 中铁屑是过量的,其目的是_____;步骤IV脱水的方法是____________。
(2)乙组用环戊二烯二聚体(沸点为174℃)制备环戊二烯(沸点为419℃),已知:(C5H6)2(环戊二烯二聚体)![]() 2C5H6(环戊二烯)。分离得到环戊二烯的操作方法为________。
2C5H6(环戊二烯)。分离得到环戊二烯的操作方法为________。
(3)丙组同学制备二茂铁的装置如图所示(夹持装置已略去)。

已知:二甲基亚砜的结构式为 ,热稳定性好,能溶解大多数有机物。
,热稳定性好,能溶解大多数有机物。
①图中冷却水从接口______进入(填“a”或“b”)。
②装药品前及整个过程需通入干燥的A,装药品前通入N2的目的是_________。
③反应后分离出上层橙黄色乙醚清液,先用盐酸洗涤,其目的是_______;再用水洗,水洗时能说明已洗涤干净的依据是_________;洗涤后得到的二茂铁乙醚溶液获得二茂铁固体可采用的操作方法是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①、过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及H2O、Cr2O72―、NO2―、H+、NO3―、Cr3+六种微粒,已知反应过程中NO2-浓度变化如图所示,下列说法不正确的是

A. Cr2O72-中Cr化合价是+6价
B. 反应的氧化产物是NO3-
C. 消耗1mol氧化剂,转移电子6mol
D. 随着反应的进行,溶液中的H+ 浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com