
【题目】原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36, Y基态原子最外层电子数是其内层电子总数的3倍,X、W基态原子是同周期元素中未成对电子数最多的原子,X与Z的原子核内质子数之和等于W原子核内质子数,Z基态原子只有1个未成对的电子。
回答下列问题:
(1)已知化合物XZ3与H2Y(Y的氢化物)发生反应的化学方程式为XZ3+H2Y→XH3+HZY,则元素的电负性:Y Z(填“大于”或“小于”),化合物HZY分子的空间构型为 。
(2)X的一种氢化物的相对分子质量为32,1mol该氢化物中的σ键数是 ,该氢化物在水中的溶解性如何?主要原因是什么?
(3)元素Y 3个原子形成的单质分子与元素X、Y形成的一种离子互为等电子体,这种离子的化学式是 。
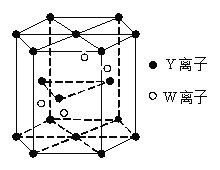
(4)基态W原子的电子排布式是 ,元素Y和W的一种化合物的晶体结构如右图所示,该晶体的化学式为 。(W处于晶体内部,Y分别处于晶胞面心、顶点、和内部)
(5)金属原子 (选填“钾”、“镁”、“铜”)形成的晶体的堆积方式,与上述晶胞中Y离子的堆积方式相同。
【答案】(1)大于 V形
(2)5×6.02×1023 能与水分子间形成氢键,易溶于水
(3)NO2-
(4)1s22s22p63s23p63d54s1或[Ar]3d54s1Cr2O3
(5)镁
【解析】试题分析:原子序数依次增加的X、Y、Z、W四种元素原子序数均小于36,Y基态原子最外层电子数是其内层电子总数的3倍,则Y为O元素;X、W基态原子是同周期元素中未成对电子数最多的原子,X原子序数比氧小则X在第二周期为N元素;则W为第三周期的P或第四周期的Cr;已知X与Z的原子核内质子数之和等于W原子核内质子数,若W为P,则Z为O,与Y相同,所以不符合题意,若W为Cr,则Z为Cl,而且Cl的基态原子只有1个未成对的电子;综上可知:X为N元素,Y为O元素,Z为Cl元素,W为Cr元素;
(1)已知化合物NCl3与H2O发生反应的化学方程式为NCl3+H2O→NH3+HClO,反应产物HClO中O元素为-2价,Cl元素为+1价,即O的得电子能力更强,所以电负性O大于Cl,HClO的结构为H-O-Cl,与H2O的H-O-H相似,是V形;
(2)N的一种氢化物常见的有NH3和N2H4,相对分子质量为32的是N2H4,其结构式为![]() ,分子中含有5个σ键,所以1mol该氢化物中的σ键数是5×6.02×1023;N2H4能与水分子间形成氢键,所以N2H4易溶于水;
,分子中含有5个σ键,所以1mol该氢化物中的σ键数是5×6.02×1023;N2H4能与水分子间形成氢键,所以N2H4易溶于水;
(3)元素O的一种单质分子与元素N、O形成的一种离子互为等电子体,已知O3和NO2-的原子数和价电子数相同互为等电子体,
(4)W为Cr元素,原子核外有24个电子,所以基态原子的电子排布式是;1s22s22p63s23p63d54s1,由图可知,晶胞内部含有4个Cr离子,O2-为:上下面12×2,顶点16×12,侧面12×6,所以共有6个,则Cr与O的离子数之比为2:3,所以该晶体的化学式为Cr2O3;
(5)由图可知,该晶胞为六方最密堆积,与Mg晶体的堆积方式相同。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 石英是制造光导纤维的原料,也是常用的半导体材料
B. 氧化铝是冶炼金属铝的原料,也是较好的耐火材料
C. 天然氨基酸能溶于强碱或强酸溶液,是两性化合物
D. 船舶外壳装上锌块,是牺牲阳极的阴极保护法进行防腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2,其部分生产流程如下:

已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 。
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: 。
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3。pH调节的范围是 ,试剂X可以选用 (填选项字母)。
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3·H2O
(4)电解(Ⅴ)中阳极的电极反应式为 。
(5)Zn和MnO2是制作电池的原料。某锌-锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。该电池的正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用
B.向某溶液中滴加硝酸酸化的BaCl2溶液产生白色沉淀,则该溶液中含有SO2-4
C.在电解精炼铜过程中,阳极质量的减少多于阴极质量的增加
D.298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,下列操作对实验结果没有影响的是( )
A. 容量瓶中原有少量蒸馏水 B. 洗涤烧杯和玻棒的溶液未转入容量瓶中
C. 定容时观察液面俯视 D. 定容时观察液面仰视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1989年世界卫生组织把铝确定为食品污染源之一,而加以控制使用。铝在下列应用时应加以控制的是( )
①制铝合金 ②制电线 ③制炊具 ④银色漆颜料 ⑤明矾净水 ⑥明矾与苏打制食品膨松剂 ⑦易拉罐 ⑧用Al(OH)3凝胶制胃舒平药片 ⑨包装糖果和小食品.
A. ③⑤⑧⑨ B. ③⑤⑥⑦⑧⑨ C. ③⑤⑨ D. ⑥⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)上述流程中“碱浸”后,物质A必须经过 (填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为 。
(2)上述流程中采用稀碱液比用热水更好,理由是稀碱液能 Na2S水解(选促进或抑制)
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)= mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)

(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如右图所示)。为使除汞效果最佳,应控制的条件是x控制 、pH控制 。
②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是
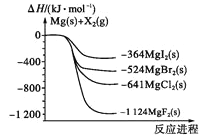
A.由MgCl2制取Mg是放热过程
B.热稳定性:MgI2<MgBr2<MgCl2<MgF2
C.常温下氧化性:F2<Cl2<Br2<I2
D.由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:
MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(g),ΔH=-117kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是______________,基态铜原子的核外电子排布式为________________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____________(填晶体类型)。
(3)CO和CO的一种生活中常见等电子体分子,两者相比较沸点较高的为__________(填化学式)。CN-中碳原子杂化轨道类型为_______________,C、N、O三元素的第一电离能最大的为_______________(用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示。每个铜原子周围距离最近的铜原子数目__________。
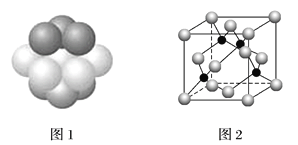
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为_____________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________________(填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的1/4,则该晶体中铜原子和M原子之间的最短距离为_______________pm(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com