
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要视角.硫及其化合物与价态变化为坐标的二维转化关系如图1所示.
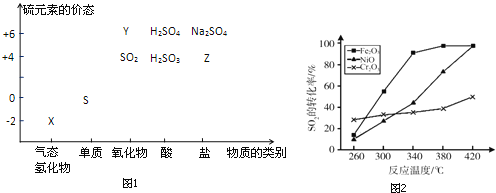
完成下列填空:
(1)图中X的电子式为__;其水溶液在空气中放置易变浑浊,写出反应的化学方程式__;该变化说明S的非金属性比O__(填“强”或“弱”),从原子结构的角度解释原因:__.通过__(举两例),也可以判断氧、硫两种元素的非金属性强弱.
(2)下列物质用于Na2S2O3制备,从氧化还原反应的角度,理论上有可能的是__(选填编号).
a Na2S+S b Z+S c Na2SO3+Y d NaHS+NaHSO3
(3)已知反应:Na2S2O3+H2SO4→Na2SO4+S↓+SO2+H2O,研究其反应速率时,下列方案合理的是__(选填编号).
a 测定一段时间内生成SO2的体积,得出该反应的速率
b 研究浓度、温度等因素对该反应速率的影响,比较反应出现浑浊的时间
c 用Na2S2O3固体分别与浓、稀硫酸反应,研究浓度对该反应速率的影响
(4)治理含CO、SO2的烟道气,以Fe2O3做催化剂,将CO、SO2在380℃时转化为S和一种无毒气体.已知:①硫的熔点:112.8℃、沸点:444.6℃;②反应每得到1mol硫,放出270kJ的热量.写出该治理烟道气反应的热化学方程式__.
(5)其他条件相同、催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图2.不考虑催化剂价格因素,生产中选Fe2O3做催化剂的主要原因是__.
【答案】![]()
![]() 弱 硫原子半径大于氧原子,硫原子得电子能力小于氧原子 H2O的稳定性大于H2S或SO2中硫显正价,氧显负价 bd b 2CO(g)+SO2(g)
弱 硫原子半径大于氧原子,硫原子得电子能力小于氧原子 H2O的稳定性大于H2S或SO2中硫显正价,氧显负价 bd b 2CO(g)+SO2(g)![]() S(l)+2CO2 (g)△H=﹣270kJ/mol Fe2O3作催化剂,在相对较低温度下,单位时间内获得较高的SO2转化率,且能耗小
S(l)+2CO2 (g)△H=﹣270kJ/mol Fe2O3作催化剂,在相对较低温度下,单位时间内获得较高的SO2转化率,且能耗小
【解析】
(1)X是-2价硫的气态氢化物,即硫化氢,其电子式为![]() ,-2价的硫具有很强的还原性,因此久置在空气中会被氧气氧化得到单质硫,反应方程式为
,-2价的硫具有很强的还原性,因此久置在空气中会被氧气氧化得到单质硫,反应方程式为![]() ,相当于非金属间的置换反应,因此氧的非金属性强于硫,这也可以从结构上看出:氧和硫同主族不同周期,硫的半径比氧大,因此得电子能力相对较弱。除此以外还可从氢化物的稳定性、互化物的化合价等方面来判断;
,相当于非金属间的置换反应,因此氧的非金属性强于硫,这也可以从结构上看出:氧和硫同主族不同周期,硫的半径比氧大,因此得电子能力相对较弱。除此以外还可从氢化物的稳定性、互化物的化合价等方面来判断;
(2)我们可以近似认为![]() 中每个硫为+2价,再来看选项:
中每个硫为+2价,再来看选项:
a.0价和-2价的硫不可能反应得到+2价,a项错误;
b.+4价和0价的硫,可能发生归中反应得到+2价,b项正确;
c.+4价和+6价的硫,不可能反应得到+2价,c项错误;
d.-2价和+4价的硫,可能发生归中反应得到+2价,d项正确,
答案选bd;
(3)a.二氧化硫会部分溶解在水中,导致实际测得的体积偏小,a项错误;
b.反应速率越快,溶液中就越快出现硫的浑浊,因此可以用来探究反应速率,b项正确;
c.浓硫酸氧化性较强,和稀硫酸的反应产物不一样,不同的反应本身速率就不同,c项错误;
答案选b;
(4)![]() 被还原为单质硫,则
被还原为单质硫,则![]() 被氧化,结合其氧化产物是一种无毒气体,推测为
被氧化,结合其氧化产物是一种无毒气体,推测为![]() ,注意在题目给的温度下硫是液体,据此写出热化学方程式:
,注意在题目给的温度下硫是液体,据此写出热化学方程式: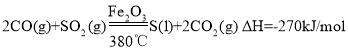 ;
;
(5)根据图2我们发现,![]() 能在较低的温度下获得较高的转化率,因此效率最高,同时可以节约能耗。
能在较低的温度下获得较高的转化率,因此效率最高,同时可以节约能耗。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答问题:
① | |||||||
② | |||||||
③ | ④ | ⑤ | |||||
⑥ |
(1)①和②形成的最简单化合物的结构式是__________,该分子的空间构型是________。
(2)⑤元素位于元素周期表 ___ ,最外层电子的排布式 _________ ,原子核外有 _______种能量不同的电子。CCl4 是一种常见的有机溶剂,判断其属于 _______ (填“极性”、“非极性”)共价键,_________ 分子(填“极性”、“非极性”)。
(3)某元素3P亚层上只有一个电子,判断其离子与②,⑤离子半径大小 ______ (用微粒符号表示),写出该元素单质与元素③最高价氧化物对应水合物反应的化学方程式:________。
(4)设计一个实验方法:比较⑤与⑥单质氧化性的强弱,填入下表。
实验步骤 | ________ |
实验现象 | ________ |
实验原理 | ________ |
实验结论 | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】矿物斜长石(主要成份为KAlSi3O8)在一定温度范围内用氯化钠熔浸可制得氯化钾,反应原理是NaCl(l)+KAlSi3O8(s)![]() KCl(l)+NaAlSi3O8(s)。
KCl(l)+NaAlSi3O8(s)。
(1)氯原子最外层的电子排布式___;氧原子核外电子的轨道式___;铝原子核外有___种不同能量的电子。
(2)上述反应涉及的元素中,原子半径最大的是___。该反应中位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,该元素是___;从原子结构方面去分析钠元素的金属性强于铝元素的原因是___。
(3)为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量的百分率)与温度的关系,进行对照实验(保持其它条件不变),获得如下数据:
时间(h) 熔出率 温度 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 | 5.0 |
860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 | 0.690 |
950℃ | 0.669 | 0.714 | 0.710 | 0.714 | 0.714 | ― |
①分析以上数据可以得出,氯化钠熔浸钾长石是___(填“放热”或“吸热”)反应。
②950℃时,欲提高熔出钾的速率可以采取的措施是___(选填编号)。
a.充分搅拌 b.延长反应时间
c.增大反应体系的压强 d.将钾长石粉粹成更小的颗粒
(2)该方法制得KCl提纯后可用来冶炼金属钾。反应Na(l)+KCl(l)![]() NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法是否能说明钠比钾更活泼?___,(填“能说明”或“不能说明”)原因是___。
NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法是否能说明钠比钾更活泼?___,(填“能说明”或“不能说明”)原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,把SiO2细粉放入蒸馏水中,搅拌至平衡,生成H4SiO4溶液(SiO2+2H2OH4SiO4),该反应平衡常数K随温度的变化如图示,搅拌1小时,测得H4SiO4的质量分数为0.01%(溶液密度为1.0g/mL),下列分析正确的是( )
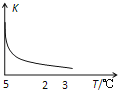
A.该反应平衡常数的表达式为K=c(H4SiO4)
B.该生成H4SiO4的反应为吸热反应
C.用H4SiO4表示的反应速率为1.04×10﹣2mol/(Lh)
D.若K值变大,在平衡移动时逆反应速率先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表中的部分元素,请回答下列有关问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
(1)写出下列元素的符号:①______,⑥______,⑦______。
(2)上述表中的元素中,最活泼的金属元素是______(填元素符号,下同),非金属性最强的元素是______,最不活泼的元素是______。
(3)上述表中元素的最高价氧化物对应的水化物中,酸性最强的是______(填化学式,下同),碱性最强的是______,属于两性氢氧化物的是______,写出这三种物质之间相互反应的化学方程式:______,______,______。
(4)上述表中的元素(不考虑0族元素)中,原子半径最小的是______(填元素符号,下同),原子半径最大的是______。
(5)在③与④中,化学性质较活的是______(填元素符号);在⑧与中,其单质的氧化性较强的是______(填元素符号),请设计实验加以证明:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素的原子结构,回答下列问题:
五种元素的原子结构,回答下列问题:
(1)只有![]() 层与
层与![]() 层的原子有______;
层的原子有______;
(2)含有![]() 层的原子有______;
层的原子有______;
(3)最外层电子数相同的原子有______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷分子是以碳原子为中心的正四面体结构,而不是平面正方形结构。可佐证该说法的事实是( )
A.![]() 只有一种结构B.
只有一种结构B.![]() 只有一种结构
只有一种结构
C.![]() 只有一种结构D.
只有一种结构D.![]() 的四个价键的键长、键角、键能完全相同
的四个价键的键长、键角、键能完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。
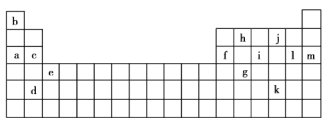
(1)a和c的I1大小关系是______大于______。(填字母)
(2)上述元素中,原子中未成对电子数最多的是______(填字母),写出该元素基态原子的核外电子排布式:______。
(3)根据下表所提供的电离能数据,回答下列问题。
锂 | X | Y | |
I1 | 520 | 496 | 580 |
I2 | 7296 | 4570 | 1820 |
I3 | 11799 | 6920 | 2750 |
I4 | 9550 | 11600 |
①表中X可能为以上13种元素中的______(填字母)元素。用元素符号表示![]() 和j形成的一种化合物的化学式:______。
和j形成的一种化合物的化学式:______。
②Y是周期表中第______族元素。
③以上13种元素中,______(填字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸H2B在水溶液中存在下列关系:
①H2B=H++HB-,②HB-![]() H++B2-,则下列说法中一定不正确的是
H++B2-,则下列说法中一定不正确的是
A.NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
B.在Na2B溶液中一定有:c(Na+)=2[c(B2-)+c(HB-)+c(H2B)]
C.NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+2c(B2-)
D.在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com