
 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等.下列说法不正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等.下列说法不正确的是( )| A、原子半径:Y>Z>W |
| B、一定条件下,Y可置换出X |
| C、气态氢化物稳定性:Z>W |
| D、熔点YW2>XW4 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、不能发生丁达尔效应的分散系有氯化钠溶液、水等 |
| B、向煮沸的1mol/LNaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| C、可吸入颗粒(直径在10-7m以上)形成气溶胶,对人类健康危害极大 |
| D、FeCl3溶液与Fe(OH)3胶体可以用丁达尔效应鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用钠、镁分别与水反应,可证明钠、镁的金属性强弱 |
| B、用氯化镁、氯化铝分别与过量浓氨水反应,可证明镁、铝的金属性强弱 |
| C、用铁、石墨与硫酸铜溶液组成原电池,可证明铁、铜的金属性强弱 |
| D、把氯气通入到硫化钠的水溶液中,看到淡黄色沉淀,可证明氯气、硫的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

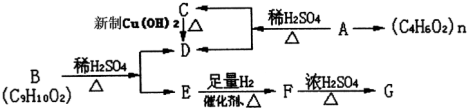
查看答案和解析>>
科目:高中化学 来源: 题型:
 用如图所示装置(夹持仪器已省略)进行实验,E为分液漏斗活塞.将液体A逐滴加入到固体B 中,请回答下列问题:
用如图所示装置(夹持仪器已省略)进行实验,E为分液漏斗活塞.将液体A逐滴加入到固体B 中,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
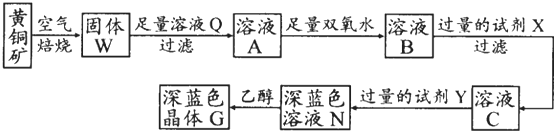
| Fe(OH)2 | Cu(OH)2 | Fe(OH)3 | |
| Ksp | 8.0×1016 | 2.2×1022 | 4.0×1038 |
| 完全沉淀pH | ≥9.6 | ≥6.4 | ≥3.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com