
【题目】如图为1mol SO2Cl2(g)和1mol SCl2(g)反应生成SOCl2(g)过程中的能量变化示意图,已知E1=x kJmol﹣1、E2=y kJmol﹣1 , 下列有关说法中正确的是( ) 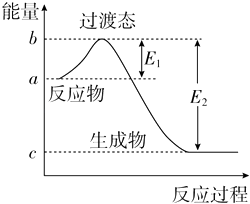
A.若在反应体系中加入催化剂,E1不变
B.若在反应体系中加入催化剂,△H减小
C.反应的活化能等于y kJmol﹣1
D.1 mol SO2Cl2(g)和1 mol SCl2(g)反应生成SOCl2(g)的△H=(x﹣y) kJmol﹣1
【答案】D
【解析】解:催化剂能降低反应的活化能,所以E1变小,但催化剂不会改变化学反应的反应热,所以△H不变,反应热等于反应物的键能总和与生成物的键能总和之差,即△H=E1﹣E2 , A.若在反应体系中加入催化剂,E1变小,故A错误;
B.催化剂不会改变化学反应的反应热,所以△H不变,故B错误;
C.由图可知,反应的活化能等于E1=x kJmol﹣1 , 故C错误;
D.1 mol SO2Cl2(g)和1 mol SCl2(g)反应生成SOCl2(g)的△H=E1﹣E2=(x﹣y) kJmol﹣1 , 故D正确;
故选D.
【考点精析】本题主要考查了反应热和焓变的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.硅是良好的半导体材料,常用于制造光导纤维
B.高炉炼铁原料有铁矿石、黏土、空气和石灰石
C.制备水泥和玻璃的主要原料都有石灰石
D.煤在空气中加强热得到焦炭、煤焦油、焦炉气、粗氨水等产品的过程叫做煤的干馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl﹣、SO42﹣、Br﹣、CO32﹣HCO3﹣等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
(1)火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图所示: 
(i)天然海水的pH≈8,呈弱碱性.用离子方程式解释主要原因 .
(ii)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是;氧化后的“海水”需要用大量的天然海水与之混后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸.
(iii)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=(用含硫微粒浓度的代数式表示).
(iv)相同物质的量的SO2与NH3溶于水发生反应的离子方程式为 , 所得溶液中c(H+)﹣c(OH﹣)=(填字母编号).
A.c(SO32﹣)﹣c(H2SO3) B.c(SO32﹣)+c(NH3 . H2O)﹣c(H2SO3)
C.c(HSO3﹣)+c(SO32﹣)﹣c(NH4+) D.c(HSO3﹣)+2c(SO32﹣)﹣c(NH4+)
(2)重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g/mL)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol/L.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
难溶 | AgI | AgOH | Ag2S | pbI2 | Pb(OH)2 | PbS |
Ksp | 8.3×10﹣17 | 5.6×10﹣8 | 6.3×10﹣50 | 7.1×10﹣9 | 1.2×10﹣15 | 3.4×10﹣28 |
(i)你认为往废水中投入(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KI D.Ca(OH)2
(ii)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)= .
(iii)如果用食盐处理只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%(ρ≈1gmL﹣1).若环境要求排放标准为c(Ag+)低于1.0×10﹣8mol/L,问该工厂处理后的废水中c(Ag+)= . (已知KSP(AgCl)=1.8×10﹣10)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应及平衡常数 | 温度/℃ | ||
500 | 800 | ||
①2H2(g)+CO(g)CH3OH(g)△H1 | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g)CO(g)+H2O(g)△H2 | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g)CH3OH(g)+H2O(g)△H3 | K3 | ||
(1)反应②的反应热△H20(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)K(B) (填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=(用K1、K2表示).500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是; 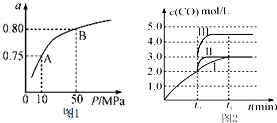
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO﹣),用含a和b的代数式表示该混合溶液中乙酸的电离常数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示为高温超导领域里的一种化合物——钙钛矿晶体结构,该结构是具有代表性的最小重复单元。
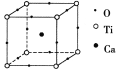
(1)在该物质的晶体结构中,每个钛离子周围与它最近且距离相等的钛离子、钙离子各有__________个、__________个。
(2)若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构如图中正方体边长(钛原子之间的距离)为d nm(1 nm=1×10-9 m),则该晶体的密度为__________g/cm3(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有(如图)。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。
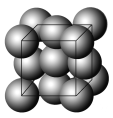
(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_______。
(3)一个晶胞的体积是多少?
(4)金晶体的密度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的下列说法中正确的是( )
A.晶体中分子间作用力越大,分子越稳定
B.氯化钠熔化时离子键未被削弱
C.冰熔化时水分子中共价键发生断裂
D.原子晶体中共价键越强,熔点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组溶液混合后,溶液一定呈中性的是( )
A.等体积、等物质的量浓度的氨水与盐酸混合
B.pH之和为14的氨水与硝酸等体积混合
C.pH之和为14的Ba(OH)2溶液与NaHSO4溶液等体积混合
D.等体积、等物质的量浓度的Ca(OH)2溶液与Na2CO3溶液混合
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com